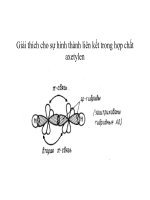
Bài giảng Hóa học vô cơ
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (1.49 MB, 98 trang )
HịA HC VỌ C
1
CÁC NGUYÊN T KIM LOI
KHI S
2
MC TIÊU
1. Xác đnh đưc v trí vƠ đặc điểm về cấu trúc
electron ca các kim loi phơn nhóm IA, IIA
2. Liệt kê đưc một s tính chất hoá hc ca các
đn chất
3. Viết đưc phưng trình phản ng ca các hp
chất điển hình ca chúng
4. Kể ra đưc một s ng dng vƠ các kim loi
vai trò sinh hc ca đn chất vƠ hp chất ca
trên.
3
I. Kim loi nhóm IA - KLK (Li, Na, K, Rb, Cs, Fr)
1. V trí và đặc điểm
- Electron hóa trị: ns
1
- Năng lượng ion hóa I
1
nhỏ (4 - 5eV) nên dễ mất 1e tạo
ion M
+
thể hiện tính khử mạnh
- nhiệt độ lớn hơn nhiệt độ sôi, hơi của kim loại kiềm
chứa khoảng 1% các phân tử M
2
- Khi bị đốt cháy, KLK và hợp chất cho ngọn lửa có
màu: * Li – đỏ son * Rb – hồng
* Na – vàng * Cs – xanh lam
* K – tím
4
2. Tính chất hóa hc
2.1. Phản ứng với oxy:
- Phản ứng nhiệt độ thưng tạo oxyd
4M + O
2
→ 2 M
2
O
- Phản ứng nhiệt độ cao:
2Na + O
2
→ Na
2
O
2
( peroxyd)
K (Rb,Cs) + O
2
→ KO
2
(superoxyd)
2.2. Phản ứng với Hydro
2M + H
2
→ 2MH
MH + H
2
O → MOH + 1/2H
2
(rất mạnh)
5
- Dựa vào lượng H
2
giải phóng ra, sử dụng MH để định
lượng nước trong hợp chất hữu cơ.
2.3. Phản ứng với H
2
O
2M + 2H
2
O → 2MOH + H
2
- Li pứ êm dịu
- Na pứ nhanh
- K pứ mạnh kèm ngọn lửa
- Rb, Cs nổ khi tiếp xúc với nước.
6
3. Một s hp chất
3.1. Peroxyd
- phản ứng mạnh với nước giải phóng H
2
O
2
Na
2
O
2
+ H
2
O → H
2
O
2
+ 2NaOH
( H
2
O
2
→ H
2
O + O
2
trong MT kiềm)
- phản ứng với acid:
Na
2
O
2
+ H
2
SO
4
→ Na
2
SO
4
+ H
2
O
2
- phản ứng với CO
2
Na
2
O
2
+ CO
2
→ Na
2
CO
3
+ 1/2O
2
7
3.2. Superoxyd:
- phản ứng với C, CO, NO
4KO
2
+ 2C → 2K
2
CO
3
+ O
2
2KO
2
+ CO → K
2
CO
3
+ O
2
2KO
2
+ 3NO → KNO
3
+ KNO
2
+ NO
2
- pứ với H
2
O
2KO
2
+ 2H
2
O → KOH + H
2
O
2
+ O
2
- phản ứng với CO
2
2KO
2
+ CO
2
→ K
2
CO
3
+ 3/2O
2
- phản ứng với acid
2KO
2
+ H
2
SO
4
→ K
2
SO
4
+ H
2
O
2
+ O
2
8
3.3. Hydroxyd
- Dễ tan trong nước tạo base mạnh
- Bền nhiệt, không bị phân hủy nhiệt ngay cả khi nóng
chảy ( trừ LiOH)
3.4. Muối
- Là các hợp chất ion
- Dễ tan trong nước
9
Mui MHCO
3
Mui M
2
CO
3
Dễ tan (trừ NaHCO
3
)
Bền nhiệt độ thưng,
dễ phân hủy khi bị đun
nóng
Có thể tách ra dạng tự
do
Dễ tan
Bền nhiệt, không bị phân
hủy nhiệt độ nóng
chảy
10
4. Vai trò sinh hc ca các nguyên t KLK
4.1. Na
+
- Tham gia vào quá trình điều hòa thăng bằng acid-
base của cơ thể, tham gia hệ thống đệm trong máu.
- Duy trì áp suất thẩm thấu của máu và các dịch tổ
chức.
- Là thành phần chính của các cation trong dịch gian
bào.
- Liên quan đến hoạt động bình thưng của cơ và sự
thẩm thấu qua màng tế bào.
- Nhu cầu dạng Na
+
dạng NaCl của ngưi khoảng 5-
15g/ngày.
11
4.2. K
+
- Là cation chủ chốt của dịch nội bào, là thành phần
quan trọng của dịch gian bào.
-Tham gia dẫn truyền xung động thần kinh, điều
hòa sự co bóp của cơ tim và cơ xương.
- Tham gia hệ thống đệm của tế bào, hoạt hóa nhiều
enzym.
- Chế độ ăn bình thưng cần 4g K/ngày
12
5. ng dng trong y hc ca các nguyên t KLK
5.1. Na
* NaCl 0,9% (dd muối đẳng trương):
- Thuốc truyền tĩnh mạch bổ xung muối, nước trong
trưng hợp tiêu chảy mất nước, mất máu, sốt cao.
- Có tác dụng sát trùng
* NaHCO
3
:
- thuốc muối dạ dày
- chữa nhiệt miệng
- tá dược trong một số loại thuốc
- thành phần ozesol
13
5.2. K
• KCl dạng bột hay thuốc tiêm tĩnh mạch nồng độ ≤
40mEg/lit điều trị trong trưng hợp cơ thể thiếu hụt
kali.
• KBr: thuốc an thần, chữa bệnh động kinh.
• Điều trị tiêu chảy mất nước, dùng phối hợp KCl,
NaCl, NaHCO
3
với glucose.
14
II. Kim loi nhóm IIA - Kim loi Kiềm thổ
(Be, Mg, Ca, Sr, Ba, Ra)
1. V trí và đặc điểm
- Electron hóa trị: ns
2
- Hầu hết các hợp chất đều là hợp chất ion (trừ Be).
- Khi bị đốt cháy, KL kiềm thổ và hợp chất cho ngọn lửa có
màu:
* Ca – đỏ cam
* Sr – đỏ
* Ba – lục.
15
2. Tính chất hóa hc
2.1. Phản ứng với oxy:
- nhiệt độ thưng, Be và Mg bền trong không
khí, các KL khác bị oxy hóa nhanh chóng tạo oxyd.
- Phản ứng nhiệt độ cao Ba có thể cho BaO
2
:
Ba + O
2
→ BaO
2
( peroxyd)
2.2. Phản ứng với nước:
- Mg pứ chậm với nước nóng do tạo lớp hydroxyd
bền bảo vệ:
Mg + H
2
O → Mg(OH)
2
+ H
2
Mg(OH)
2
+ 2NH
4
Cl → MgCl
2
+ 2NH
3
+
2H
2
O
- Các kim loại khác pứ dễ dàng với nước nhiệt độ
thưng.
16
3. Một s hp chất
3.1. Peroxyd
- Tác dụng với acid tạo H
2
O
2
BaO
2
+ H
2
SO
4
→ H
2
O
2
+ BaSO
4
- Tác dụng với chất khử
BaO
2
+ H
2
→ Ba(OH)
2
2BaO
2
+ S → 2BaO + SO
2
-
Tác dụng với chất oxi hóa
BaO
2
+ HgCl
2
→ BaCl
2
+ Hg + O
2
17
3.2. Muối
Muối M(HCO
3
)
2
Muối MCO
3
Dễ
tan, kém bền nhiệt
Khó
tan, kém bền nhiệt
Chỉ
tồn tại trong dung
dịch
Tồn
tại được dạng
tinh
thể
18
4. Vai trò sinh hc ca các nguyên t KLK thổ
4.1. Ca
2+
- Ca
2+
có trong cơ thể với 1 lượng lớn, tập trung chủ
yếu xương và răng (80% Ca
3
(PO
4
)
2
,13% CaCO
3
)
- Tham gia vào quá trình đông máu.
- Kích thích hoạt động của cơ, cơ tim, thần kinh.
- Nhu cầu canxi theo lứa tuổi.
19
4.2. Mg
2+
- Trong cơ thể có 71g, tập trung chủ yếu xương dưới
dạng muối phức của C và P.
- Là một trong các cation chính của các tổ chức đệm.
- Có mặt trong các dịch cơ thể, cơ.
- Kích thích nhu động ruột, tăng tiết mật.
20
5. ng dng trong y hc ca các nguyên t KLK thổ
5.1. Ca
- CaSO
4
.H
2
O (thạch cao nung) dùng bó bột chỉnh hình
- CaBr
2
: an thần, chữa co giật trẻ em
- CaCl
2
5% (tiêm tĩnh mạch): cầm máu, chống co thắt khi
trẻ sơ sinh co giật
- Muối Ca, Na của EDTA: chữa nhiễm độc KL nặng.
21
5.2. Mg
- MgSO
4
(dạng bột): nhuận tràng, thông mật.
- MgSO
4
(dạng tiêm): an thần, ức chế các cơn co thắt.
- Mg(OH)
2
có trong thành phần của thuốc dạ dày
5.3. Ba
- BaSO
4
dùng trong kỹ thuật X - quang.
22
CÁC NGUYÊN T KIM LOI
KHI P
23
MC TIÊU
1. Xác đnh đưc v trí vƠ đặc điểm về cấu trúc
electron ca các kim loi phơn nhóm IIIA, IVA
2. Liệt kê đưc một s tính chất hoá hc ca các
đn chất
3. Viết đưc phưng trình phản ng ca các hp
chất điển hình ca chúng
4. Kể ra đưc một s ng dng vƠ vai trò sinh hc
ca đn chất vƠ hp chất ca các kim loi nói
trên.
24
I. Kim loi nhóm IIIA (Al, Ga, In, Tl)
1. V trí và đặc điểm
- Electron hóa trị: ns
2
np
1
- Số oxy hóa bền: Al
+3
, Tl
+
.
- Có khả năng tạo phức.
25