ngân hàng câu hỏi và đáp án hóa đại cương chương 2 liên kết hóa học và cấu tạo phân tử
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (297.67 KB, 7 trang )
Chương 2: Liên kết hóa học và cấu tạo phân tử
Chương 2:
LIÊN KẾT HOÁ HỌC VÀ CẤU TẠO PHÂN TỬ
I. MỨC ĐỘ BIẾT
Câu 1: Nhận xét nào sau đây đúng khi nói về đặc điểm của liên kết ion:
A. Mỗi ion tạo ra điện trường xung quanh nó, nên liên kết ion xảy ra theo mọi
hướng hay thường nói liên kết ion là liên kết không có hướng.
B. Không bảo hoà, nghĩa là mỗi ion có thể liên kết được nhiều ion xung quanh nó.
C. Liên kết rất bền.
D. Tất cả đều đúng
Câu 2: Phát biểu nào dưới đây chưa chính xác:
A. Độ dài liên kết là khoảng cách 2 hạt nhân nguyên tử liên kết.
B. Năng lượng liên kết là năng lượng cần thiết để phá vỡ liên kết có trong 1 mol
chất.
C. Góc liên kết là góc được tạo bởi 1 nguyên tử liên kết trực tiếp với 2 nguyên tử
D. Độ bội của liên kết bằng số cặp electron góp chung
Câu 3: Phát biểu nào sau đây không phù hợp với lý thuyết liên kết - hóa trị (VB):
A. Liên kết cộng hóa trị được hình thành do sự kết đôi của 2 electron spin trái dấu,
ta nói ở đây có sự xen phủ của 2 obitan nguyên tử.
B. Công hóa trị của một nguyên tố bằng số electron độc thân (ở trạng thái cơ bản
và kích thích)
C. Liên kết cộng hóa trị bền khi mức độ xen phủ lớn.
D. Nitơ có hóa trị 5 trong hợp chất HNO
3
Câu 4: Phát biểu nào dưới đây là đúng:
Sự lai hóa obitan nguyên tử có thể xảy ra giữa:
A. Các obitan nguyên tử có cùng số lượng tử chính n.
B. Các obitan nguyên tử có năng lượng xấp xĩ nhau, có tính chất đối xứng giống
nhau đối với trực nối tâm của 2 nguyên tử.
C. Các obitan nguyên tử có cùng số lượng tử phụ l
D. Các obitan nguyên tử có năng lượng khác nhau
Câu 5: Bản chất của liên kết ion là:
A. Sự dùng chung cặp electron hóa trị
B. Lực tĩnh điện giữa các ion trái dấu
C. Sự xen phủ của các obitan nguyên tử hóa trị
D. Sự chuyển electron từ nguyên tử này sang nguyên tử kia
Câu 6: Mỗi liên kết cộng hóa trị được tạo thành theo phương pháp VB:
A. Bằng 2 electron có các số lượng tử m
s
cùng dấu
B. Bằng sự chuyển elctron từ nguyên tử này sang nguyên tử khác
C. Bằng 2 electron có các số lượng tử m
s
khác dấu
D. Bằng lực tĩnh điện giữa 2 nguyên tử tham gia liên kết
Câu 7: Trạng thái hoá trị của một nguyên tố:
A. Bằng số electron ở lớp ngoài cùng của nguyên tử nguyên tố đó.
B. Bằng số electron ở phân lớp ngoài cùng của nguyên tử nguyên tố đó.
Trang 18
Chương 2: Liên kết hóa học và cấu tạo phân tử
C. Bằng số electron độc thân của nguyên tử nguyên tố đó ở trạng thái cơ bản và
trạng thái kích thích có thể xảy ra khi phản ứng
D. Bằng số electron độc thân của nguyên tử nguyên tố đó ở trạng thái cơ bản
Câu 8: Câu trả lời nào sau đây đúng? Các nguyên tố halogen:
A. Đều có trạng thái hoá trị 1, 2, 3, 4, 5, 6 và 7.
B. Đều có trạng thái hoá trị 1, 3, 5 và 7.
C. Đều có trạng thái hoá trị 1, 2, 3 và 4
D. Đều có trạng thái hoá trị 1, 3, 5 và 7 trừ flo chỉ có hoá trị 1
Câu 9: Nguyên tử Be, B, C trong các phân tử BeH
2
, BF
3
, CH
4
có kiểu lai hóa tương ứng là:
A. sp, sp
2
, sp
3
B. sp, sp
3
, sp
2
C. sp
2
, sp
3
, sp D. sp
3
, sp, sp
2
Câu 10: Trong phân tử BF
3
, nguyên tử B có kiểu lai hóa sp
2
. Vậy dạng hình học của phân
tử BF
3
là:
A. Đường thẳng B. Gấp khúc
C. Tam giác D.Tứ diện
Câu 11: Trong tiểu phân NH
4
+
, nguyên tử N có kiểu lai hóa sp
3
. Vậy dạng hình học của
tiểu phân NH
4
+
là:
A. Đường thẳng B. Gấp khúc
C. Tam giác D.Tứ diện
Câu 12: Cho các phân tử N
2
, CO, HBr, NH
3
, NH
3
BCl
3
, NH
4
NO
2
. Hãy chọn phân tử có
liên kết cho nhận:
A. N
2
, CO, HBr, NH
3
B. NH
3
, NH
3
BCl
3
, NH
4
NO
2
C. CO, NH
3
BCl
3
, NH
4
NO
2
D. CO, HBr, NH
3
, NH
3
BCl
3
Câu 13: Theo quy tắc bát tử, CTCT nào sau đây là phù hợp:
H O
S O
H O
A.
H O O
S
H O O
B.
H O O
S
H O O
C.
D. A, B ñuùng
Câu 14: Phát biểu nào dưới đây là đúng:
Theo lý thuyết MO, độ bền tương đối của các tiêu phân giảm theo dãy:
A.
+−
>>
222
OOO
B.
+−
>>
2
2
2
OOO
C.
−+
>>
222
OOO
D.
−+
>>
2
2
2
OOO
Câu 15: Cấu hình electron viết sau đây:
( )( )
( )
( )
( )
( )
1
*
24
,
2
*
2
xzyxss
πσπσσKK
là phù hợp
với tiểu phân:
A. BO B. CO C. NO D. NO
+
II. MỨC ĐỘ HIỂU
Câu 1: Chỉ ra các hợp chất có liên kết ion:
A. HCl, NH
3
; CH
4
C. FeO, MgS, Al
2
O
3
B. CaO; NaCl, K
2
O D. B, C đều đúng.
Câu 2: Chỉ ra các phân tử có liên kết cộng hóa trị không cực
A. N
2
; NaCl; HCl C. MgO; H
2
O; H
2
S
Trang 19
Chương 2: Liên kết hóa học và cấu tạo phân tử
B. CH
4
; NH
3
; P
2
O
5
D. N
2
, Cl
2
; H
2
Câu 3: Các chất nào sau đây đều là hợp chất cộng hóa trị:
A. KCl, Al
2
O
3
, P
2
O
5
B. CO
2
, H
2
SO
4
, C
2
H
5
OH
C. NaOH, NH
3
, C
6
H
6
D. NaCl, MgO, KNO
3
Câu 4: Phân tử nào dưới đây có cả liên kết ion và liên kết cộng hóa trị:
A. HNO
2
C. NaClO B.CH
2
O D. PH
3
Câu 5: Phân tử nào dưới đây có liên kết phân cực mạnh nhất:
A. Cl
2
O B. NH
3
C. NO D. H
2
Câu 6: X là nguyên tố thuộc chu kỳ 3, nhóm IA; Y là nguyên tố thuộc chu kỳ 2, nhóm
IVA. Hợp chất của X và Y thuộc loại:
A. Hợp chất Ion
B. Hợp chất cộng hóa trị phân cực
C. Hợp chất CHT không phân cực
D. Tùy thuộc vào độ âm điện của nguyên tố.
Câu 7: Hợp chất nào sau đây tuân theo quy tắc bát tử:
A. ZnCl
2
B. Al
2
O
3
C. FeS D. AgNO
3
Câu 8: Các hợp chất nào dưới đây không tuân theo quy tắc bát tử:
A. H
2
S. B. N
2
O
5
. C. PCl
3
. D. SF
6
.
Câu 9: Trong các nguyên tử trung tâm (có gạch dưới) của các phân tử: H
2
O, SO
2
, CH
4
,
BeCl
2
; nguyên tử có trạng thái lai hoá sp là:
A. H
2
O B. SO
2
C. CH
4
D. BeCl
2
Câu 10: Trong các nguyên tử trung tâm (có gạch dưới) của các phân tử: H
2
O, SO
2
, BF
3
,
BeCl
2
; nguyên tử có trạng thái lai hoá sp
3
là:
A. H
2
O B. SO
2
C. BF
3
D. BeCl
2
Câu 11: Nguyên tử A có 20 proton, nguyên tử B có 17 proton.Công thức của hợp chất vá
kiểu liên kết được hình thành giữa hai nguyên tử của hai nguyên tố đó là:
A. AB, liên kết ion B. AB
2
, liên kết ion
C.A
2
B, liên kết ion D.AB
2
, liên kết cộng hoá trị
Câu 12: X có độ âm điện là 0,93. Hợp chất XY là hợp chất Ion. Độ âm điện của Y là :
A. Nhỏ hơn 2,63 B. Lớn hơn 2,63
C. Nhỏ hơn 0,77 D. Lớn hơn 0,77
Câu 13: Mức độ phân cực các liên kết tăng dần theo trật tự nào dưới đây:
A. H
2
S; H
2
O; NH
3
B. NH
3
; H
2
O; H
2
S
C. H
2
O; H
2
S; NH
3
D. H
2
S; NH
3
; H
2
O
Câu 14: Để giải thích cấu tạo của phân tử PCl
5
ta có thể dùng:
A. Quy tắc bát tử
B. Trạng thái kích thích của nguyên tử P
C. Trạng thái kích thích của nguyên tử Cl
D. Cả A, B, C đều đúng
Câu 15: Sự hình thành phân tử Br
2
là do sự xen phủ của:
A. 2 opitan p. B. 2 opitan s.
C. opitan s và opitan p. D. opitan p và opitan d.
III. MỨC ĐỘ VẬN DỤNG
Trang 20
Chương 2: Liên kết hóa học và cấu tạo phân tử
Câu 1: Cấu hình electron của phân tử nitơ là:
A.
( )( )
( )
( ) ( )
( )
112
2
*
2
yxzss
ππσσσKK
B.
( )( )
( )
( ) ( )
22
2
*
2
xzss
πσσσKK
C.
( )( )
( )
( )
( )
24
2
*
2
zxyss
σπσσKK
D. Tất cả đều sai
Câu 2: Theo phương pháp MO, cấu hình electron nào dưới đây đúng cho phân tử NO?
A.
( )( )
( )
( )
( )
( )
1
*
4
,
2
2
*
2
xyxzss
ππσσσKK
B.
( )( )
( )
( )
( )
( )
1
*
4
,
2
2
*
2
yyxzss
ππσσσKK
C.
( )( )
( )
( )
( )
( )
1
*
24
,
2
*
2
xzyxss
πσπσσKK
D. Tất cả đều sai
Câu 3: Theo phương pháp MO, cấu hình electron nào dưới đây đúng cho phân tử CO?
A.
( )( )
( )
( )
( )
2
2
4
,
2
*
2
2
2
z
p
yxss
σπσσKK
B.
( )( )
( )
( )
( )
4
,
2
2
2
*
2
2
2 yxzss
πσσσKK
C.
( )( )
( )
( )
( )
( )
2
*
22
,
2
*
2
2
2 xzyxss
πσπσσKK
D. Tất cả đều sai
Câu 4: Cấu hình electron của phân tử Oxi là:
A.
( )
( )
( )
( )
( ) ( )
11
42
2
2
2
2
*
y
*
xy,xz
*
ss
πππσσσ
B.
( )
( )
( )
( )
( ) ( )
11
24
2
2
2
2
*
y
*
xzy,x
*
ss
ππσπσσ
C.
( )
( )
( )
( )
( )
2
42
2
2
2
2
*
zy,xz
*
ss
σπσσσ
C. Tất cả đều sai
Câu 5: Theo thuyết VB, các công hóa trị mà nguyên tố Telu (Z = 52) có thể biểu lộ là:
A. 2 B. 2, 4, 6 C. 2, 4 D. 2, 4, 6, 8
Câu 6: Trong các nguyên tử sau nguyên tử nào không có cấu hình electron ở trạng thái
kích thích:
A. As (Z = 33) B. Br (Z = 35)
C. Ga (Z = 31) D. Cs (Z = 55)
Câu 7: Trong các nguyên tử sau đây, nguyên tử nào có thê có nhiều cấu hình electron ở
trạng thái kích thích nhất?
A. Sn (Z = 50) B. I (Z = 53)
C. Sb (Z = 51) D. In (Z = 49)
Câu 8: Trong các tiểu phân sau đây, tiểu phân nào có góc liên kết gần bằng 104
0
:
A. SnCl
2
B. OF
2
C. SO
2
D. CO
2
Câu 9: Trong các phân tử sau đây, phân tử nào không tuân theo quy tắc bát tử:
A. BF
3
B. PCl
5
C. NO D. Tất cả đều đúng
Câu 10: Trong các phân tử sau đây, phân tử nào không tồn tại?
A. He
2
B. Be
2
C. Ne
2
D. Tất cả đều không tồn tại
Câu 11: Hợp chất nào sau đây chỉ có liên kết cộng hóa trị
A.Na
2
SO
4
B.CaO C. HClO D.KNO
3
Câu 12: Theo lý thuyết MO, trong các tiêu phân sau đây, tiểu phân nào có bậc liên kết
bằng 1:
A.
+
2
H
B.
2
H
C.
+
2
He
D.
2
He
Câu 13: Theo lý thuyết MO, trong các tiêu phân sau đây, tiểu phân nào có bậc liên kết
bằng 1,5:
Trang 21
Chương 2: Liên kết hóa học và cấu tạo phân tử
A.
−2
2
O
B.
2
O
C.
+
2
O
D.
−
2
O
Câu 14: Theo lý thuyết MO, trong các tiêu phân sau đây, tiểu phân nào có bậc liên kết
bằng 2,5:
A.
2
O
B.
NO
C.
CO
D.
BN
Câu 15: Phát biểu nào dưới đây là đúng:
A. CO
2
và SO
2
đều có cấu trúc thẳng hàng.
B. CH
4
và NH
4
+
đều có cấu trúc tứ diện đều.
C.
−2
3
CO
và
−2
3
SO
đều có cấu trúc phẳng
D. H
2
O và BeCl
2
đều có cấu trúc gấp khúc
IV. MỨC ĐỘ TỔNG HỢP
Câu 1: Hãy sắp xếp độ bền liên kết và góc liên kết trong phân tử NH
3
, PH
3
, AsH
3
, SbH
3
theo chiều giảm dần:
A. NH
3
> PH
3
> AsH
3
> SbH
3
B. SbH
3
> AsH
3
> PH
3
> NH
3
C. AsH
3
> SbH
3
> PH
3
> NH
3
D. Tất cả đều sai
Câu 2: Trong phân tử HClO
4
có loại liên kết :
A. 1 liên kết Ion, 1 liên kết cộng hóa trị và 3 liên kết phối trí
B. 1 liên kết Ion, 2 liên kết cộng hóa trị và 2 liên kết phối trí
C. 2 liên kết cộng hóa trị và 3 liên kết phối trí
D. 1 liên kết cộng hóa trị và 4 liên kết phối trí
Câu 3: Trong phân tử NaHSO
4
có những loại liên kết nào?
A. Liên kết CHT và liên kết cho nhận
B. Liên kết ion và liên kết cộng hóa trị
C. Liên kết ion và liên kết cho nhận
D. Liên kết CHT – cho nhận – ion
Câu 4: Trong phân tử NH
4
Cl có các loại liên kết :
A. Cộng hóa trị B. Ion C. Cho nhận D. Cả A, B và C
Câu 5: Cấu dạng hình học nào sau đây không đúng:
F F
F
B
A.
F F
F
P
B.
Cl Cl
Cl
Al
C.
F F
O
D.
Câu 6: Tiểu phân nào sau đây có liên kết ngắn nhất:
A. O
2
B.
−2
2
O
C.
−
2
O
D.
+
2
O
Câu 7:
Cho
biết
kết
luận
về
trạng
thái
lai
hóa của
nguyên
tử
trung
tâm
nào
dưới
đ
ây
là đúng
?
A.
C
trong
CO
2
lai
hóa
sp. B.
N
trong
NH
3
lai
hóa
sp
2
.
C.
S
trong
SO
3
lai
hóa
sp
3
.
D.
O
trong
H
2
O
lai
hóa
sp.
Câu 8:
Trong
các
phân
tử
dưới
đ
ây,
phân
tử
nào có
cấu
tạo
hình
học
dạng
tháp
đ
áy
Trang 22
Chương 2: Liên kết hóa học và cấu tạo phân tử
tam giác?
A. BH
3
B. PH
3
C. SO
3
D. AlCl
3
Câu 9: Cho các tiểu: BeF
2
, BF
3
, NF
3
, SnCl
2.
Vậy các góc liên kết có trong các tiêu phân
trên được sắp xếp theo chiều tăng dần là:
A.
2
F BeSnClBFNF <<<
233
B.
3
F NSnClBFBF <<<
223
C.
2
F BeBFSnClNF <<<
323
D. Tất cả đều sai
Câu 10: Chiều dài liên kết của các tiểu phân:
−−+ 2
2222
,,, OOOO
được sắp xếp theo chiều
giảm dần là:
A.
+−−
>>>
222
2
2
OOOO
B.
+−−
>>>
22
2
22
OOOO
C.
−−+
>>>
2
22
2
2
OOOO
D. Tất cả đều sai
Câu 11: Cấu dạng hình học của các tiểu phân nào sau đây theo VSEPR là không đúng:
N
H
H
H
H
A.
B.
C.
O
H
H
H
(+)
(+)
N
H
H
(-)
As
H
H
D.
H
Câu 12: Cấu dạng hình học của các tiểu phân nào sau đây theo VSEPR là đúng:
A. Cl Sn Cl
D.
N
O
N
(-)
N
H
H
B.
H
C. S C N
Câu 13: Trong các tiểu phân: CCl
4
,
+
4
NH
,
−2
4
SO
, NH
3
, các tiểu phân sau đây có cấu trúc
tứ diện đều giống CH
4
:
A. CCl
4
,
+
4
NH
B. CCl
4
,
+
4
NH
,
−2
4
SO
C. CCl
4
D. CCl
4
,
NH
3
Câu 14: Phát biểu nào dưới đây là đúng:
Cho ba phân tử sau: SCl
2
, OF
2
và OCl
2
. Trong các phân tử đó, góc hóa trị xếp tăng dần
theo dãy:
A. OCl
2
< SCl
2
< OF
2
B. OF
2
< OCl
2
< SCl
2
C. OF
2
< SCl
2
< OCl
2
D. SCl
2
< OF
2
< OCl
2
Câu 15: Phát biểu nào dưới đây là đúng:
A. Độ lớn của góc hóa trị HSH của phân tử H
2
S lớn hơn góc hóa trị HOH của phân tử
H
2
O
B. Độ lớn của góc hóa trị HSH của phân tử H
2
S bằng góc hóa trị HOH của phân tử H
2
O
C. Độ lớn của góc hóa trị FOF của phân tử OF
2
lớn hơn góc hóa trị HOH của phân tử H
2
O
D. Độ lớn của góc hóa trị FOF của phân tử OF
2
nhỏ hơn góc hóa trị HOH của phân tử
H
2
O
Trang 23
Chương 2: Liên kết hóa học và cấu tạo phân tử
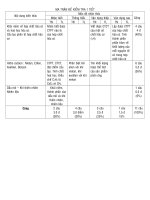
Đáp án chương 2:
LIÊN KẾT HOÁ HỌC VÀ CẤU TẠO PHÂN TỬ
I. MỨC ĐỘ BIẾT: II. MỨC ĐỘ HIỂU:
IIi. MỨC ĐỘ VẬN
DỤNG:
IV. MỨC ĐỘ TỔNG
HỢP :
Câu 1 D Câu 1 D Câu 1 C Câu 1 A
Câu 2 B Câu 2 D Câu 2 C Câu 2 C
Câu 3 D Câu 3 B Câu 3 A Câu 3 D
Câu 4 B Câu 4 C Câu 4 A Câu 4 D
Câu 5 B Câu 5 B Câu 5 B Câu 5 B
Câu 6 C Câu 6 A Câu 6 D Câu 6 D
Câu 7 C Câu 7 B Câu 7 B Câu 7 A
Câu 8 D Câu 8 D Câu 8 B Câu 8 B
Câu 9 A Câu 9 D Câu 9 D Câu 9 C
Câu 10 C Câu 10 A Câu 10 D Câu 10 A
Câu 11 D Câu 11 B Câu 11 C Câu 11 D
Câu 12 C Câu 12 B Câu 12 B Câu 12 C
Câu 13 B Câu 13 D Câu 13 D Câu 13 B
Câu 14 D Câu 14 B Câu 14 B Câu 14 D
Câu 15 C Câu 15 A Câu 15 B Câu 15 D
Trang 24