Tiet 38 su chuyen the cua cac chat
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (106.07 KB, 35 trang )
Bài 38:
SỰ CHUYỂN THỂ
CỦA CÁC CHẤT
ĐẶT VẤN ĐỀ VÀO BÀI:
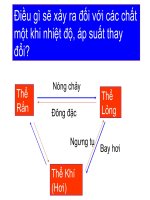
Khi nhiệt độ, áp suất thay đổi, các chất
có thể chuyển từ rắn sang lỏng, họăc
từ lỏng sang khí và ngược lại. Nước có
thể bay hơi họăc đơng lại thành nước
đá, các kim lọai có thể chảy lỏng và
bay hơi.
Vậy sự chuyển thể của các chất có đặc
điểm gì?
Hình ảnh minh họa
I. Sự nóng chảy:
Q trình chuyển từ thể rắn sang
thể lỏng của các chất gọi là sự
nóng chảy.
Q trình chuyển ngược lại từ thể
lỏng sang thể rắn của các chất
gọi là sự đông đặc.
I. Sự nóng chảy:
1. Thí nghiệm:
Nhiệt độ
a. Đun nóng chảy
kim lọai vẽ
232 C
đường biểu diễn sự
biến thiên của nhiệt
Thiếc rắn
độ theo thời gian.
Thiếc lỏng
0
Thời gian
C1: Dựa vào đồ thị hãy mô tả và nhận xét
sự thay đổi nhiệt độ trong q trình nóng
chảy và đơng đặc của thiếc.
Khi đun nóng thiếc nhiệt độ
tăng theo thời gian, đến 2320C
thiếc bắt đầu nóng chảy. Trong suốt
thời gian nóng chảy nhiệt độ khơng
thay đổi 2320C. Sau khi chảy lỏng
hịan tồn thì nhiệt độ lại tiếp tục
tăng.
I. Sự nóng chảy:
1. Thí nghiệm:
b. Kết luận:
* Mỗi chất rắn kết tinh (ứng với một cấu trúc
tinh thể) có một nhiệt độ nóng chảy khơng đổi
xác định ở mỗi áp suất cho trước.
* Các chất rắn vơ định hình (thủy tinh, nhựa
dẻo, sáp nến, …) khơng có nhiệt độ nóng
chảy xác định.
Nhiệt độ nóng chảy của một số chất:
Chất rắn
Tc(0C)
Ni ken
Sắt
Thép
Đồng đỏ
Vàng
Bạc
Nhơm
Chì
Thiếc
Nước đá
1452
1530
1300
1083
1063
960
659
327
232
0
I. Sự nóng chảy:
2. Nhiệt nóng chảy:
Nhiệt lượng cung cấp cho chất rắn
trong q trình nóng chảy gọi là nhiệt
nóng chảy của chất rắn đó.
Q = λm
λ là nhiệt nóng chảy riêng, phụ thuộc
vào bản chất của chất rắn, đơn vị đo
là: J/Kg
I. Sự nóng chảy:
2. Nhiệt nóng chảy:
Nhiệt nóng chảy riêng
của một chất rắn có
độ lớn bằng nhiệt
lượng cần cung cấp
để làm nóng chảy
hịan tịan 1kg chất
rắn đó ở nhiệt độ
nóng chảy.
Chất rắn
λ (J/Kg)
Nước đá
Nhơm
Sắt
Chì
Bạc
Vàng
Thiếc
3,33.105
3,97.105
2,72.105
0,25.105
0,88.105
0,64.105
0,59.105
I. Sự nóng chảy:
3. Ứng dụng:
* Đúc các chi tiết máy, đúc tượng,
đúc chuông.
* Lyện kim.
II. Sự bay hơi:
Quá trình chuyển từ thể lỏng sang thể
khí ở bề mặt chất lỏng gọi là sự bay
hơi.
Ngược lại, q trình chuyển từ thể
khí sang thể lỏng gọi là sự ngưng tụ.
II. Sự bay hơi:
1. Thí nghiệm:
a. * Đổ một lớp nước lên trên mặt đĩa nhôm.
Thổi nhẹ lên mặt nước này hoặc hơ nóng đĩa
này, ta thấy lớp nước dần biến mất: nước đã
bốc thành hơi bay vào khơng khí.
* Nếu đặt bản thủy tinh gần miệng cốc nước
nóng, ta thấy trên mặt bản thủy tinh xuất hiện
các giọt nước : hơi nước từ cốc bay lên đã bay
lên đọng thành nước.
II. Sự bay hơi:
1. Thí nghiệm:
b. * Nguyên nhân là do một số phân tử chất lỏng
ở mặt thống có động năng lớn nên thắng được
công cản do lực hút của các phận tử chất lỏng
nằm trên mặt thoáng để thoát ra khỏi mặt thoáng
và trở thành phân tử hơi của chính chất ấy.
* Đồng thời khi đó cũng xảy ra cũng xảy ra quá
trình ngưng tụ do một số phân tử hơi chuyển động
nhiệt hỗn loạn va chạm vào mặt thoáng và bị các
phân tử chất lỏng nằm trên mặt thoáng hút.
C2: Nhiệt độ của khối chất lỏng khi
bay hơi tăng hay giảm? Tại sao?
* Khi chất lỏng bay hơi: nhiệt độ tăng
do các phân tử chất lỏng có động
năng lớn thóat ra khỏi bề mặt của
khối chất lỏng giảm bớt năng
lượng nhiệt độ của nó giảm.
II. Sự bay hơi:
1. Thí nghiệm:
c. * Sự ngưng tụ luôn xảy ra kèm theo sự
bay hơi.
* Nếu số phân tử thóat ra khỏi bề mặt chất
lỏng nhiều hơn số phân tử hơi bị hút vào
ta nói chất lỏng bị bay hơi.
* Nếu số phân tử hơi bị hút vào nhiều hơn
số phân tử chất lỏng thóat khỏi bề mặt chất
lỏng ta nói chất hơi bị ngưng tụ.
C3: Tốc độ bay hơi phụ thuộc như thế
nào vào nhiệt độ, diện tích bề mặt và áp
suất phía trên bề mặt chất lỏng? Tại sao?
* Khi nhiệt độ tăng số phân tử chuyển
động nhiệt có động năng lớn càng
nhiều tốc độ bay hơi càng nhanh.
* Khi diện tích mặt thóang càng rộng và
áp suất hơi trên mặt chất lỏng càng nhỏ
tốc độ bay hơi càng tăng.
II. Sự bay hơi:
2. Hơi khơ và hơi bão hịa:
* Khi tốc độ bay hơi lớn hơn tốc độ ngưng
tụ, áp suất hơi tăng dần và hơi ở phía trên
bề mặt chất lỏng là hơi khô. Hơi khô tuân
theo định luật Bôi lơ – Mariôt.
II. Sự bay hơi:
2. Hơi khơ và hơi bão hịa:
* Khi tốc độ bay hơi bằng tốc độ ngưng tụ,
hơi ở phía trên bề mặt chất lỏng là hơi bão
hịa có áp suất đạt giá trị cực đại gọi là áp
suất hơi bão hịa. Áp suất hơi bão hịa
khơng phụ thuộc thể tích và khơng tn
theo định luật Bơi lơ – Mariơt, nó chỉ phụ
thuộc vào bản chất và nhiệt độ của chất
lỏng.
C4: Tại sao áp suất hơi bão hịa
khơng phụ thuộc thể tích và lại tăng
theo nhiệt độ?
Khi nhiệt độ tăng tốc độ bay hơi lớn áp
suất hơi bão hịa tăng.
Khi thể tích chứa hơi bão hịa giảm áp suất
hơi bão hòa tăng làm tăng tốc độ ngưng
tụ, giảm tốc độ bay hơi trạng thái cân
bằng động áp suất hơi bão hòa giữ
nguyên.
II. Sự bay hơi:
3. Ứng dụng:
* Vòng tuần hòan của nước trong
thiên nhiên.
* Trong ngành sản xuất muối.
* Trong kỹ thuật làm lạnh.
III. Sự sơi:
Q trình chuyển từ thể lỏng sang
thể khí xảy ra ở cả bên trong và
trên bề mặt chất lỏng gọi là sự sôi.
III. Sự sơi:
1. Thí nghiệm:
Dưới áp suất chuẩn, mỗi chất lỏng sôi ở
một nhiệt độ xác định và không thay đổi.
Nhiệt dộ sôi của chất lỏng phụ thuộc áp
suất chất khí ở phía trên bề mặt chất lỏng.
Áp suất chất khí càng lớn, nhiệt độ sơi của
chất lỏng càng cao.
Bảng nhiệt độ sôi:
Một số chất
Chất lỏng
Ts( C)
Rượu
Nước
Xăng
Dầu hỏa
78,3
100
80,2
290
0
Của nước
Áp suất
(atm)
Ts(0C)
0,1
0,5
1
5
10
45
81
100
151
181
III. Sự sơi:
2. Nhiệt hóa hơi:
Nhiệt lượng cung cấp cho khối chất
lỏng trong q trình sơi gọi là nhiệt
hóa hơi của chất lỏng ở nhiệt độ sơi.
Q = L.m
Trong đó L là nhiệt hóa hơi riêng
(J/kg).