Bài giảng chế biến khí : QUÁ TRÌNH HALOGEN HÓA part 4 doc
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (795.65 KB, 5 trang )
hệ thống trung hòa (d) bằng dung dịch NaOH để tiếp tục loại bỏ vết khí HCl còn lại.
Sau đó hỗn hợp khí sản phẩm được nén bởi máy nén (e), làm lạnh ở (f), làm khô ở
(g) và ngưng tụ ở thiết bị (h). Khí không ngưng gồm CH
4
dư và một ít CH
3
Cl cho
quay lại thiết bị phản ứng (a). Phần lỏng thu được đem đi phân tách bằng chưng cất.
Thành phần sản phẩm gồm CH
2
Cl
2
(70%m), CHCl
3
(27%m) và rất ít CCl
4
(3%m) và có thể có chứa CH
3
Cl nếu cần.
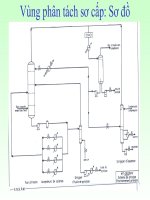
Hình 1: Sơ đồ Clo hóa CH
4
bằng phương pháp Hoechst
(sản xuất CH
2
Cl
2
và CHCl
3
)
a. thiết bị phản ứng e. máy nén
b. thiết bị làm lạnh bằng không khí f. thiết bị ngưng tụ bằng nước
c. tháp hấp thụ khí HCl g. hệ thống làm khô khí
d. hệ thống trung hòa
h. hệ thống ngưng tụ thứ cấp và chứa sản phẩm thô
i. các tháp chưng cất thu hồi CH
3
Cl, CH
2
Cl
2
, CHCl
3
, CCl
4
.
d. Sơ đồ quá trình Hoechst sản xuất CCl
4
16
e
Cl
2
CH
4
f
b
CH
3
Cl
CH
2
Cl
CHCl
3
CCl
4
i i i
h
dcc
a
g
HCl
31%
HCl
20%
NaOH
Sơ đồ công nghệ gồm 6 thiết bị phản ứng nối tiếp nhau. Nguyên tắc của
phương pháp là nguyên liệu cho vào tháp thứ nhất còn khí Cl
2
được cho vào từng
thiết bị phản ứng.
Hình 2: Sơ đồ sản xuất CCl
4
bằng quá trình Clo hóa CH
4
(Hoechst)
a. hệ 6 thiết bị phản ứng e. Bể chứa sản phẩm thô
b. thiết bị làm lạnh f. Tháp tách nước
c. thiết bị ngưng tụ bằng không khí g. bể chứa trung gian
d. thiết bị ngưng tụ thứ cấp h. tháp tách sản phẩm nhẹ cuối
i. tháp làm sạch CCl
4
m. thiết bị ngưng tụ hơi
j. tháp tách sản phẩm nặng cuối n. thiết bị làm lạnh và tách pha
l. hấp thụ đoạn nhiệt HCl o. thiết bị phân tách khí thải
17
nước
thải
CCl
4
HCl
31%
Phần
nhẹ
(CH
3
Cl)
CH
4
Cl
2
H
2
O
H
2
O
HCl
20%
cbb
b
a
a
a
d
l
m
n
o
khí thải
đi làm
sạch
f
e
g
h i
j
Phần nặng
Nguyên liệu với lượng dư CH
4
(và CH
3
Cl hồi lưu) và một phần Cl
2
vào thiết
bị phản ứng thứ nhất, toàn bộ lượng Clo sẽ chuyển hóa ở 400
o
C. Hỗn hợp khí sản
phẩm ở thiết bị thứ nhất được làm lạnh và đưa vào thiết bị phản ứng thứ hai có bổ
sung lượng Cl
2
cần thiết. Sự thêm Cl
2
từng bậc với sự làm lạnh gián đoạn đến thiết
bị phản ứng cuối cùng với tỷ lệ CH
4
: Cl
2
= 1:4. Hỗn hợp khí đi ra sẽ được làm lạnh
2 bậc đến -20
o
C. Phần lỏng thu được chủ yếu là CCl
4
được đưa về bể chứa sản
phẩm thô (e). Hỗn hợp khí có chứa HCl đưa sang thiết bị hấp thụ đoạn nhiệt (l)
bằng H
2
O hoặc bằng dung dịch HCl 20%, ở đáy thu được HCl 31%. Hơi lấy ra ở
đỉnh sẽ được ngưng tụ ở thiết bị (m) bằng dòng lưu chất lạnh. Đa số CH
3
Cl thoát ra
ở thiết bị làm lạnh và phân tách pha (n). Nước rửa ở (m) được làm sạch trước khi
loại bỏ. Khí thải làm sạch trước khi thải ra môi trường.
Lỏng thu được đưa về thùng chứa sản phẩm thô còn chứa thành phần khí tự
do CH
3
Cl, Cl
2
, HCl được đưa sang thiết bị tách nước (f), các vết nước thu hồi bằng
chưng cất và đưa về thiết bị hấp thụ HCl. Sản phẩm tiếp tục đưa sang tháp tách sản
phẩm nhẹ (h); ở đỉnh thu được sản phẩm nhẹ hồi lưu về thiết bị phản ứng , phần
lỏng ở đáy (h) được đưa sang thiết bị làm sạch và tách sản phẩm CCl
4
ở thiết bị (i)
và (j). Cặn cuối cùng với thành phần chứa 2 ÷ 3% m CCl
4
dùng để sản xuất
hexacloetan, tetracloetylen, tricloetylen.
1.4. Quá trình clo hóa etan
1.4.1. Sản phẩm của quá trình clo hóa etan: sản phẩm ứng dụng chính là C
2
H
5
Cl
• Tính chất của Clorua etan: Ở điều kiện thường, là chất khí không màu, hóa
lỏng ở 12,2
o
C, tan ít trong nước.
• Ứng dụng:
- làm dung môi trích ly cho cho chất thơm, dùng trong y học
- làm tác nhân etyl hóa
- trước đây dùng để sản xuất TEL
1.4.2. Các phương pháp sản xuất C
2
H
5
Cl:
- clo hóa etan
18
- hydroclo hóa etylen
- kết hợp clo hóa và hydroclo hóa (quá trình Shell)
Sơ đồ công nghệ quá trình Shell:
Quá trình thực hiện theo phản ứng sau:
CH
3
- CH
3
+ Cl
2
→ CH
3
CH
2
Cl + HCl
CH
2
= CH
2
+ HCl → CH
3
CH
2
Cl
CH
3
- CH
3
+ CH
2
= CH
2
+ Cl
2
→ 2CH
3
CH
2
Cl
Hình 3: Sơ đồcông nghệ Shell sản xuất C
2
H
5
Cl
1. thiết bị gia nhiệt
2. thiết bị clo hóa với C
2
H
6
: Cl
2
= 4:1 và t = 400÷450
o
C
3. thiết bị trao đổi nhiệt (ngưng tụ)
4. tháp chưng tách C
2
H
5
Cl và HCl
5. máy nén
6. thiết bị phản ứng : hydroclo hóa ống chùm
7. Tháp chưng tách C
2
H
5
Cl, etan chưa phản ứng, HCl và C
2
H
4
1.5. Quá trình clo hóa parafin cao phân tử
Quá trình clo hóa các parafin cao phân tử nhằm thu các sản phẩm sau:
19
C
2
H
4
C
2
H
6
Cl
2
2
4 7
1
5
1
6
3
C
2
H
5
C
- dẫn xuất clo của phân đoạn C
14
÷ C
17
: chứa khoảng 50% clo → làm chất hóa dẻo
cho PVC
- dẫn xuất clo của phân đoạn C
10
÷ C
13
: chứa khoảng 70 ÷ 75% clo → làm chất
chống cháy cho cao su, bông sợi, chất dẻo
- phụ gia cho sơn vecni, nhựa đường → làm hóa dẻo, chống cháy, ít bay hơi
- phụ gia cho dầu cắt kim loại ( trong chế tạo máy) → tác dụng bôi trơn khi nhiệt độ
do ma sát làm phân hủy kim loại thành clorua kim loại
- trong công nghiệp da: chống thấm nước
Tên thương mại của các dẫn xuất Clo parafin (Witaclo) của hãng Dynamit Nobel:
C
10
- C
13
: 49% Cl → Witaclo 149
57% Cl → Witaclo 157
C
14
- C
17
: 40% Cl → Witaclo 340
50% Cl → Witaclo 350
C
20
- C
28
: 20% Cl → Witaclo 520
40% Cl → Witaclo 540
• Điều kiện phản ứng:
o Clo hóa pha lỏng
o Nhiệt độ thấp (để tránh sản phẩm có màu)
⇒ dùng ánh sáng để khơi mào cho phản ứng, vì vậy cho phép thực hiện
phản ứng ở nhiệt độ từ 80 ÷ 100
o
C
• Thiết bị phản ứng:
o Có nguồn sáng
o Sục Cl
2
vào pha lỏng parafin
o Có trao đổi nhiệt để tránh sản phẩm có màu
• Sản phẩm: sản phẩm chứa hàm lượng clo cao nhất khoảng 71 ÷ 72%. Nếu
hàm lượng clo cao hơn thì độ nhớt sẽ phẩm sẽ cao.
20