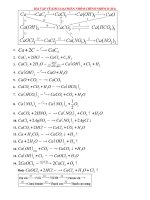bài tập hợp kim và ăn mòn kim loại
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (191.66 KB, 2 trang )
Khóa hc Hc thêm Hóa 12 –Thy Dng
Hp kim và n mòn kim loi
Hocmai.vn – Ngôi trng chung ca hc trò Vit
Tng đài t vn: 1900 58-58-12
- Trang | 1 -
Câu 1 : Trong phn ng ca đn cht kim loi vi phi kim và vi dung dch axit, nguyên t kim loi luôn:
A. Là cht kh B. Là cht oxi hoá
C. Va là cht kh, va là cht oxi hoá D. Không thay đi s oxi hoá.
Câu 2 : Mt vt làm bng st tráng km (tôn). Nu trên b mt đó có vt sây sát sâu ti lp st bên trong,
khi vt đó tip xúc vi không khí m thì:
A. Lp km b n mòn nhanh chóng B. St b n mòn nhanh chóng.
C. Km và st đu b n mòn nhanh chóng D. Không có hin tng gì xy ra.
Câu 3 : Mt vt bng st tráng thic (đó xc sâu ti lp st) tip xúc vi môi trng cht đin li thì :
A. C Fe và Sn điu b n mòn. B. C Fe và Sn không b n mòn.
C. Fe b n mòn, Sn không b n mòn. D. Sn b n mòn, Fe không b n mòn.
Câu 4: V tàu đi bin (phn chìm di nc) thép thng b g. C ch ca quá trình n mòn đin cc
âm và đin cc dng ln lt là
A. Fe
2
Fe
+ 2e và 2H
2
O + O
2
+ 4e 4
OH
.
B. Fe
3
Fe
+ 3e và 2
H
+ 2e
H
2
.
C. Fe
2
Fe
+ 2e,
2
Fe
3
Fe
+ 1e và 2H
2
O + O
2
+ 4e 4
OH
.
D. Fe
2
Fe
+ 2e,
2
Fe
3
Fe
+ 1e và
2
H
+ 2e H
2
.
Câu 5: Có ba thanh kim loi là: st nguyên cht (X), km nguyên cht (Y), st ln km (Z). Trong không
khí m thì
A. thanh X d b n mòn nht. B. thanh Y d b n mòn nht.
C. thanh Z d b n mòn nht. D. các thanh b n mòn nh nhau.
Câu 6: Cho các cp kim loi nguyên cht tip xúc trc tip vi nhau: Fe và Pb ; Fe và Zn ; Fe và Sn ; Fe
và Ni. Khi nhúng các cp kim loi trên vào dung dch axit, s cp kim loi trong đó Fe b phá hu trc là
A. 4. B. 1. C. 2. D. 3.
Câu 7: Cho các hp kim sau: Cu-Fe (I) ; Zn-Fe (II) ; Fe-C (III) ; Sn-Fe (IV). Khi tip xúc vi dung dch
cht đin li thí các hp kim mà trong đó Fe đu b n mòn trc là
A. I, II và IV. B. I, II và III. C. I, III và IV. D. II, III và IV.
Câu 8: Mt lá st đang tác dng vi dung dch H
2
SO
4
loãng, nu thêm vài git dung dch CuSO
4
vào thì
lng bt khí H
2
A. bay ra không đi. B. không bay ra na. C. bay ra ít hn. D. bay ra nhiu hn.
Câu 9: Có 4 dung dch riêng bit: a) HCl, b) CuCl
2
, c) FeCl
3
, d) HCl có ln CuCl
2
. Nhúng vào mi
dung dch mt thanh Fe nguyên cht. S trng hp xut hin n mòn đin hoá hc là
A. 0. B. 1. C. 2. D. 3.
Câu 10:
Tin hành bn thí nghim sau:
- (1): Nhúng thanh Fe vào dung dch FeCl
3
;
- (2): Nhúng thanh Fe vào dung dch CuSO
4
;
- (3): Nhúng thanh Cu vào dung dch FeCl
3
;
- (4): Cho thanh Fe tip xúc vi thanh Cu ri nhúng vào dung dch HCl.
S trng hp xut hin n mòn đin hóa hc là
A. 1. B. 2. C. 4. D. 3.
Câu 11 : Loi phn ng hoá hc nào xy ra trong s n mòn kim loi:
A. Phn ng th B. Phn ng oxi hoá - kh.
HP KIM VÀ N MÒN KIM LOI
(BÀI TP T LUYN)
Giáo viên: PHÙNG BÁ DNG
Các bài tp trong tài liu này đc biên son kèm theo bài ging “Hp kim và n mòn kim loi” thuc Khóa hc
hc thêm Hóa 12 – Thy Dng ti website Hocmai.vn đ giúp các Bn kim tra, cng c li các kin thc đc
giáo viên truyn đt trong bài ging tng ng. s dng hiu qu, Bn cn hc trc bài ging “Hp kim và n
mòn kim loi” sau đó làm đy đ các bài tp trong tài liu này.
Khóa hc Hc thêm Hóa 12 –Thy Dng
Hp kim và n mòn kim loi
Hocmai.vn – Ngôi trng chung ca hc trò Vit
Tng đài t vn: 1900 58-58-12
- Trang | 2 -
C. Phn ng phân hu D. Phn ng hoá hc.
Câu 12 : Ngâm mt lá st trong dung dch HCl; st b n mòn chm, khí thoát ra chm. Nu thêm vài git
dung dch CuSO
4
vào hn hp thì:
A. Dung dch xut hin màu xanh. B. St tan nhanh hn, khí thoát ra nhanh hn.
C. Hin tng không thay đi. D. Có đng kim loi bám vào thanh st.
Ngun:
Hocmai.vn