Thiết kế hệ thống chưng luyện liên tục loại tháp đệm để phân tách hỗn hợp Metylic Etylic.
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (509.62 KB, 63 trang )
Mục lục
Phần 1
Giới thiệu hỗn hợp và Sơ đồ dây chuyền công nghệ
I. Giới thiệu về hỗn hợp chưng
II Sơ đồ dây chuyền công nghệ
II Thuyết minh dây chuyền
III Chế độ thủy động của tháp đệm
Phần 2
Tính toán thiết bị chính
I. Cân bằng vật liệu
II. Đường kính tháp
III. Chiều cao tháp
IV. Tính trở lực của tháp
V. Tính cân bằng nhiệt lượng
IV. Tính toán cơ khí
Phần 3
Tính thiết bị phụ
Phần 4
Kết luận
Tài liệu tham khảo
1
Lêi nãi ®Çu
Ngày nay cùng với sự phát triển vượt bậc của nền công nghiệp thế giới và nước
nhà, các ngánh công nghiệp nhất là công nghiệp hóa chất và thực phẩm vần thiết nhiều
hóa chất có độ tinh khiết cao. Để đạt được điều này người ta thường tiến hành phân
tách các cấu tử ra khỏi hỗn hợp đầu, trong đó chưng cất là một trong những phương
pháp được sử dụng phổ biến hiện nay.
Chưng cất là quá trình dùng nhiệt để tách một phần hỗn hợp lỏng ra thành các
cấu tử riêng biệt dựa vào độ bay hơi khác nhau của chúng trong hỗn hợp ở cùng nhiệt
độ đo. Phương pháp này ứng dụng để tách hỗn hợp các cấu tử dễ bay hơi có tính chất
hòa tan hoàn toàn hoặc một phần vào nhau. Hỗn hợp này có thể chỉ có hai cấu tử hoặc
nhiều hơn. Với hệ hai cấu tử sẽ thu được sản phẩm đỉnh gồm phần lớn là cấu tử dễ bay
hơi và sản phẩm đáy chứa đa phần là cấu tử khó bay hơi.
Trong sản xuất ta thường gặp các phương pháp chưng khác nhau như : chưng đơn
giản, chưng bằng hơi nước trực tiếp, chưng chân không và đặc biệt hơn là chưng
luyện.
Chưng luyện là phương pháp thông dụng dùng để tách hoàn toàn hỗn hợp các cấu
tử dễ bay hơi có tính chất hòa tan một phần hoặc hòa tan hoàn toàn vào nhau.Chưng
luyện ở áp suất thấp dùng cho các hỗn hợp dễ bị phân hủy nhiệt ở nhiệt độ cao ,các
cấu tử dễ bay hơi và ngược lại.
Vật liệu gia công là thép không gỉ bởi vì hỗn hợp cần tách là hệ ăn mòn mạnh,
mặt khác tuy giá thành sản xuất còn cao nhưng đáp ứng được những tiêu chuẩn cơ bản
của thiết bị hóa chất đó là: chống ăn mòn, bền nhiệt, cơ tính tốt, tuổi thọ làm việc lâu
dài …
Đồ án môn Quá trình và Thiết bị bước đầu giúp sinh viên làm quen với việc
tính toán và thiết kế một dây chuyền sản xuất, mà cụ thể trong đồ án này là hệ thống
chưng luyện liên tục.
Với đề tài:
Thiết kế hệ thống chưng luyện liên tục loại tháp đệm để phân tách hỗn hợp
Metylic- Etylic.
Tập đồ án này bao gồm 6 nội dung chính :
− Tính cân bằng vật liệu của tháp
− Xác định đường kính tháp
− Xác định chiều cao tháp dựa vào phương pháp số đơn vị chuyển khối
− Tính trở lực và cân bằng nhiệt lượng của tháp
− Tính toán cơ khí
− Tính toán thiết bị phụ
PHẦN 1
GIỚI THIỆU HỖN HỢP VÀ SƠ ĐỒ DÂY CHUYỀN CÔNG NGHỆ
2
I.GIỚI THIỆU VỀ HỖN HỢP CHƯNG:
Metylic là chất lỏng linh động và không màu, hòa tan trong nước theo bất cứ tỷ lệ
nào. Nhiệt độ sôi 67.40C , Metylic là chất độc đói với cơ thể, nếu uống từ 8 đến 10g thì
có thể bị ngộ độc, mát bị rối loạn và có thể mù lòa.
Etylic cũng là chất lỏng linh động không màu và có thể hòa tan vô hạn trong nước.
Nhiệt độ sôi của nó là 78.40C, Etylic được ứng dụng rất nhiều trong công nghiệp, đời
sống hàng ngày. Metylic – Etylic là sản phẩm của quá trình lên men hoặc quá trình
tổng hợp khác, 2 chất này ở trạng thái bình thường là chất lỏng không liên kết, có độ
bay hơi khác nhau. ở đây metylic bay hơi trước do nhiệt độ sôi của nó thấp hơn của
etylic. Hỗn hợp ăn mòn yếu nên trong quá trình lựa chọn thiết bị để chưng luyện thì ta
nên sử dụng loại thép các bon thường để tránh lãng phí.
II.SƠ ĐỒ DÂY CHUYỀN CÔNG NGHỆ
12
Chú thích:
1:Thùng
2:Bể
cao vị
chứa
3: Thiết
bị đun
4:Lưu
lượng kế
3
5:Tháp
chưng
6:Thiết
bị ngưng
7:Thiết
bị làm
lạnh
dung
dịch đầu
8:Bể
chứa sản
phẩm
đỉnh
sôi hỗn
hợp đầu
9:Bể
chứa sản
phẩm
đáy
10:Thiết
bị đun
sôi đáy
tháp
luyện
tụ
11 Cốc
tháo
nước
ngưng
12 : Bơm
li tâm
II. Thuyết minh dây chuyền :
Nguyên liệu đầu được chứa trong thùng chứa (2) và được bơm (12) bơm lên
thùng cao vị (1). Hỗn hợp đầu từ thùng cao vị tự chảy xuống thiết bị đun sôi hỗn hợp
đầu (3). lưu lượng được khống chế bằng cách điều chỉnh hệ thống van và lưu lượng kế
(4) hơi nước bão hòa từ nồi hơi vào đun sôi hỗn hợp đầu đến nhiệt độ sôi sau khi đạt
tới nhiệt độ sôi hỗn hợp này được đưa vào đĩa tiếp liệu của tháp chưng luyện (5) loại
đệm.Trong tháp hơi đi từ dưới lên tiếp xúc trực tiếp với lỏng chảy từ trên xuống, tại
đây xảy ra quá trình bốc hơi và ngưng tụ nhiều lần. Theo chiều cao của tháp, càng lên
cao thì nhiệt độ càng thấp nên khi hơi đi qua các tầng đệm từ dưới lên , cấu tử có nhiệt
độ sôi cao sẽ ngưng tụ.Quá trình tiếp xúc lỏng hơi trong tháp diễn ra liên tục làm cho
trong pha hơi càng giầu cấu tử dễ bay hơi. Cuối cùng trên đỉnh tháp ta sẽ thu được hầu
hết là cấu tử dễ bay hơi (cụ thể ở đây là Metylic) và một phần cấu tử khó bay hơi
(Etylic). Hỗn hợp hơi này được đưa vào thiết bị ngưng tụ (6) và tại đây nó được ngưng
tụ hoàn toàn (tác nhân là nước lạnh). Một phần chất lỏng sau khi ngưng tụ được đưa
hồi lưu trở về tháp chưng luyện và cũng được khống chế bằng lưu lượng kế , phần còn
lại đạt yêu cầu sẽ được đưa vào thiết bị làm lạnh (7) để làm lạnh đến nhiệt độ cần thiết
sau đó được đưa vào thùng chứa sản phẩm đỉnh (8).
Chất lỏng hồi lưu đi từ trên xuống dưới, gặp hơi có nhiệt độ cao đi từ dưới lên,
một phần cấu tử có nhiệt độ cao tiếp tục ngưng tụ thành lỏng đi xuống.Do đó nồng độ
cấu tử khó bay hơi trong pha lỏng ngày càng nhiều , cuối cùng ở đáy tháp ta thu được
hỗn hợp lỏng gồm hầu hết là cấu tử khó bay hơi (etylic) và một phần rất ít cấu tử dễ
bay hơi (Meylic), hỗn hợp lỏng được đưa ra khỏi đáy tháp qua thiết bị phân dòng, một
phần được đưa ra thùng chứa sản phẩm đáy (9) , một phần được đưa vào thiết bị đun
sôi đáy tháp (10) và một phần được hồi lưu trở lại đáy tháp.Thiết bị này có tác dụng
đun sôi tuần hoàn và bốc hơi sản phẩm đáy (tạo dòng hơi đi từ dưới lên trong tháp).
Nước ngưng của thiết bị gia nhiệt được tháo qua thiết bị tháo nước ngưng ( 11),Tháp
chưng luyện làm việc ở chế độ liên tục, hỗn hợp đầu vào và sản phẩm được lấy ra liên
tục.
III. Chế độ thuỷ động của tháp đệm
Trong tháp đệm có 3 chế độ thủy động là chế độ chảy dòng, chế độ quá độ và chế độ
chảy xoáy.
Khi vận tốc khí bé lực hút phân tử lớn hơn và vượt lực ỳ. Lúc này quá trình chuyển
khối được xác định bằng dòng khuếch tán phân tử. Tăng vận tốc lực lỳ trở lên cân
bằng với lực hút phân tử. Quá trình chuyển khối lúc này không chỉ được quyết định
4
bằng khuếch tán phân tử mà cả bằng cả khuếch tán đối lưu. Chế độ thủy động này gọi
là chế độ quá độ. Nếu ta tiếp tục tăng vận tốc khí lên nữa thì chế độ quá độ chuyển
sang chế độ chảy xoáy. Trong giai đoạn này quá trình khuếch tán sẽ được quyết định
bằng khuếch tán đối lưu.
Nếu ta tăng vận tốc khí lên đến một giới hạn nào đó thì sẽ xảy ra hiện tượng đảo pha.
Lúc này chất lỏng sẽ chiếm toàn bộ chiều cao tháp và trở thành pha liên tục, còn pha
khí khuếch tán vào trong pha lỏng và trở thành pha phân tán. Vận tốc khí ứng với thời
điểm này gọi là vận tốc đảo pha. Khí sục vào lỏng và tạo thành bọt khí vì thế trong giai
đoạn này chế độ làm việc trong tháp gọi là chế độ sủi bọt. Ở chế độ này vận tốc
chuyển khối nhanh đồng thời trở lực cũng tăng nhanh.
Trong thực tế, ta thường cho tháp đệm làm việc ở chế độ màng có vận tốc nhỏ hơn vận
tốc đảo pha một ít vì quá trình chuyển khối trong giai đoạn sủi bọt là mạnh nhất nhưng
vì giai đoạn đó khó khống chế quá trình làm việc.
Ưu điểm của của tháp đệm :
- Hiệu suất cao vì bề mặt tiếp xúc pha lớn
- Cấu tạo tháp đơn giản
- Trở lực trong tháp không lớn lắm
- Giới hạn làm việc tương đối rộng
Nhược điểm :
• Khó làm ướt đều đệm
• Tháp cao quá thì phân phối chất lỏng không đều
Bảng kê các ký hiệu thường dùng trong bản đồ án này :
• F: lượng hỗn hợp đầu, (kg/s)
• P: lượng sản phẩm đỉnh, (kg/s)
• W: lượng sản phẩm đáy, ( kg/s)
• Các chỉ số F, P, W , A , B : tương ứng chỉ đại lượng đó thuộc về hỗn hợp đầu, sản phẩm
đỉnh, sản phẩm đáy, của các cấu tử là Metylic và Etylic
• a: phần trăm khối lượng của Metylic trong hỗn hợp (kg Metylic / kg hỗn hợp )
• x : nồng độ phần mol của Metylic trong hỗn hợp ( kmol Metylic / kmol hỗn hợp )
• M: khối lượng mol phân tử ( kg/ kmol)
• μ : độ nhớt động lực , (N.s/m2 )
• Các chỉ số A, B , X ,Y , hh tương ứng thuộc về cấu tử Metylic, Etylic, thành phẩn lỏng,
thành phần hơi và của hỗn hợp
ρ : khối lượng riêng ( kg/m3)
5
PHẦN 2
TÍNH TOÁN THIẾT BỊ CHÍNH
Các số liệu ban đầu:
-Năng suất tính theo độ hỗn hợp đầu F = 9.88 tấn/h = 9880 kg/h
-Nồng độ cấu tử dễ bay hơi trong:
+ Hỗn hợp đầu:
aF = 3.55 phần mol
+ Sản phẩm đỉnh: aP = 96 phần mol
+ Sản phẩm đáy: x w = 1 phần mol
-Tháp làm việc ở áp suất thường.
-Hỗn hợp đầu được gia nhiệt đến nhiệt độ sôi.
I. TÍNH CÂN BẰNG VẬT LIỆU TOÀN THIẾT BỊ
1.Tính toán cân bằng vật liệu cho toàn tháp
1.1.Đổi từ phần mol sang khối lượng
aF =
xF × M A
3.55 × 32
=
= 0.109 phần khối lượng
x F × M A + (1 − x F ) × M B 3.55 × 32 + (1 − 3.55) × 46
aP =
xP × M A
96 × 32
=
= 0.773 phần khối lượng
x P × M A + (1 − x P ) × M B 96 × 32 + (1 − 96 ) × 46
aw =
xw × M A
1 × 32
=
= 0.028 phần khối lượng
x w × M A + (1 − x w ) × M B 1 × 32 + (1 −1) × 46
- Khối lượng mol trung bình trong pha lỏng được tính:
M = x.MA + (1- x)MB
MF= xF.MA+ (1- xF)MB
= 3.55 × 32 + (1 − 3.55) × 46 = 43.9(kg / kmol )
MP = xP.MA + (1- xP)MB
= 96 × 32 + (1 − 96) × 46 = 34.38(kg / kmol )
MW = xW.MA + (1- xW)MB
= 1× 32 + (1 − 1) × 46 = 45.44( kg / kmol )
1.2. Hệ phương trình cân bằng vật liệu
•Phương trình cân bằng vật liệu cho toàn tháp :
F = P + W ; (1)
•Đối với cấu tử dễ bay hơi (etylic) :
FaF = Pap + Waw ( 2)
• Thay (1) vào (2) rút ra :
• Lượng sản phẩm đáy :
Với F = 3300 kg/h = 3300: 43.49 = 75.171(kmol/h)
aF − aw
•
0.109 − 0.028
358.792
= 3300 ×
= 358.792( kg / h ) =
= 10.436(kmol / h)
a P − aW
0.773 − 0.028
33.38
Từ đó suy ra lượng sản phẩm đỉnh :
W = F – P = 3300 – 358.792 = 2941.208( kg/h)= 2941.208:45.44=64.727(kmol/h)
1.3. Chỉ số hồi lưu tối thiểu (Rmin)
P=F
6
Dựng đường cân bằng theo số liệu đường cân bằng sau:
X
0
5
10
20
30
40
50
60
Y
0
7.4
T0c
78.3 77.2 76.5 75
70
80
90
100
14.3 27.1 39.6 51.5 62.6 72.3 79.8 86.6 83.2 100
73.6 72.2 70.8 69.4 68.2 66.9 65.9 64.9
Từ số liệu trong bảng trên ta vẽ đồ thị đường cân bằng lỏng (x) – hơi (y).
xw=0.04
XF=0.15
xp=0.83
* Từ đường cân bằng lỏng (x) – hơi (y) với xF = 0.15
→ y*F = 0.2077
→ Rmin =
→ Rmin =
x p − y F*
[III-81]
y F* − xF
x p − y F*
y − xF
*
F
=
0.83 − 0.2077
= 10.785
0.2077 − 0.15
1.4.Xác định chỉ số Rth
Hệ số hiệu chỉnh: β =
Rx
Rmin
Vấn đề chọn chỉ số hồi lưu thích hợp là rất quan trọng, vì khi chỉ số hồi lưu bé thì số
bậc của tháp lớn nhưng tiêu tốn ít hơi đốt, ngược lại khi chỉ số hồi lưu lớn thì số bậc
của tháp co ít hơn nhưng tiêu tốn hơi đốt lại rất lớn.
- Với mỗi giá trị của R x > Rmin từ đồ thị cân bằng lỏng hơi của hỗn hợp Metylic và
etylic ta xác định được một giá trị của Nlt tương ứng.
* Ở đây ta có phương trình đoạn luyện và đoạn chưng như sau:
- Phương trình đoạn luyện:
y=
xp
R
x+
R +1
R +1
y = Ax + B
7
A=
R
R +1
B=
xp
R +1
- Phương trình đoạn chưng:
R+ f
f −1
x−
xw
y = Ax − B
R +1
R +1
R+ f
f −1
F
A=
B=
xw
với f =
R +1
R +1
P
y=
Với RX1= 11.864.
Phương trình đoạn luyện : y = 0.922x + 0.065
Phương trình đoạn chưng: y = 1.484x -0.019
Có 28 đĩa trong đó đoạn luyện 14, đoạn chưng 14.
Với RX2 = 12.942
Phương trình đoạn luyện : y = 0.928x + 0.06
Phương trình đoạn chưng: y = 1.445x -0.018
Có 23 đĩa trong đó đoạn luyện 12, đoạn chưng 11.
Với RX3= 14.021
Phương trình đoạn luyện : y = 0.933x + 0.055
Phương trình đoạn chưng: y = 1.413x -0.017
Có 21 đĩa trong đó đoạn luyện 11, đoạn chưng 10.
Với RX4 = 15.099
Phương trình đoạn luyện : y = 0.938x + 0.052
Phương trình đoạn chưng: y = 1.385x -0.015
Có 19 đĩa trong đó đoạn luyện 11, đoạn chưng 8.
Với RX5 = 16.178
Phương trình đoạn luyện : y = 0.942x + 0.048
Phương trình đoạn chưng: y = 1.361x -0.014
Có 18 đĩa trong đó đoạn luyện 10, đoạn chưng 8.
Từ các phương trình làm việc trên ta vẽ đồ thị biểu diễn quan hệ x –y để tìm
được số đĩa lý thuyết tương ứng với từng giá trị Rx.
Các đồ thị được biểu diễn ở trang bên:
* Số đĩa lý thuyết Nlt và chỉ số hồi lưu Rx được tổng hợp trong bảng sau :
β
Rx
Nlt
Nlt(Rx+1)
1.1
1.2
11.864 12.942
28
23
360.192 320.666
1.3
1.4
14.021
15.099
21
19
315.441 305.881
8
1.5
16.178
18
309.204
Từ các giá trị tìm được ở bảng trên, ta xây dựng đồ thị biểu diễn mối quan hệ giữa R x –
Nlt(Rx+1)
Nlt(Rx+1)
R1 R2
R3
R4 R5
Rx
Để xác định chỉ số hồi lưu thích hợp người ta xác định chỉ số hồi lưu từ điều kiện
thể tích tháp nhỏ nhất ( không tính đến các chỉ tiêu kinh tế vận hành). Mặt khác dễ
dàng nhận thấy thể tích làm việc của tháp tỉ lệ với tích số N lt(Rx+1).Từ đồ thị trên,
điểm cực tiểu của đường vẽ được sẽ cho ta giá trị thể tích thiết bị bé nhất và ứng với
điểm đó sẽ có chỉ số hồi lưu thích hợp.
Mà Nlt(Rx+1) = 305.881 là giá trị nhỏ nhất, ứng với giá trị nhỏ nhất đó thì Rx= 15.099.
Vậy chỉ số hồi lưu thích hợp Rth= 15.099 và số đĩa lý thuyết Nlt= 19
2. Phương trình đường nồng độ làm việc
2.1.Đoạn luyện
Rth
xP
y=
x+
Rth +1
Rth +1
[III- 78]
*Thay số :
15.099
0.83
y=
x+
= 0.938 x + 0.052
15.099 + 1
15.099 + 1
Trong đó:
y: Là nồng độ phần mol của cấu tử dễ bay hơi trong pha hơi đi từ dưới lên.
x: Là nồng độ phần mol của cấu tử dễ bay hơi trong pha lỏng chảy từ trên xuống.
Rth: Là chỉ số hồi lưu thích hợp.
2.2. Đoạn chưng
9
- Lượng sản phẩm đầu trên một đơn vị sản phẩm đỉnh :
F 75.171
f = =
= 7.203 ( kmol h2 đầu / kmol sản phẩm đỉnh );
P 10.436
+Phương trình đường nồng độ làm việc của đoạn chưng :
R + f
f −1
15.099 + 7.203
7.203 − 1
y = th
x−
xw =
x−
× 0.04 = 1.385 x − 0.015
Rth + 1
Rth + 1
15.099 + 1
15.099 + 1
* Nhiệt độ sôi
- Nhiệt độ sôi của hỗn hợp đầu toF : từ xF = 0.15 theo bảng t-x, nội suy toF = 75.75oC
- Nhiệt độ hơi tại đỉnh tháp toP : từ yp = 0.83 theo bảng t –y nội suy toP = 66.6
- Nhiệt độ sôi của sản phẩm đáy tow : Từ xw= 0.04 theo bảng t- x nội suy tow = 77.42
II. TÍNH ĐƯỜNG KÍNH THÁP CHƯNG LUYỆN
Công thức tính đường kính tháp chưng luyện loại đệm :
D=
4G
ρ ytb .W ytb
= 0,0188.
g tb
ρ ytb .W ytb
[STQTTBT2-181]
Trong đó :
Wytb: tốc độ của khí và hơi(m/s)
gtb: lượng hơi trung bình đi trong tháp (kg/h)
ρ ytb .W ytb : tốc độ hơi trung bình đi trong tháp (kg/m2s)
Vì lượng hơi đi và lượng lỏng thay đổi theo chiều cao của tháp và khác nhau
trong mỗi đoạn nên ta phải tính hơi trung bình cho từng đoạn.
1.Lượng hơi trung bình đi trong tháp
1.1.Lượng hơi trung bình đi trong đoạn luyện
Lượng hơi trung bình đi trong đoạn luyện được tính gần đúng bằng trung bình
cộng của lượng hơi đi ra khỏi đĩa trên cùng của tháp và lượng hơi đi vào đĩa dưới cùng
của đoạn luyện.
g tb =
g đ + g1
, kg/s
2
(STQTTB T2-181)
Trong đó:
+ gtb :lượng hơi trung bình của đoạn luyện (kg/h)
+ gđ : lượng hơi đi ra khỏi đĩa trên cùng của đoạn luyện (kg/h);
+ g1 : lượng hơi đi vào đĩa dưới cùng của đoạn luyện ( kg/h);
* Lượng hơi đi ra khỏi đỉnh tháp :
gđ = GR + GP = GP(Rth + 1)
(STQTTB T2-181)
Trong đó
GP : lượng sản phẩm đỉnh ( kg/h)
GR : lượng lỏng hồi lưu đỉnh tháp (kg/h)
Rth : chỉ số hồi lưu thích hợp
⇒ gđ = 358.792( 15.099 + 1) = 5776.192 (kg/h)
* Lượng hơi đi vào đoạn luyện:
10
Lượng hơi g1, hàm lượng hơi y1, lượng lỏng của đĩa thứ nhất của đoạn luyện G 1 được
xác định theo hệ phương trình cân bằng vật liệu và nhiệt lượng cho đoạn luyện :
g1 = G1 + GP
g1 . y1 = G1a1 + GP a P
g r = g r
d d
11
(STQTTB T2-182)
Trong đó
a1 = a F = 0.109 phần khối lượng
r1 : ẩn nhiệt hóa hơi của hỗn hợp hơi ở đĩa thứ nhất của đoạn luyện (kJ/kg) ;
rđ : ẩn nhiệt hóa hơi của hỗn hợp hơi ra khỏi đỉnh tháp (kJ/kg)
r1 = rAy1 + (1- y1)rB;
STQTTB T2-182)
rđ = rAyđ + (1- yđ)rB;
Trong đó:
yđ : hàm lượng hơi sản phẩm đỉnh = aP = 0.773 phần khối lượng
rA ; rB : lần lượt là ẩn nhiệt hóa hơi của Metylic và Etylic nguyên chất (kJ/kg)
Từ x F= 0.15 tra bảng IX2a [STQTTB T2-148] suy ra nhiệt độ tF = 75.750C. Tra
0
bảng I.213 [STQTTB T1-257] với nhiệt độ hỗn hợp đầu t F ta được:
rA = 261.55 ( Kcal/kg) = 1095.058 (KJ/kg)
rB = 208.7 ( Kcal/kg) = 873.785 (KJ/kg )
→ r1 = 1095.058 y1 + 873.785 ( 1-y1) =221.273y1+873.785 (*)
Từ xP = 0.83 tra bảng IX2a [STQTTB T1-148] suy ra nhiệt độ của hỗn hợp đỉnh
tP= 66.60C, nội suy từ bảng I.213 [STQTTB T1 -257] với nhiệt độ hỗn hợp đỉnh t P ta
được:
rA = 266.7(Kcal/kg) = 1116.62 (KJ/kg)
rB = 212.02(Kcal/kg) = 887.685 (KJ/kg)
→rđ = aPrA + (1- aP )rB =
= 0.773 x 1116.62 + (1- 0.773) x 887.685 = 1064.652 (KJ/kg) (**)
Thay (*)&(**) vào hệ trên ta có :
g1 = G1 + 358.792
g1 . y1 = 0.109G1 + 358.792 × 0.773
g1 ( 221.273 y1 + 873.785) = 5776.192 ×1064.652
Giải hệ ta có:
→g1 = 6790.168( kg/h );
→ y1 = 0.144 phần khối lượng
→ G1 = 6431.376 ( kg/h );
→ lượng hơi trung bình của đoạn luyện :
→ g tb =
g1 + g d
6790.168 + 5776.192
=
= 6238.18( kg / h)
2
2
Thay y1vào (*) ta có :
r1 = 1095.058 0.14 + 873.785 ( 1-0.14)=905.648(KJ/kg)
11
1.2. Lượng hơi trung bình đi trong đoạn chưng
g1' + g n'
[STQTTB T2-182]
g =
2
Trong đó :
+ g’tb: lượng hơi trung bình của đoạn chưng ( kg/h)
+ g’n: lượng hơi đi ra khỏi đoạn chưng ( kg/h)
+ g’1 : lượng hơi đi vào đoạn chưng (kg/h)
Vì lượng hơi đi ra khỏi đoạn chưng bằng lượng hơi đi vào đoạn luyện nên ta có :
’
g n = g1
g ' + g1
→ g tb' = 1
[STQTTB T2-182]
2
Ta có hệ phương trình cân bằng vật liệu và nhiệt lượng cho đoạn chưng :
'
tb
G1' = g1' + Gw
' '
'
G1.x1 = g1. y w1 + Gw .xw
' '
'
'
g1.r1 = g1.r1 = g n .rn
[STQTTB T2-182]
Trong đó:
- G’1: lượng lỏng đi vào đoạn chưng(kg/h)
- g’1 : lượng hơi đi vào đoạn chưng (kg/h)
- x’1 : hàm lượng lỏng(phần khối lượng)
- r’n : ẩn nhiệt hóa hơi của hỗn hợp đi vào đĩa trên cùng của đoạn chưng (KJ/kg)
- r’1 : ẩn nhiệt hóa hơi của hỗn hợp hơi đi vào lớp đệm thứ nhất của đoạn chưng
( KJ/kg)
- xw : thành phần cấu tử dễ bay hơi (Metylic ) trong sản phẩm đáy ;
- r1 : ẩn nhiệt hóa hơi của hỗn hợp hơi đi vào lớp đệm trên cùng của đoạn chưng
(KJ/kg)
- rA : ẩn nhiệt hóa hơi của Metylic (KJ/kg)
- rB : ẩn nhiệt hóa hơi của Etylic (KJ/kg)
y '1 = y ∗ w là nồng độ cân bằng ứng với x w . Dựa theo đồ thị đường cân bằng lỏng
hơi ở trên ta có:
Ứng với x w = 0.04 ta có y w = 0.0595 ta đổi sang phần khối lượng
y *w =
0.0595 × M A
0.0595 × 32
=
= 0.042
0.0595 × M A + (1 − 0.0595) M B 0.0595 × 32 + 0.9405 × 46
Mặt khác ta có:
r1' = rA y1' + (1 − y1' )rB
rn' = rA y n' + (1 − y n' )rB
Tại x w = 0.04 nội suy từ bảng I.212 [STQTTB T1 -254] suy ra toC=77.42oC
Ta được :
RA = 260.548
(Kcal/kg) = 1090.862(KJ/kg);
12
RB = 208.032(Kcal/kg) = 870.988(KJ/kg);
⇒ r '1 = 1090.862 × 0.042 + (1 − 0.042) × 870.988 = 880.222( KJ / kg )
Thay vào hệ phương trình ta có :
⇒ G1' = 9927.516( Kg / h);
⇒ x1' = 0.038
⇒ g '1 = 6980.308( Kg / h)
⇒ lượng hơi trung bình của đoạn chưng :
g1' + g n'
6986.308 + 6790.168
g =
=
= 6888,238( Kg / h)
2
2
'
tb
2. Tính khối lượng riêng trung bình
a) Đối với pha hơi :
*Đoạn luyện :
ρ tbl =
[ ytbA .M A + (1 − y tbA )M B ].273 ( STQTT 2 − 183)
22,4.TL `
⇒ ρ tbl =
-Với y tbA =
[ ytbA .M A + (1 − y tbA )M B ].273 = [ 0.512 × 32 + (1 − 0,512) × 46].273 = 1.377(kg / m 3 );
22,4.(70.94 + 273)
22,4.TL `
y p + y1
2
+) y1= 0.144 phần khối lượng ta đổi sang phần mol:
0.144
32
= 0.195 (phần mol)
y1 =
0.144 (1 − 0.144)
+
32
46
+) yp=0.83(phần mol)
y tbA =
0.195 + 0.83
= 0.512 (phần mol)
2
- Từ bảng IX 2a(STQTTBT2-148) ta có totbL= 70.94oC
*Đoạn chưng:
ρ tbC =
[ y tbA .M A + (1 − y tbA ) M B ].273
22,4.TC `
⇒ ρ tbC =
( STQTT 2 − 183)
[ y tbA .M A + (1 − y tbA ) M B ].273 [ 0.12725 × 32 + (1 − 0,12725) × 46].273
=
= 1.544(kg / m 3 );
-Với y tbA =
22,4.(76.485 + 273)
22,4.TC `
y '1 + y1
2
+) y1= 0.144 phần khối lượng ta đổi sang phần mol:
0.144
32
= 0.195 (phần mol)
y1 =
0.144 (1 − 0.144)
+
32
46
+) y’1=yw=0.0595 (phần mol)
13
0.195 + 0.0595
= 0.12725 (phần mol)
2
y tbA =
- Từ bảng IX 2a(STQTTBT2-148) ta có totbL= 70.94oC
b) Đối với pha lỏng :
a
1 − atbA
1
= tbA +
ρxtb
ρxtbA
ρxtbB `
[STQTTBT2-183]
Trong đó :
- atb : phần khối lượng trung bình của cấu tử Mêtylic
- ρ xtbA : khối lượng riêng của cấu tử Mêtylic (kg/m 3)
- ρ xtbB : khối lượng riêng của cấu tử êtylic (kg/m 3)
* Đoạn luyện :
a
1 − atbAL
1
= tbAL +
ρxtL
ρxtbA
atbAL =
aF + a p
ρxtbB
=
2
x p + xw
xtbAL =
2
0.109 + 0.773
= 0.441 (phần khối lượng)
2
=
0.15 + 0.83
= 0.49 (phần mol)
2
o
Nội suy từ bảng IX2a(STQTTBT2-148) ở nhệt độ trung bình t X tbL = 70.94 O C
Theo bảng I.2 trong (STQTTBT1-9) ta nội suy được:
ρxtbA = 745.06.983 (kg/m3)
ρxtbB = 743.607 (kg/m3)
⇒
1
=
ρ xtbL
0,215 1 − 0,215
+
⇒ ρ xtbc = 743,92( kg / m 3 )
745,06 743,607
*Đoạn chưng:
1
ρxtbc
=
atbAC =
atbAC
ρxtbA
+
1 − atbAC
ρxtbB
a F + a '1
2
Với a’1: nồng độ phần khối lượng của pha lỏng ở lớp đệm cuối cùng của đoạn chưng.
a’1= x’1=0.038(phần khối lượng)
Đổi x’1 ra phần mol ta có:
0.038
32
x1' =
= 0.054 (phần mol)
0.038 (1 − 0.038)
+
32
46
0.109 + 0.038
→ a tbAC =
= 0.0735 (phần khối lượng)
2
14
x F + x 1'
xtbAL =
2
=
0.15 + 0.054
= 0.102 (phần mol)
2
o
Nội suy từ bảng IX2a(STQTTBT2-148) ở nhệt độ trung bình t X tbC = 76.485 O C
Theo bảng I.2 trong (STQTTBT1-9) ta nội suy được:
ρxtbA = 740.1 (kg/m3)
ρxtbB = 738.9 (kg/m3)
⇒
1
ρ xtbC
=
0.0735 1 − 0.0735
+
⇒ ρ xtbC = 738.99(kg / m 3 );
740.1
738.9
3.Tính tốc độ của khí và hơi đi trong tháp đệm
Có rất nhiều cách tính tốc dộ của hơi đi trong tháp đệm nhưng ta tính dựa vào vận tốc
đảo pha. Khi đó W=(0.80.9)W’s
Công thức tính vận tốc đảo pha :
Y=
WS'2 .σ d y ytb µ xtb
g .Vd3 .ρ xtb µ n
0.16
Y = 1,2.e −4 X
G
X = x
G
y
[STQTTBT2- 187]
1
4 ρ ytb
.
ρ
xtb
1
8
Trong đó:
-
W’s: tốc độ bắt đầu tạo nhũ tương, còn gọi là vận tốc đảo pha(m/s)
ρ xtb , ρ ytb :khôi lượng riêng trung bình của pha lỏng và pha khí
-
µ xtb : độ nhớt của hỗn hợp lỏng của đoạn chưng ở
-
µn
t tbo
: độ nhớt của nước ở 20oC
- Gx Gy : Lưu lượng lỏng và lưu lượng hơi trung bình(Kg/s)
*Chọn đệm vòng loại Rasiga kích thước :20x20x2,2 tra từ bảng IX.8[STQTTBT2193]
→ σđ = 240(m2/m3)
→Vđ = 0,73(m3/m3)
3.1.Tốc độ khí và lỏng đi trong đoạn chưng
-Độ nhớt hỗn hợp lỏng của đoạn chưng :
lg µxC = xtbC lg µA + (1 − xtbC ) lg µB ;
[STQTTBT1- 84]
Trong đó :
xtbc=0.102 : nồng độ phần mol của metylic ở đoạn chưng(phần mol)
μA ; μB : lần lượt là độ nhớt của 2 cấu tử metylicvà etylic ở nhiệt độ
totbC=76.485oC
Từ toán đồ I.18 trong STQTTBT1 – 90 ta có:
15
⇒ μA = 0,272.10-3(Ns/m2)=0,272(cp)
⇒ μB = 0,43.10-3(Ns/m2) =0,43(cp)
-Do đó :
⇒ lg µxC = 0,102 lg 0,272 + (1 − 0,102) lg 0,43
⇔ µxC = 0,41(cp )
Từ bảng I.101 [ I-91 ] tìm được μn = 1 (cp )
GxC=
G1 + G1' + F 6431,376 + 9927,516 + 3300
=
= 9829,446 (kg/h)
2
2
GyC=g tb' = 6888.238 (kg/h)
G
X = xC
G
yC
1
4 ρ ytbC
.
ρ
xtbC
1
1
1
8 9829,446 4 1,544 8
=
= 0.501
6888,238 738,99
Y = 1,2.e −4 X =1,2.e-4.0,51 = 0.1633
Y=
WSC'2 .σ d ρ ytbC µ xtbC
g .Vd3 .ρ xtbC µ n
'
⇔ WSC
= 1,246( m / s ) ;
0.16
W '2 .240.1,544 0,41
⇔ 0,1633 = SC 3
10.0,73 .738,9 1
0,16
Lấy WC = 0,8WSC' = 0,8 ×1,246 = 0,997( m / s )
3.2. Tốc độ của khí hơi đi trong đoạn luyện
+Độ nhớt của hỗn hợp lỏng đoạn luyện :
lg µ tbL = xtbL . lg µ A + (1 − xtbL ) lg µ B
Trong đó :
xtbc=0.49 : nồng độ phần mol của metylic ở đoạn luyện(phần mol)
μA ; μB : lần lượt là độ nhớt của 2 cấu tử metylicvà etylic ở nhiệt độ totbL=70.94oC
Nội suy từ bảng I.113- STQTTBT1-116:
⇒ μA = 0,285.10-3(Ns/m2) =0,285 (cp)
⇒ μB = 0,475.10-3(Ns/m2)=0,475 (cp)
-Do đó :
⇒lg µxL = 0,49 lg 0,285 + (1 − 0,49) lg 0,475
⇔ µxC = 0,37(cp )
Từ bảng I.101 [ I-91 ] tìm được μn = 1 (cp )
GxL=
G1 + G P .Rth 6431,376 + 358,792.15,099
=
= 5924,388 (kg/h)
2
2
GyL=g tb' = 6238,18 (kg/h)
G
X = xL
G
yL
1
4 ρ ytbL
.
ρ
xtbL
1
1
1
8 5924,388 4 1,377 8
=
= 0.45
6238,18 743,92
Y = 1,2.e −4 X =1,2.e-4.0,45 = 0.198
16
Y=
WSL'2 .σ d ρ ytbL µ xtbL
g.Vd3 .ρ xtbL µ n
⇔ WSL' = 1,428( m / s ) ;
0.16
⇔ 0,198 =
WSL'2 .240.1,377 0,37
10.0,733.743,92 1
0 ,16
Lấy WL = 0,8WSL' = 0,8 ×1,428 = 1,143( m / s )
4. Đường kính của tháp
* Đường kính đoạn Luyện:
g tb
6283.18
= 0.0188
=1.188( m)
ρytbL .WL
1.377 ×1.143
DL = 0,0188.
* Đường kính đoạn chưng:
DC = 0,0188.
g tb
6888.238
= 0.0188
= 1.257(m)
ρ ytbC .WC
1.544 × 0.997
Dựa vào kết quả nhận được chọn đường kính theo bảng quy chuẩn cho tháp (bảng
6.27-sách TTQTTBT2-115)
Ta có DL= DC=1.2 (m)
Khi đó vận tốc của hơi đi trong tháp sẽ là:
2
1.188
WL = 1.143 ×
= 1.120(m / s )
1.2
2
1.257
WC = 0.997 ×
= 1.094(m / s )
1.2
Lúc này giá trị của vận tốc làm việc :
WL= 0.78W’SL
WC= 0.88W’SC
III. CHIỀU CAO THÁP CHƯNG LOẠI ĐỆM
Có rất nhiều phương pháp để tínhchiều cao của tháp đệm ở dday ta tính theo số đơn vị
chuyển khối.
*Chiều cao làm việc của tháp đệm :
H = hđv.my
[STQTTBT2-175]
Trong đó :
− hđv : chiều cao của một đơn vị chuyển khối (m)
− my :số đơn vị chuyển khối tính theo pha hơi
Ta có :
yP
my = ∫
yW
dy
y −y
hđv = h1 +
*
m.G y
.h2
Gx
[STQTTBT2-177]
Với :
17
− h1 là chiều cao của 1 đơn vị chuyển khối đối với pha hơi (m)
− h2 là chiều cao của 1 đơn vị chuyển khối đối với pha lỏng (m)
2
Vđ
h1 =
. Re 0y, 25 . Pry3 ( m )
a.ψ.σđ
µx
h2 = 256
ρ
x
2
3
0 , 25
0 ,5
. Re x . Prx ( m )
Trong đó:
- a: hệ số phụ thuộc vào dạng đệm (đệm vòng a = 0.123)
- µ x : độ nhớt của pha lỏng (N.s/m2)
- Vđ: thể tích tự do của đệm (Vđ=0.73m3 /m3)
- ρ x : Khối lượng riêng của lỏng(kg/m3)
- ψ : hệ số thấm ướt của đệm, nó phụ thuộc vào tỷ số giữa mật độ tưới
thực tế lên tiết diện ngang của tháo và mật độ tưới thích hợp.
1.Tính chiều cao của 1 đơn vị chuyển khối đối với pha hơi & pha lỏng của tháp
2
h1 =
Vđ
. Re 0y, 25 . Pry3 ( m )
a.ψ.σđ
µx
h2 = 256
ρ
x
2
3
0 , 25
0,5
. Re x . Prx ( m )
1.1.Chuẩn số Renold của pha hơi và pha lỏng
+ Re x =
+ Re yc =
0,04.G x
Ft .σ đ .µ x
(STQTTBT2-178)
0,4.ρ y .Ws'
µ y .σ đ
Với Ft: là tiết diện mặt cắt tháp
πD 2 3.14 × 1.2 2
F t=
=
1.13(m 2 )
4
4
Gx ,Gy : Lưu lượng lỏng và lưu lượng hơi trung bình(Kg/s)
a, Đoạn chưng :
*Đối với pha lỏng:
GxC= 9829.446(kg/h)=2.73(Kg/s)
+ Re xC =
0,04.G xC
Ft .σ đ .µ xC
→ Re xC =
0,04 × 2.73
= 0.982
1.13 × 240 × 0.41 × 10 −3
*Đối với pha hơi:
18
Re yc =
0,4.ρ yc .Wsc'
µ yc .σ đ
M C = xtbC .M A + (1 − xtbC ) M B = 0,102.32 + (1 − 0,102).48 = 44.572( đvC )
Nội suy từ bảng I.113- STQTTBT1-116:
⇒ μA = 114,5.10-7(Ns/m2)
⇒ μB = 103,12.10-7(Ns/m2)
MC
→ µ yC =
yC .
⇒ µ yC =
Re yC =
MA
M
+ (1 − y C ) . B
µA
µB
44.572
32
46
0,12725.
+ (1 − 0,1275).
−7
114,5.10
103.12.10 −7
= 1.049.10 −5 ( N .s / m 2 )
0.4 × 1.544 × 1.246
= 305.66
1.049 × 10 −5 × 240
b) Đoạn luyện:
*Đối với pha lỏng:
GxL=5924.388(kg/h)=1.646 (kg/s)
+ Re xL =
0,04.G xL
Ft .σ đ .µ xL
Re xL =
0,04 × 1.646
= 0.656
1.13 × 240 × 0.37 × 10 −3
*Đối với pha hơi:
Re yL =
0,4.ρ yL .WsL'
µ yL .σ đ
M L = x tbL .M A + (1 − xtbL ) M B = 0,49.32 + (1 − 0,49 ).46 = 39.14( đvC )
Nội suy từ bảng I.113- STQTTBT1-116:
⇒ μA = 112,65.10-7(Ns/m2)
⇒ μB = 101,735.10-7(Ns/m2)
MC
→ µ yC =
yC .
⇒ µ yC =
Re yC =
MA
M
+ (1 − y C ) . B
µA
µB
39.14
32
46
0,5125.
+ (1 − 0,5125).
−7
112,65.10
101,735.10 −7
0.4 × 1.377 ×1.428
= 306.572
1.069 × 10 −5 × 240
1.2. Hệ số khuếch tán của pha lỏng và pha hơi
a)Hệ số khuếch án của pha hơi:
*Đoạn chưng:
19
(
= 1.069.10 −5 N .s / m 2
)
D yC =
−4
3
2
C
2
0.0043.10 .T
1
1
+
M A M B (m2/s)
.
[STQTTBT2-133]
1
13
P. v A + v B3
Trong đó :
− DyC : là hệ số khuếch tán của pha hơi (m2/s);
− P : là áp suất tuyệt đối của hệ 2 cấu tử metylic-etylic = 1at ;
− ν A ;ν B : lần lượt là thể tích mol của hơi metylic-etylic (cm3/mol);
− TC : là nhiệt độ tuyệt đối của đoạn chưng = 76.485oC
− TL : là nhiệt độ tuyệt đối của đoạn luyện = 70.94oC
− MA , MB : là khối lượng mol phân tử của 2 cấu tử metylic-etylic ( đvC)
+ν A = 4.3,7 + 1.14,8+1.7,4 = 37 (cm3/mol);
+ν B = 6.3,7 + 2.14,8+1.7,4 = 59.2(cm3/mol);
Thay vào ta được :
3
D yC =
0,0043.10 − 4.TC2
1
1
PC . v A3 + v B3
2
1
1
+
=
MA MB
.
3
=
0,0043.10 − 4.(76.485 + 273) 2
1. 37 + 59.2
*Đoạn luyện:
1
3
1
3
(
1
1
+
= 1,237.10 − 5 m 2 / s
32 46
.
2
)
3
D yL =
0,0043.10 − 4.TL2
1
13
PL . v A + v B3
2
1
1
+
=
MA MB
.
3
=
0,0043.10 − 4.(70.94 + 273) 2
2
.
(
1
1
+
= 1,229.10 − 5 m 2 / s
32 46
1
13
1. 37 + 59.2 3
b)Hệ số khuếch án của pha lỏng:
Trước tiên tính hệ số khuếch tán của hỗn hợp lỏng ở 20oC:
10 −6.
D x 20 =
1
1
+
MA MB
1
13
A.B. µ B 20 .ν A + ν B3
)
[STQTTBT2-133]
2
Trong đó:
20
- A, B : là hệ số phụ thuộc vào bản chất dung môi và chất tan
Ta có A=B=1do 2 cấu tử không lien kết với nhau
- DxC20 : là hệ số khuếch tán của pha lỏng ở 20o C (m2/s) ;
- ν A ;ν B : lần lượt là thể tích mol của hơi metylic-etylic (cm3/mol);
- MA , MB : là khối lượng mol phân tử của 2 cấu tử metylic-etylic ( đvC
- µ B20=1.19 cp : độ nhớt của etylic ở 20oC
1
1
+
MA MB
10 − 6.
⇒ D xC 20 =
1
13
A.B. µ B 20 .ν A + ν B3
−9
2
= 4,037.10 m / s
(
)
10 − 6.
2
=
1
1
+
32 46
1
13
1.1. 1,19 . 37 + 59.2 3
2
=
*Đoạn chưng:
+ DxC = DxC 20 [1 + b( ttbC − 20) ]
+b=
0,2. µ B 20
3
hệ số hiệu chỉnh
ρ B 20
Tra bảng I.2 STQTTBT1- 9 CÓ ρ B 20 = 789 Kg / m 3
b=
0,2. 1.19
3
789
= 0.0236
D xC = 4,037.10 − 9 [1 + 0,0236.( 76.485 − 20) ] = 9,42 × 10 − 9 (m 2 / s)
*Đoạn chưng:
D xC = 4,037.10 −9 [1 + 0,0236.( 70.94 − 20) ] = 8,89 × 10 − 9 (m 2 / s)
1.3.Tính chuẩn số Prant(Pr)
*Đoạn Chưng:
Pha hơi:
PryC =
µ yC
ρ yC .D yC
[ STQTTBT2- 178]
Thay số ta được :
PryC =
µyC
ρyC .D yC
=
1,049.10 −5
= 0,549
1,544.1,237.10 −5
Pha lỏng:
PrxC =
µ xC
ρ xC .DxC
Thay số ta được :
Pr xC=
0.41 × 10 −3
= 58.904
738.9 × 9.42 × 10 −9
*Đoạn Luyện:
Pha hơi:
21
Pr yL =
µ yL
[ STQTTBT2- 178]
ρ yL .D yL
Thay số ta được :
Pr yL =
µyL
ρyL .D yL
=
1,069.10 −5
= 0,632
1,377.1,229.10 −5
Pha lỏng:
PrxL =
µ xL
ρ xL .DxL
Thay số ta được :
Pr xL=
0.37 × 10 −3
= 55.947
743.92 × 8.89 × 10 −9
1.4.Tính hệ số thấm ướt ψ
+Mật độ tưới thực tế :
V
U tt = x (m3/m2.h)
Ft
[STQTTBT2 - 177]
Trong đó :
− Vx : lưu lượng thể tích của pha lỏng (m3/s)
− Ft : tiết diện ngang của tháp
+Mật độ tưới thích hợp :
Uth = σđ.B (m3/m2.h)
− B =0.65: hệ số cho trong bảng IX.6 [STQTTBT2-177]
− σđ : bề mặt riêng của đệm (m2/m3)
*Đoạn chưng:
Uth = 240.0,065 = 15,6 (m3/m2.h)
U ttC =
⇒
(
V xC
G xC
9829.446
=
=
= 11.772 m 3 / m 2 .h
Ft
Ft ρ xC 1.13 × 738.9
)
U tt 11.772
=
= 0.755
U th
15,6
Từ hình IX.16 [STQTTBT2-178 ] nội suy được hệ số thấm ướt của đệm với vòng đệm
Ψ = 0,775
*Đoạn Luyện:
Uth = 240.0,065 = 15,6 (m3/m2.h) ;
U ttL =
⇒
(
V xL
G xL
5924.388
=
=
= 7.05 m 3 / m 2 .h
Ft
Ft ρ xL 1.13 × 743.92
)
U tt 7.05
=
= 0,452
U th 15,6
Từ hình IX.16 [STQTTBT2-178 ] nội suy được hệ số thấm ướt của đệm với vòng đệm
Ψ = 0,557
22
1.5.Tính giá trị h1, h2
*Đoạn luyện:
⇒ h1L =
2
2
Vđ
0,73
. Re 0yL, 25 . Pr yL3 =
× 306.572 0, 25 × 0.632 3 = 0.137( m )
a.ψ .σ đ
0,123 × 0.557 × 240
⇒h2 L
µxL
= 256
ρ
xL
2
3
0 , 25
0 ,5
. Re xL . PrxL
2
0.37 ×10 −3
= 256 ×
743.92
3
× 0.565 0.25 ×55.497 0.5 = 0.104( m)
*Đoạn chưng:
⇒ h1C
2
Vđ
0 , 25
3
=
. Re yC . Pr yC
a.ψ .σ đ
2
=
0,73
× 305.66 0, 25 × 0.549 3 = 0.1089( m )
0,123 × 0.775 × 240
⇒h2C
µxC
= 256
ρ
Cx
2
3
0 , 25
0,5
. Re xC . PrxC
0.41 ×10 −3
= 256 ×
738.9
2
3
×0.982 0.25 ×58.904 0.5 = 0.132(m)
2) Tính số đơn vị chuyển khối
Với mỗi giá trị y trong khoảng 0.5 → 0.83 ta tìm được y* .Từ đó xây dựng đồ thị
1
= f ( y)
y −y
*
*Kết quả được tổng hợp ở bảng sau:
x
x*
x - x*
y
0.04
0.027
0.013
0.04
0.05
0.036
0.014
0.054
0.08
0.065
0.015
0.096
0.01
0.085
0.015
0.123
0.11
0.096
0.014
0.138
0.14
0.127
0.013
0.179
23
y*
0.06
0.074
0.116
0.143
0.157
0.195
y* - y
0.02
0.02
0.02
0.02
0.019
0.016
1/(y*-y)
50
50
50
50
52.63
62.5
m
1.538
1.429
1.333
1.333
1.357
1.231
0.15
0.2
0.3
0.4
0.5
0.6
0.7
0.75
0.8
0.83
0.138
0.175
0.249
0.327
0.408
0.489
0.586
0.63
0.704
0.734
0.012
0.025
0.051
0.073
0.092
0.111
0.114
0.12
0.096
0.096
0.193
0.239
0.327
0.427
0.521
0.614
0.708
0.756
0.802
0.83
0.208
0.271
0.396
0.511
0.626
0.723
0.789
0.843
0.866
0.863
0.015
0.032
0.069
0.084
0.105
0.109
0.081
0.087
0.064
0.033
66.67
31.25
14.49
11.9
9.52
9.17
12.35
11.49
15.63
30.3
1.25
1.28
1.353
1.151
1.141
0.982
0.711
0.725
0.667
0.344
*Đồ thị tích phân xác định số đơn vị chuyển khối của đoạn chưng và đoạn luyện :
Ta có mi = tgα =
y* − y
hệ số phân bố trung bình ở điều kiện cân bằng pha và tính
x* − x
riêng cho từng đoạn tháp.Giá trị i chạy từ 3-6 chọn i=6
*Với đoạn luyện:
Chọn các giá trị mi tương ứng với giá trị x = 0.2; 0.3; 0.4; 0.6; 0.7; 0.8
6
mL =
∑m
iL
i =1
6
=1.024
*Với đoạn chưng:
Chọn các giá trị mi tương ứng với giá trị x = 0.04; 0.05; 0.08; 0.1; 0.11; 0.14
6
mC =
∑m
iC
i =1
6
=1.322
Số đơn vị chuyển khối tính theo pha hơi:
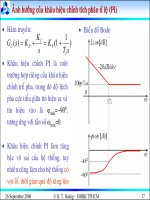
Đoạn chưng:
m yC =
yF
∫
yW
0 ,193
dy
dy
= ∫ *
*
y − y 0, 04 y − y
24
YF=0.193
Yw=0.04
Yp=0.83
Hình 2.
Ta tính tích phân trên dựa vào công thức Sim sơn
Đặt: F =
1
hC
[ F0 + F6 + 4( F1 + F3 + F5 ) + 2( F2 + F4 ) ]
⇒ m yC =
3
y −y
*
Với hC : trung bình khoảng cách giữa các giá trị y của đoạn chưng
0.014 + 0.042 + 0.03 + 0.015 + 0.041 + 0.014
= 0.026
6
⇒ m yC = 8.42
hC =
Đoạn luyện:
m yL =
yP
∫
yF
0 ,83
dy
dy
=
∫ y* − y
y * − y 0,193
Ta tính tích phân trên dựa vào công thức Sim sơn
Đặt: F =
1
hC
⇒ m yC =
[ F0 + F9 + 4( F1 + F3 + F5 + F7 ) + 2( F2 + F4 + F6 + F8 ) ]
3
y −y
*
Với hC : trung bình khoảng cách giữa các giá trị y của đoạn luyện
0.046 + 0.088 + 0.1 + 0.094 + 0.093 + 0.094 + 0.048 + 0.046 + 0.028
= 0.071
9
⇒ m yC = 10.78
hC =
3) Xác định chiều cao của một đơn vị chuyển khối:
Đoạn chưng:
25