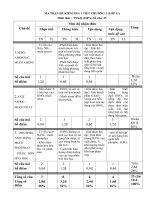
BẢNG MÔ TẢ CHƯƠNG II HÓA HỌC LỚP 8
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (59.89 KB, 6 trang )
BẢNG MÔ TẢ CHƯƠNG II
HÓA HỌC LỚP 8
I. Mục tiêu:
1. Kiến thức
- Hiện tượng vật lí là hiện tượng trong đó không có sự biến đổi chất này thành chất khác.
- Hiện tượng hoá học là hiện tượng trong đó có sự biến đổi chất này thành chất khác.
- Phản ứng hoá học là quá trình biến đổi chất này thành chất khác.
- Để xảy ra phản ứng hoá học, các chất phản ứng phải tiếp xúc với nhau, hoặc cần thêm nhiệt độ cao, áp suất cao hay
chất xúc tác.
- Để nhận biết có phản ứng hoá học xảy ra, dựa vào một số dấu hiệu có chất mới tạo thành mà ta quan sát được như
thay đổi màu sắc, tạo kết tủa, khí thoát ra…
- Hiểu được: Trong một phản ứng hoá học, tổng khối lượng của các chất phản ứng bằng tổng khối lượng các sản
phẩm.
- Phương trình hoá học biểu diển phản ứng hoá học.
- Các bước lập phương trình hoá học.
- ý nghĩa của phương trình hoá học: Cho biết các chất phản ứng và sản phẩm, tỉ lệ số phân tử, số nguyên tử giữa các
chất trong phản ứng.
2. Kĩ năng
- Quan sát được một số hiện tượng cụ thể, rút ra nhận xét về hiện tượng vật lí và hiện tượng hoá học.
- Phân biệt được hiện tượng vật lí và hiện tượng hoá học.
- Quan sát thí nghiệm, hình vẽ hoặc hình ảnh cụ thể, rút ra được nhận xét về phản ứng hoá học, điều kiện và dấu hiệu
để nhận biết có phản ứng hoá học xảy ra.
- Viết được phương trình hoá học bằng chữ để biểu diển phản ứng hoá học.
- Xác định được chất phản ứng (chất tham gia, chất ban đầu) và sản phẩm (chất tạo thành).
- Quan sát thí nghiệm cụ thể, nhận xét, rút ra được kết luận về sự bảo toàn khối lượng các chất trong phản ứng hoá
học.
- Viết được biểu thức liên hệ giữa khối lượng các chất trong một số phản ứng cụ thể.
- Tính được khối lượng của một chất trong phản ứng khi biết khối lượng của các chất còn lại.
- Biết lập phương trình hoá học khi biết các chất phản ứng (tham gia) và sản phẩm.
- Xác định được ý nghĩa của một số phương trình hoá học cụ thể.
3. Phát triển năng lực
- Năng lực sử dụng ngôn ngữ hóa học.
- Năng lực tính toán.
- Năng lực giải quyết vấn đề thông qua môn hóa học.
- Năng lực vận dụng kiến thức hóa học vào thực tế cuộc sống.
II. Bảng mô tả các mức yêu cầu cần đạt cho mỗi loại câu hỏi/bài tập trong chủ đề:
Nhận biết
Nội dung
(Mô tả yêu cầu cần
đạt)
- Sự biến
Câu hỏi/
- Nêu được khái niệm
đổi chất
Bài tập định hiện tượng vật lí,
- Phản ứng
tính
hiện tượng hoá học.
hóa học
- Nhận biết được một
- Định luật
số hiện tượng vật lí,
bảo toàn
hiện tượng hoá học.
khối lượng
- Nhận biết được quá
- Phương
trình biến đổi chất
trình hóa
này thành chất khác.
học
- Nêu được điều kiện
để phản ứng hóa học
xảy ra.
- Nêu được khái
niệm chất tham gia
và sản phẩm của
phản ứng cho trước.
- Nêu được định luật
bảo toàn khối lượng.
- Viết được một số
phương trình hóa
học đơn giản biểu
Loại câu
hỏi/bài tập
Thông hiểu
(Mô tả yêu cầu cần
đạt)
- Phân biệt được hiện
tượng vật lí, hiện
tượng hoá học.
- Giải thích được một
số hiện tượng vật lí,
hiện tượng hoá học.
- Xác định được điều
kiện để xảy ra phản
ứng hóa học, các
chất ban đầu phải
tiếp xúc với nhau,
hoặc cần thêm nhiệt
độ cao, áp suất cao
hoặc chất xúc tác.
- Viết được phương
trình hóa học bằng
chữ để biểu diễn
phản ứng hóa học.
- Viết được biểu thức
tính khối lượng áp
dụng định luật bảo
Vận dụng thấp
(Mô tả yêu cầu cần
đạt)
- Dựa vào một số dấu
hiệu quan sát được
(thay đổi màu sắc, tạo
kết tủa, khí thoát
ra…) để xác định
phản ứng hóa học xảy
ra.
- Xác định được chất
phản ứngvà sản
phẩm.
- Xác định được ý
nghĩa của một số
phương trình hóa học
cụ thể, tỉ lệ giữa số
nguyên tử, số phân tử
giữa chúng.
- Rút ra được ý nghĩa
của phương trình hóa
học, cho biết các chất
phản ứng và sản
phẩm, tỉ lệ số nguyên
Vận dụng cao
(Mô tả yêu cầu cần
đạt)
- Dựa vào hiện
tượng thí nghiệm,
hình vẽ,…xác định
được điều kiện và
dấu hiệu để nhận
biết có xảy ra phản
ứng hóa học hay
không.
- Xác định được một
số hiện tượng trong
tự nhiên và chỉ ra
được hiện tượng vật
lí và hiện tượng hóa
học.
diễn phản ứng hóa
học đã được giới
thiệu.
toàn khối lượng.
- Xác định được các
bước lập phương
trình hóa học cho
một số hóa học cụ
thể.
- Lập được phương
trình hóa học khí
biết các chất tham
gia, sản phẩm
Câu hỏi/
Bài tập định
lượng
Giải thích được
các hiện tượng thí
nghiệm.
Bài tập
thực
hành/thí
nghiệm
gắn với
hiện tượng
thực tiễn
tử, số phân tử giữa
chúng.
Tính được khối lượng
của một chất trong
phản ứng khi biết
khối lượng của các
chất còn lại.
Giải thích được
một số hiện tượng
thí nghiệm liên quan
đế thực tiễn.
- Giải thích được
một số hiện tượng
thí nghiệm hoặc
hiện tượng trong tự
nhiên về sự bảo
toàn khối lượng các
chất trong phản ứng
hóa học.
- Viết được một số
phương trình hóa
học bằng chữ,
phương trình hóa
học đơn giản xảy ra
trong thực tiễn.
III. Câu hỏi:
1. Mức độ biết:
Câu 1: Hiện tượng nào là hiện tượng hóa học trong số các hiện tượng cho dưới đây?
A. Hòa tan thuốc tím vào nước sẽ tạo thành dung dịch thuốc tím
B. Làm bay hơi dung dịch muối ăn sẽ tạo thành tinh thể muối ăn
C. Thủy tinh đun cho nóng chảy và thổi thành bình cầu
D. Sắt để lâu trong không khí sẽ bị gỉ
Câu 2: Trong các hiện tượng sau đây, hiện tượng nào là hiện tượng vật lí?
A. Đun qúa lửa mỡ sẽ khét.
B. Sự kết tinh muối ăn.
C. Về mùa hè, thức ăn thường bị thiu. D. Khi đốt nóng một lá sắt thì thấy khối lượng tăng lên.
Câu 3: Quá trình nào sau đây có phản ứng hóa học xảy ra?
A. Cồn để trong lọ không kín bị bay hơi.
B. Dây sắt được cắt nhỏ thành đoạn rồi tán thành đinh.
C. Hoàn tan đường vào nước ta được dung dịch nước đường.
D. Đèn tín hiệu giao thông chuyển từ màu đỏ sang màu xanh.
Câu 4: Phát biểu nào sau đây đúng nhất?
A. Trong phản ứng hóa học khối lượng mỗi chất không thay đổi.
B. Trong phản ứng hóa học liên kết giữa các nguyên tử không thay đổi.
C. Trong phản ứng hóa học số nguyên tử của mỗi nguyên tố thay đổi.
D. Trong phản ứng hóa học tổng khối lượng các chất trước và sau phản ứng không thay đổi.
Câu 5: Phương trình hóa học cho biết
A. Tỉ lệ số nguyên tử, số phân tử giữa các chất cũng như từng cặp chất trong phản ứng.
B. Số phân tử các chất tham gia phản ứng.
C. Số phân tử các chất sản phẩm.
D. Tỉ lệ về khối lượng giữa các chất trong phản ứng.
→ 2Al2O3 . Tỉ lệ số nguyên tử, số phân tử giữa các chất trong phản ứng lần
Câu 6: Cho phương trình hóa học 4Al + 3O 2
lượt là
A. 2:3:4
B. 3:2:4
C. 4:3:2
D. 2:4:3
Câu 7: Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử, số phân tử giũa các chất trong các theo sơ đồ sau:
a. O2 + H2 − − − > H2O
b. Al + O2 − − − > Al2O3
c. Na2CO3 + Ca(OH)2 − − − > CaCO3
+ NaOH
2. Mức độ thông hiểu:
Câu 1: Các quá trình dưới đây là hiện tượng hóa học hay hiện tượng vật lý? Giải thích.
a. Hòa tan mực vào nước.
b. Khi đung ấm nước sôi thấy khói (hơi nước) bốc lên.
c. Sắt để ngoài không khí lâu ngày bị gỉ sắt.
d. Tách muối ăn từ nước biển.
Câu 2: Trong khi tiến hành thí nghiệm, dựa vào đâu mà em biết đã có phản ứng hóa học xảy ra?
Câu 3: Khẳng định sau gồm 2 ý: “Trong phản ứng hoá học, chỉ diễn ra sự thay đổi liên kết giữa các nguyên tử, nên tổng khối
lượng các chất được bảo toàn”. Hãy chọn phương án đúng trong các phương án sau:
A. Ý 1 đúng, ý 2 sai.
B. Cả hai ý đều đúng, nhưng ý 1 không giải thích cho ý 2.
C. Ý 1 sai, ý 2 đúng.
D. Cả hai ý đều đúng và ý 1 giải thích cho ý 2.
Câu 4: Viết phương trình chữ của các phản ứng sau:
a. Khí hiđro tác dụng với khí oxi tạo thành hơi nước.
b. Đốt khí axetylen trong không khí sinh ra khí cacbonic và hơi nước.
c. Nung đá vôi chứa canxi cacbonat tạo thành vôi sống là canxi oxit và khí cacbonic.
d. Đốt than (cacbon) trong không khí thu được khí cacbonic.
Câu 5: Hoàn thành phương trình hóa học theo sơ đồ sau:
a. O2 + Na − − − > Na2O
b. Mg + O2 − − − > MgO
c. Al + Cl2 − − − > AlCl3
3. Vận dụng thấp:
Câu 1: Sắt cháy trong oxi không có ngọn lửa, không khói nhưng sáng chói, tạo ra các hạt nhỏ nóng chảy màu nâu là oxit
sắt từ. Hãy ghi lại phương trình chữ và nêu dấu hiệu xảy ra phản ứng ?
Câu 2: Khi cho một mẫu vôi sống (có tên là canxi oxit) vào nước, thấy nước nóng lên, thậm chí có thể sôi lên sùng sục,
mẩu vôi sống tan ra. Theo em có phản ứng hóa học xảy ra không? Vì sao?
Câu 3: Cho kim loại nhôm tác dụng với axit clohiđric HCl tạo ra nhôm clorua AlCl3 và khí hiđro H2.
a. Lập phương trình hóa học của phản ứng.
b. Cho biết tỉ lệ giữa số nguyên tữ nhôm lần lượt với số phân tử của ba chất trong phản ứng.
Câu 4: Một thanh sắt nặng 56 gam để ngoài không khí bị khí oxi phản ứng tạo thành gỉ là oxit sắt từ Fe3O4. Sau một thời
gian đem cân lại, thấy thanh sắt ngặng 57,6 gam.
a. Viết công thức khối lượng của phản ứng xảy ra.
b. Khí oxi đã phản ứng bao nhiêu gam.
4. Vận dụng cao:
Câu 1: Khi đốt nến, nến chảy lỏng thấm vào bấc. Sau đó, nến lỏng chuyển thành hơi. Hơi nến cháy trong không khí tạo ra
cacbon đioxit và hơi nước. Hãy phân tích các giai đoạn của quá trình mô tả trên và chỉ rõ giai đoạn nào có hiện tượng hóa học?
Câu 2: Khi trời lạnh, thường thấy mỡ đóng thành váng. Khi đun nóng, các váng mỡ này tan chảy. Nếu đun quá lửa, thì
một phần mỡ hóa hơi và một phần bị cháy đen. Hãy chỉ ra đâu là hiện tượng vật lí, đâu là hiện tượng hóa học của các quá trình
trên.
Câu 3: Trong quá trình các chú thợ xây dựng hoàn thiện ngôi nhà mới của gia đình bạn Tuấn. Tuấn để ý quan sát và thấy
hiện tượng xảy ra như sau: Nước vôi (có chứa canxi hiđroxit) được quét lên tường một thời gian sau đó sẽ khô và hóa rắn (chất
này là canxi cacbonat). Em giúp bạn Tuấn trả lời các câu hỏi sau đây nhé.
a. Dấu hiệu nào chứng tỏ có phản ứng hóa học xảy ra?
b. Viết phương trình chữ của phản ứng, biết rằng có chất khí cacbonic (có trong không khí) tham gia phản ứng và sản
phẩm ngoài chất rắn còn có nước (chất này bay hơi)?
Câu 4: Cho sơ đồ phản ứng sau: FexOy + H2SO4 − − − > Fex(SO4)y + H2O
a. Xác định x , y, biết x ≠ y.
b. Lập phương trình hóa học trên.
c. Tìm tỉ lệ số phân tử giữa các chất trong phản ứng hóa học trên.