DSpace at VNU: Kiểm nghiệm cơ chế phản ứng H2(k)+Cl2(k)- 2HCl(k) bằng phương pháp tính hóa học lượng tử
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (788.23 KB, 14 trang )
ĐẠI HỌC QUỐC GIA HÀ NỘI
TRƢỜNG ĐẠI HỌC KHOA HỌC TỰ NHIÊN
---------------------
VŨ THỊ NGỌC LAN
KIỂM NGHIỆM CƠ CHẾ PHẢN ỨNG H2(k)+ Cl2(k) → 2HCl(k)
BẰNG PHƢƠNG PHÁP TÍNH HÓA HỌC LƢỢNG TỬ
LUẬN VĂN THẠC SĨ
Hà Nội - 2015
ĐẠI HỌC QUỐC GIA HÀ NỘI
TRƢỜNG ĐẠI HỌC KHOA HỌC TỰ NHIÊN
---------------------
VŨ THỊ NGỌC LAN
KIỂM NGHIỆM CƠ CHẾ PHẢN ỨNG H2(k)+ Cl2(k) → 2HCl(k)
BẰNG PHƢƠNG PHÁP TÍNH HÓA HỌC LƢỢNG TỬ
Chuyên ngành: Hóa lý thuyết và hóa lý
Mã số: 60440119
LUẬN VĂN THẠC SĨ KHOA HỌC
NGƯỜI HƯỚNG DẪN KHOA HỌC: PGS.TS. Phạm Văn Nhiêu
TS. Vũ Việt Cường
Hà Nội - 2015
Luận văn thạc sĩ
LỜI CẢM ƠN
===***===
Trong quá trình thực hiện đề tài: “KIỂM NGHIỆM CƠ CHẾ PHẢN ỨNG
H2(k)+ Cl2(k) → 2HCl(k) BẰNG PHƢƠNG PHÁP TÍNH HÓA HỌC LƢỢNG TỬ”.
Tôi đã nhận được rất nhiều sự giúp đỡ tạo điều kiện của tập thể lãnh đạo, các nhà
khoa học, cán bộ, chuyên viên, giảng viên, cán bộ các phòng, ban chức năng của
trường, đặc biệt là các thầy cô khoa Hóa- trường ĐHKHTN- ĐHQGH tôi xin bày
tỏ lòng biết ơn chân thành về sự giúp đỡ đó.
Tôi xin bày tỏ lòng biết ơn sâu sắc nhất tới PGS.TS Phạm Văn Nhiêu và TS
Vũ Việt Cường – những người thầy giáo đã trực tiếp hướng dẫn tận tình, tâm huyết,
truyền đạt những kiến thức và kinh nghiệm quý báu cho tôi trong quá trình học tập
và nghiên cứu để hoàn thành luận văn này.
Đồng thời, con cũng xin gửi lời cảm ơn tới bố mẹ, các thầy giáo, cô giáo,
các anh, chị, em đồng nghiệp nơi tôi công tác tại trường THPT Chí Linh- Hải
Dương, bạn bè và người thân đã động viên, nhiệt tình giúp đỡ tôi trong suốt quá
trình học tập và hoàn thành luận văn của mình.
Do còn giới hạn về mặt thời gian cũng như những kinh nghiệm, khả năng
của bản thân còn hạn chế nên luận văn không tránh khỏi những thiếu sót. Rất mong
nhận được sự đóng góp ý kiến chân thành của quý thầy cô và bạn bè.
Một lần nữa, tôi xin trân trọng cảm ơn với tất cả tấm lòng!
Hà Nội, ngày 10 tháng 10 năm 2015
Học viên
Vũ Thị Ngọc Lan
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
MỤC LỤC
LỜI CẢM ƠN
DANH MỤC KÍ HIỆU VIẾT TẮT
DANH MỤC BẢNG
DANH MỤC HÌNH VẼ
PHẦN MỞ ĐẦU ..........................................................................................................4
I.
Lí do chọn đề tài ............................................................................................4
II.
Mục đích nghiên cứu. ....................................................................................4
III.
Nhiệm vụ nghiên cứu. .................................... Error! Bookmark not defined.
IV.
Phƣơng pháp nghiên cứu............................... Error! Bookmark not defined.
CHƢƠNG 1: TỔNG QUAN ........................................ Error! Bookmark not defined.
1.1.
Cơ sở lý thuyết hóa học lƣợng tử .................. Error! Bookmark not defined.
1.1.1.Phƣơng trình Schrodinger ........................... Error! Bookmark not defined.
1.1.2.Sự gần đúng Born – Oppenheirmer ............. Error! Bookmark not defined.
1.1.3.Phƣơng pháp biến phân ............................... Error! Bookmark not defined.
1.1.4.Thuyết trƣờng tự hợp Hartree – Fock ......... Error! Bookmark not defined.
1.1.5.Phƣơng trình Roothaan ............................... Error! Bookmark not defined.
1.2. Cơ sở của các phƣơng pháp tính gần đúng lƣợng tửError! Bookmark not defined.
1.2.1.Giới thiệu các phƣơng pháp tính gần đúng lƣợng tửError! Bookmark not defined.
1.2.2.Tƣơng quan electron .................................... Error! Bookmark not defined.
1.2.3.Bộ hàm cơ sở ............................................... Error! Bookmark not defined.
1.2.3.1.Obitan kiểu Slater và kiểu Gauss (STOs và GTOs)Error! Bookmark not defined.
1.2.3.2. Những bộ hàm cơ sở thƣờng dùng ........... Error! Bookmark not defined.
1.2.4.Phƣơng pháp phiếm hàm mật độ(DFT) ....... Error! Bookmark not defined.
1.2.4.1. Các định lý Hohenburg – Kohn (HK) ...... Error! Bookmark not defined.
1.2.4.2. Phƣơng pháp Kohn – Sham (KS) ............. Error! Bookmark not defined.
1.2.4.3. Sự gần đúng mật độ khoanh vùng ............ Error! Bookmark not defined.
1.2.4.4. Sự gần đúng gradient tổng quát ............... Error! Bookmark not defined.
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
1.2.4.5.Phƣơng pháp hỗn hợp .............................. Error! Bookmark not defined.
1.2.4.6.Một số phƣơng pháp DFT thƣờng dùng ... Error! Bookmark not defined.
Bề mặt thế năng ( Potential Energy Surface: PES)Error! Bookmark not defined.
1.3.
1.3.1. Bề mặt thế năng ......................................... Error! Bookmark not defined.
1.3.2. Điểm yên ngựa và đƣờng phản ứng . ........ Error! Bookmark not defined.
1.3.3. Tọa độ phản ứng thực ( Intrinsic Reaction Coordinate – IRC).Error! Bookmark not d
1.4.
Cơ sở lí thuyết về động hóa học. .................... Error! Bookmark not defined.
1.4.1. Tốc độ phản ứng ........................................ Error! Bookmark not defined.
1.4.1.1. Định nghĩa .............................................. Error! Bookmark not defined.
1.4.1.2. Các yếu tố ảnh hƣởng đến tốc độ phản ứng.Error! Bookmark not defined.
1.4.2. Cơ chế phản ứng, phân tử số và bậc của phản ứngError! Bookmark not defined.
1.4.2.1. Cơ chế phản ứng ...................................... Error! Bookmark not defined.
1.4.2.2. Phân tử số ................................................ Error! Bookmark not defined.
1.4.2.3. Bậc phản ứng .......................................... Error! Bookmark not defined.
1.4.3. Hằng số tốc độ phản ứng .......................... Error! Bookmark not defined.
1.4.3.1. Phản ứng bậc 1 ........................................ Error! Bookmark not defined.
1.4.3.2. Phản ứng bậc 2 ........................................ Error! Bookmark not defined.
1.4.3.3. Phản ứng bậc ba ..................................... Error! Bookmark not defined.
1.4.4.
Phƣơng pháp nghiên cứu động học của phản ứng phức tạpError! Bookmark not de
1.4.4.1. Phƣơng pháp nồng độ dừng ................... Error! Bookmark not defined.
1.4.4.2. Phƣơng pháp giai đoạn khống chế ......... Error! Bookmark not defined.
1.4.5.
Ảnh hƣởng của nhiệt độ đến tốc độ phản ứng. Năng lƣợng hoạt hóa.Error! Bookma
1.4.5.1. Quy tắc Van't Hoff (1852-1911) .............. Error! Bookmark not defined.
1.4.5.2. Năng lƣợng hoạt hóa .............................. Error! Bookmark not defined.
1.4.5.3. Biểu thức Areniuyt .................................. Error! Bookmark not defined.
1.4.5.4. Xác định năng lƣợng hoạt hóa ............... Error! Bookmark not defined.
1.4.6.
Phản ứng quang hóa học ......................... Error! Bookmark not defined.
1.4.7. Vài nét sơ lƣợc về xúc tác .......................... Error! Bookmark not defined.
1.4.8.
Thuyết phức hoạt động (Còn gọi là trạng thái chuyển tiếp)Error! Bookmark not de
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
CHƢƠNG 2: HỆ CHẤT NGHIÊN CỨU VÀ PHƢƠNG PHÁP NGHIÊN CỨUError! Bookmark
2.1. Hệ chất nghiên cứu ........................................... Error! Bookmark not defined.
2.1.1. Hiđro ........................................................... Error! Bookmark not defined.
2.1.2. Clo .............................................................. Error! Bookmark not defined.
2.1.3. Hiđro clorua (HCl) ..................................... Error! Bookmark not defined.
2.2. Phƣơng pháp nghiên cứu ................................... Error! Bookmark not defined.
2.2.1. Phần mềm tính toán ................................... Error! Bookmark not defined.
2.2.1.1. Phần mềm Gaussian 09 .......................... Error! Bookmark not defined.
2.2.1.2. Phần mềm Gaussview 5.0. ....................... Error! Bookmark not defined.
2.2.2. Lựa chọn phần mềm và phƣơng pháp tính toán.Error! Bookmark not defined.
2.2.2.1. Lựa chọn phần mềm . .............................. Error! Bookmark not defined.
2.2.2.2. Phƣơng pháp tính toán. .......................... Error! Bookmark not defined.
2.2.3. Xác định cơ chế phản ứng . ....................... Error! Bookmark not defined.
2.2.4. Tính các thông số nhiệt động ...................... Error! Bookmark not defined.
CHƢƠNG 3: KẾT QUẢ VÀ THẢO LUẬN ................. Error! Bookmark not defined.
3.1. Lựa chọn bộ hàm và phƣơng pháp tính .............. Error! Bookmark not defined.
3.2. Kết quả tính toán .................................................. Error! Bookmark not defined.
3.2.1. Kết quả tính toán lý thuyết .......................... Error! Bookmark not defined.
3.2.2 Xây dựng đƣờng cong thế năng của các giai đoạn phản ứngError! Bookmark not de
3.2.2.1. Phản ứng sinh mạch (phản ứng khơi mào)Error! Bookmark not defined.
3.2.2.2. Phản ứng phát triển mạch ..................... Error! Bookmark not defined.
3.2.2.3. Phản ứng ngắt mạch ............................................................................... 73
3.2.3. Tính các đại lƣợng nhiệt động học ................. Error! Bookmark not defined.
PHẦN KẾT LUẬN ..................................................... Error! Bookmark not defined.
ỨNG DỤNG TRONG GIẢNG DẠY HÓA HỌC TRUNG HỌC PHỔ THÔNG...80
TÀI LIỆU THAM KHẢO ..........................................................................................5
PHỤ LỤC
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
DANH MỤC KÍ HIỆU VIẾT TẮT
Kí hiệu
Tiếng Anh
Tiếng Việt
HHLT
Quantum Chemistry
Hóa học lượng tử
LUMO
Lowest Unoccupied Molecular Orbital
NBO
Natural Bond Obital
Obitan liên kết thuần khiết
AO
Atomic Orbital
Obitan nguyên tử
MO
Molecular Orbital
Obitan phân tử
LCAO
Linear Combination of Atomic Orbital
DFT
Density Functional Theory
LDA
Local Density Approximation
GGA
Generalised Gradient Approximation
ZPE
Zero Point Energy
Năng lượng điểm không
PES
Potential Energy Surface
Bề mặt thế năng
IRC
Intrinsic Reaction Coordinate
Tọa độ phản ứng thực
IS
Intermediate State
Trạng thái trung gian
TS
Transition State
Trạng thái chuyển tiếp
Vũ Thị Ngọc Lan
Obitan phân tử không bị
chiếm thấp nhất
Tổ hợp tuyến tính các
obitan nguyên tử
Thuyết phiếm hàm mật độ
Sự gần đúng mật độ địa
phương
Sự gần đúng gradient suy
rộng
Luận văn thạc sĩ
DANH MỤC BẢNG
Bảng 3.1. Năng lượng phân tử Cl2 với các phương pháp tính và bộ hàm khác nhau.Error! Book
Bảng 3.2. Năng lượng liên kết và độ dài liên kết của nguyên tử Cl và phân tử Cl2Error! Bookmar
Bảng 3.3. Bảng các giá trị năng lượng phân tử Cl2 tại các khoảng cách giữa hai
nguyên
tử
–
Cl
Cl…………………………………………………………...……..Error!
Bookmark not defined.
Bảng 3.4. Năng lượng và độ dài liên kết của phân tử H2, HCl, Cl-H-H và nguyên tử
Cl,
H………………………………………………………………………….…….Error
! Bookmark not defined.
Bảng 3.5. Bảng các giá trị năng lượng tính theo đơn vị (au) của phân tử Cl-H-H tại
các khoảng cách dCl - H theo các góc liên kết ClHH = 1800, 1500, 1350, 900Error! Bookmark no
Bảng 3.6. Bảng các giá trị năng lượng tính theo đơn vị (Kcal/mol) của phân tử Cl
H-H tại các khoảng cách dCl - H theo các góc liên kết ClHH = 1800,1500, 1350, 900..Error! Bookm
Bảng 3.7. Năng lượng phân tử Cl-H-H tại các khoảng cách dCl - H tương ứng và
theo góc 1800 làm chuẩn…………… ....................... Error! Bookmark not defined.
Bảng 3.8. Bảng các giá trị năng lượng phân tử Cl-H-H tại các khoảng cách dCl - H
theo góc liên kết CHH = 1800 ................................... Error! Bookmark not defined.
Bảng 3.9. Năng lượng và độ dài liên kết của phân tử H2, HCl, H-Cl-Cl và nguyên tử
Cl,
H…………………………………………………………………………...…...Error
! Bookmark not defined.
Bảng 3.10. Bảng các giá trị năng lượng tính theo đơn vị (au) phân tử H-Cl-Cl tại các
khoảng cách dCl - H theo các góc liên kết HClCl = 1800, 1500, 1350, 900Error! Bookmark not de
Bảng 3.11. Bảng các giá trị năng lượng tính theo đơn vị (Kcal/mol) phân tử H-ClCl
tại
Vũ Thị Ngọc Lan
các
khoảng
cách
dCl
-
H
Luận văn thạc sĩ
…….…………………………………………….......Error!
Bookmark
not
defined.
Bảng 3.12. Năng lượng phân tử H- Cl-Cl tại các khoảng cách tương ứng . ............ 70
Bảng 3.13. Năng lượng phân tử và độ dài liên kết của phân tử Cl2 và nguyên tử
Cl………………………………………………………………………………..….E
rror! Bookmark not defined.
Bảng 3.14A. Bảng năng lượng của các nguyên tử và phân tửError! Bookmark not defined.
Bảng 3.14B. Bảng năng lượng của các nguyên tủ và phân tửError! Bookmark not defined.
DANH MỤC HÌNH VẼ
Hình 1.1. Chu kì phản ứng xúc tác .......................... Error! Bookmark not defined.
Hình 1.2. Diễn biến năng lượng của hệ phản ứng có và không có xúc tác ...... Error!
Bookmark not defined.
Hình 1.3. Biến thiên thế năng theo đường phản ứng.Error! Bookmark not defined.
Hình 3.1. Phân tử Cl2 và nguyên tử Cl sau khi chạy mô phỏng động lực học bằng
Gaussian .................................................................... Error! Bookmark not defined.
Hình 3.2. Mô phỏng đường cong thế năng của phản ứng khơi màoError! Bookmark not defin
Hình 3.3. Phân tử H2, HCl, Cl-H-H, H-Cl-Cl và nguyên tử Cl, H sau khi chạy mô
phỏng động lực học bằng Gaussian .......................... Error! Bookmark not defined.
Hình 3.4. Mô phỏng đường cong thế năng của phản ứng (1) theo góc liên kết
0
0
0
0
ClHH = 180 , 150 , 135 , 90 .................................... Error! Bookmark not defined.
Hình 3.5. Mô phỏng đường cong thế năng của phản ứng (1) theo góc liên kết
0
ClHH = 180 ............................................................. .Error! Bookmark not defined.
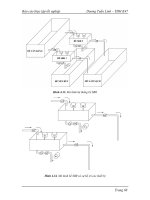
Hình 3.6. Phân tử Cl2, HCl, Cl-Cl-H, và nguyên tử H, Cl sau khi chạy mô phỏng
động lực học bằng Gaussian ..................................... Error! Bookmark not defined.
Hình 3.7. Mô phỏng đường cong thế năng của phản ứng (2) theo góc liên kết
HClCl
= 1800, 1500, 1350, 900 ............................... Error! Bookmark not defined.
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
Hình.3.8. Mô phỏng đường cong thế năng của phản ứng (2) theo góc liên kết
0
HClCl = 90 .............................................................. Error! Bookmark not defined.
Hình 3.9. Nguyên tử Cl và phân tử Cl2 sau khi chạy mô phỏng động lực học bằng
Gaussian……………………………………………………………………...…….Er
ror! Bookmark not defined.
Hình 3.10. Mô phỏng đường cong thế năng của phản ứng ngắt mạchError! Bookmark not de
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
PHẦN MỞ ĐẦU
I.
Lí do chọn đề tài
Hóa học lượng tử (HHLT) là ngành khoa học nghiên cứu các hệ lượng tử
dựa vào phương trình chính tắc của CHLT do Schrodinger đưa ra năm 1926 . Với
sự xuất hiện của HHLT đã nhanh chóng làm thay đổi cơ bản quan niệm về thế giới
vi mô nhiều ngành khoa học đặc biệt trong nghiên cứu hóa học.
HHLT giúp tìm hiểu sâu, nghiên cứu vấn đề cốt lõi nhất của hóa học là cấu
trúc và tính chất hóa lý của các chất. Bên cạnh sự phát triển mạnh mẽ của công nghệ
máy tính và sự ra đời của các phần mềm máy tính phục vụ trong việc tính HHLT
như MOPAC, HYPERCHEM, GAUSSIAN, GAUSSVIEW, VASP….Giúp cho
việc nghiên cứu HHLT được mở rộng hơn. Phần mềm tính toán cho ta biết nhiều
tham số về xác định cấu trúc phân tử, tham số về bề mặt thế năng, tham số về các
đại lượng nhiệt động học như: ∆H; ∆G; cũng như các đại lượng động học như E, tốc
độ phản ứng…. HHLT còn làm sáng tỏ nhiều cơ chế của phản ứng hóa học, giải
thích đúng đắn các quy luật hóa học, kiểm tra được kết quả thực nghiệm. Đặc biệt,
nó còn thể hiện tính ưu việt là nghiên cứu sự chuyển tiếp giữa các chất trung gian
mà có thời gian xảy ra rất ngắn. Khảo sát các phản ứng hóa học trong các điều kiện
khác nhau, nhất là đối với những phản ứng khó, phản ứng độc hại hay không thể
thực hiện được, đồng thời tiết kiệm được về kinh tế.
Với mong muốn học hỏi, hiểu biết thêm về HHLT, tìm hiểu bản chất của
phản ứng nên tôi chọn đề tài nghiên cứu:
“ Kiểm nghiệm cơ chế phản ứng H2(k)+ Cl2(k) → 2HCl(k) bằng phƣơng
pháp tính hóa học lƣợng tử”
II. Mục đích nghiên cứu.
Sử dụng lý thuyết hóa học lượng tử và các phương pháp tính toán gần đúng,
tốt áp dụng cho hệ nghiên cứu nhằm thu được các tham số về cấu trúc, tần số dao
động và các loại năng lượng… của hệ các chất tham gia, các chất sản phẩm, các
chất trung gian và các trạng thái chuyển tiếp qua đó thiết lập bề mặt thế năng đầy đủ
để giải thích cơ chế phản ứng.
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
TÀI LIỆU THAM KHẢO
Tiếng Việt
1. H. Eyring, J. Walter, G.E. Kimball (1948), Hóa học lƣợng tử (1976)bản dịch
tiếngViệt, Nhà xuất bản Khoa học và Kỹ thuật Việt Nam, Hà Nội.
2. Trần Thành Huế (2003), Hóa học đại cƣơng, Nhà xuất bản giáo dục, Hà Nội.
3. Trần Thành Huế (2006), Tƣ liệu hóa học 10, Nhà xuất bản giáo dục, Hà Nội.
4. Nguyễn Đình Huề, Nguyễn Đức Chuy (2003), Thuyết lƣợng tử về nguyên tử và
phân tử (Tập 1,2), NXBGD, Hà Nội.
5. Đoàn Minh Hùng (2015), Khảo sát thông số nhiệt động, đƣờng phản ứng của gốc
tự do Etinyl (C2H) với phân tử acryonitrin (C3H3N) trong pha khí bằng
phƣơng pháp tính hóa học lƣợng tử, Luận văn thạc sĩ, Đại học Sư phạm Hà
Nội.
6. Lê Văn Huỳnh (2014), Hóa học các nguyên tố, Nhà xuất bản Khoa học tự nhiên
và công nghệ, Hà Nội.
7. Nguyễn Hà Mi (2012), Khảo sát một số dẫn xuất halogen, ancol, phenol và axit
cacboxylic bằng phƣơng pháp hóa học lƣợng tử, Luận văn thạc sĩ, Đại học
Khoa học tự nhiên.
8. Phạm Thị Thu Ngọc (2014), Nghiên cứu lý thuyết cơ chế phản ứng N2O + H2
trong pha khí và trên nền xúc tác cluster Rh5, Luận văn thạc sĩ, Đại học Sư
phạm Hà Nội.
9. Hoàng Nhâm (2000), Hóa vô cơ (Tập 2), NXBGD, Hà Nội.
10. Trần Văn Nhân, Nguyễn Thạc Sửu, Nguyễn Văn Tuế, (2006), Hóa lí (Tập 2,3),
NXBGD, Hà Nội.
11. Nguyễn Hữu Phú (2006), Hóa lý và Hóa keo, NXBKHKT, Hà Nội.
12. Lâm Ngọc Thiềm, Phạm Văn Nhiêu, Lê Kim Long (2008), Cơ sở hóa học lƣợng
tử, NXBKHKT, Hà Nội.
13. Đào Đình Thức (2005), Cấu tạo nguyên tử và liên kết hóa học (Tập 1,2), Nhà
xuất bản giáo dục, Hà Nội.
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
14. Nguyễn Ngọc Trí (2015), Bƣớc đầu nghiên cứu động học của phản ứng đơn
phân tử phụ thuộc áp suất bằng phƣơng pháp tính hóa học lƣợng tử, Luận
văn thạc sĩ, Đại học Sư phạm Hà Nội.
15. Hồ Ngọc Tuấn (2015), Nghiên cứu lí thuyết cơ chế phản ứng của gốc etinyl với
phân tử etanol trong pha khí bằng lý thuyết phiếm hàm mật độ, Luận văn
thạc sĩ, Đại học Sư phạm Hà Nội.
16. Đặng Ứng Vận (1998), Tin học và ứng dụng trong hóa học, Nhà xuất bản giáo
dục, Hà Nội.
17. Đào Hữu Vinh, Nguyễn Duy Ái (2014), Tài liệu chuyên Hóa học 10 (Tập 2),
Nhà xuất bản giáo dục, Hà Nội.
Tiếng Anh
18. Eleen Frisch, Hrantchian, P. Hrat Roy D. Dennington II, Todd A. Keith, John
Millam,…(2009), GaussView 5 Reference, Gaussian, Inc.
19. Gloria A.A. Saracino, Roberto Improta, Vincenzo Barone (2003), “Absolute
pKa determination for cacboxylic acids using density functional theory and
the polarizable continuum model”, Chemical Physics Letters, 373, pp. 411415.
20. John A. Keith, Emily A. Carter (2012), “Quantum Chemical Benchmarking,
Validation, and Prediction of Acidity Constants for Substituted Pyridinium
Ions and Pyridinyl Radicals”, Journal of Chemical Theory and
Computation, 8, pp. 3187-3206.
21. Kristin S. Along, George C. Sheilds (2010), “Chapter 8 Theoretical Calculations
of Acid Dissociation Constants: A Review Artical”, Annual Reports in
Computation Chemistry, Volum 6, pp. 113-138.
22. Matthew D. Liptak, George C. Shields (2001), “Accurate pKa Calculation for
Carboxylic Acids Using Complete Basis Set and Gaussian-n Models
Combined with CPCM Continuum Solvation Methods”, J. Am. Chem. Soc,
123, pp. 7314-7319.
Vũ Thị Ngọc Lan
Luận văn thạc sĩ
23. Vyacheslav S. Bryantsev, Mamadou S. Diallo, Adri C. T. van Duin, William A.
Goddard III (2009), “Evaluation of B3LYP, X3LYP and M06-Class
Density Functionals for Predicting the Binding Energies of Neutral,
Protonated, and Deprotonated Water Clusters”, Journal of Chemical Theory
and Computation, 5, pp. 1016-1026.
Vũ Thị Ngọc Lan