ma tran de thi Hóa 8 ki 1
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (104.63 KB, 3 trang )
TRƯỜNG THCS TRẤN NINH
KIỂM TRA HỌC KỲ I
Năm học 2017- 2018
Môn: Hóa học 8
I. Mục tiêu.
- Kiểm tra sự hiểu biết kiến thức của học sinh trong một học kì về chất, nguyên tử, phân tử,
phản ứng hóa học, mol và tính toán hóa học.
II. Hình thức:
- Trắc nghiệm và tự lận
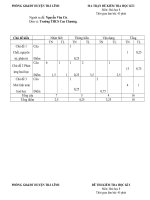
Ma trân đề kiểm tra
Nội dung
1. Chất nguyên tử phân tử.
Số câu
Số điểm
Tỉ lệ
2. Phản ứng
hoá hoc.
Số câu
Số điểm
Tỉ lệ
3. Mol và
tính toán
hoá học.
Số câu
Số điểm
Tỉ lệ
Tổngsố câu
Tổng số
điểm
Tỉ lệ %
Nhận Biết
TNKQ
TL
Biết cấu tạo
nguyên tử,
nguên tố hoá
học
1
0,5đ
=5 %
- Biết vận
Lập PTHH
dụng quy tắc
hóa trị chỉ ra
CTHH phù
hợp
1
1
0,5đ
2
=5%
=20%
Biết Áp
dụng CT tính
tỉ khối
hợp chất.
1
0,5đ
=5%
3
1,5đ
=15%
1
2đ
=20%
Mức độ kiến thức kĩ năng
Thông hiểu
Vận dụng
TNKQ
TL
TNKQ
TL
Biết ý
.
nghĩa
của
CTHH
1
0,5đ
=5 %
Tổng số
2
1đ
=10%
2
2,5đ
=25%
1
0,5đ
= 5%
Áp dụng
tính thể
.
tích
Áp dụng
CT tính
thành
phần phần
trăm các
nguyên tố
trong
1
3đ
=30%
1
3đ
= 30%
- Áp dụng
tính thể
tích và tỉ
lệ các
chất trong
phản
ứng .
1
3đ
=30%
1
3đ
=30%
3
6,5đ
= 65%
7
10đ
=100%
TRƯỜNG THCS TRẤN NINH
ĐỀ KIỂM TRA HỌC KỲ I
Năm học 2017- 2018
Môn: Hóa học 8
(Thời gian làm bài: 45 phút)
ĐỀ CHÍNH THƯC
I. Trắc nghiệm khách quan (2đ).
Chọn và chép lại đáp án đúng nhất.
Câu 1. Hạt nhân nguyên tử cấu tạo bởi:
A. Proton và electron
B. Proton và nơtron
C. Nơtron và electron
D. Proton, nơtron và electron.
Câu 2. Có 3 nguyên tử natri; 5 nguyên tử hiđro; 6 nguyên tử cacbon; 2 phân tử nước; 2
nguyên tử clo. Cách diễn đạt nào sau đây là đúng.
A. Na3; 5H2; 6C; 2H2O; 2Cl.
B. 3Na; 5H2; 6C; 2H2O; 2Cl2
C. 3Na; 5H; 6C; 2H2O; 2Cl2.
D. 3Na; 5H; 6C; 2H2O; 2Cl
Câu 3. CTHH của hợp chất nguyên tố R với nhóm SO4(II) là R2(SO4)3. CTHH của hợp
chất nguyên tố R với clo là:
A. RCl
B. RCl2
C. RCl3
D. RCl4
Câu 4. Chất khí A có d A/ H 14 CTHH của A là:
A. Cl2
B. CO2
C. C2H4
D. NH3
II. Tư luân (8đ).
Câu 1. (2đ) Lâp CTHH của hợp chất gồm các nguyên tố sau:
a. Kẽm (II) và nhóm SO4(II)
b. Lưu huỳnh (IV) và oxi.
Câu 2. (3đ)
a. Tính thể tích ở (đktc) của hỗn hợp khí gồm 0,75 mol N2 và 0,25 mol H2.
b. Tính thành phần phần trăm của Cu trong các hơp chất: CuO; CuSO4.
c. Lập PTHH sau: 1. P + O2 →
P2O5
2. Fe + HCl FeCl2 + H2
Câu 3 (3đ). Cho 13,5 gam nhôm tác dụng với HCl theo phản ứng sau:
Al + HCl →
AlCl3 + H2
a. Lập phương trình phản ứng?
b. Xác định tỉ lệ các chất của phản ứng?
c. Tính thể tích H2 sinh ra ở (đktc).
2
HẾT
- Học sinh không được sử dụng tài liệu khi làm bài.
- Giám thị không giải thích gì thêm
TRƯỜNG THCS TRẤN NINH
HƯỚNG DẨN CHẤM KIỂM TRA HỌC KỲ I
Năm học: 2017-2018
Môn: Hóa học 8
I. Trắc nghiệm khách quan. (2 đ)
Câu 1. B. Proton và nơtron
Câu 2. D. 3Na; 5H; 6C; 2H2O; 2Cl
Câu 3. C. RCl3
Câu 4. C. C2H4
II. Tư luân (8đ).
Câu 1. (2 điểm) a. – công thức chung : Znx( SO4 )y
- Theo qui tắc hóa trị: X.II = Y.II
- Chuyển tỉ lệ : x/y = II/II = 1/1
Ta có : x = 1, y = 1
Vậy công thức của hợp chất là:
ZnSO4
b.- công thức chung : SxOy
- Theo qui tắc hóa trị: X.IV = Y.II
- Chuyển tỉ lệ : X/Y = II/IV = 1/2
Ta có : x =1, y = 2
Vậy công thức của hợp chất là:
* MCuSO4 = 160(g)
%Cu = 64.100%/160 = 40%
Trong CuSO4: % Cu = 40%
0,25đ
0,25đ
0,25đ
0,25đ
0,25đ
0,25đ
0,25đ
SO2
Câu 2. (3 điểm)
a. VN2 = 0,75.22,4 = 16,8(lít)
VH2 = 0,25.22,4 = 5,6(lít)
Vhh(đktc) = VN2 + VH2 = 16,8(lít) + 5,6(lít) = 22,4(lít)
b. * MCuO = 80(g)
%Cu = 64.100% /80 = 80%
Trong CuO: % Cu = 80%
0,5đ
0,5đ
0,5đ
0,5đ
0,25đ
0,25đ
0,25đ
0,5đ
0,25đ
0,25đ
0,25đ
0,25đ
c. PTHH sau: 1. 4P + 5O2 →
2P2O5
0,5đ
2. Fe + 2HCl FeCl2 + H2
0,5đ
Câu 3. (3 điểm)
a. Al + HCl → AlCl3 + H2
0,5đ
2Al + 6 HCl → 2AlCl3 + 3H2
0,5đ
b. Tỉ lệ: nguyên tử Al : phân tử HCl : phân tử AlCl3 : phân tử H2 = 2 : 6 : 2 : 3
1đ
c. VH2 (đktc) =15,6(lit)
1đ