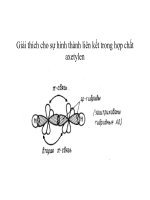
bài giảng hóa học hữu cơ phan thanh sơn nam rất hay
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (3.59 MB, 458 trang )
1
Hóa
HọcHữuCơ
TS Phan
Thanh
SơnNam
Bộ
môn
Kỹ
ThuậtHữuCơ
Khoa
Kỹ
ThuậtHóaHọc
Trường
ĐạiHọc
Bách
Khoa
TP. HCM
Điệnthoại: 8647256 ext. 5681
Email:
2
Tài
liệuthamkhảo
[1] Paula Y. Bruice, ‘Organic chemistry’,
fifth edition, Pearson
Prentice Hall, 2007
[2] Graham T.W. Solomons, Craig B. Fryhle, ‘Organic chemistry’,
eighth edition, John Wiley & Sons, 2004
[3] Francis A. Carey, ‘Organic chemistry’, fifth edition, McGraw-
Hill, 2003
[4] Robert T. Morrison, Robert N. Boyd, ‘Oragnic
chemistry’,
sixth
edition, Prentice Hall, 1992
[5] TrầnThị
Việt
Hoa, Phan
Thanh
SơnNam, ‘Hóa
hữucơ’,
NXB
ĐạiHọcQuốc
Gia
–
HCM, 2007
[6] TrầnT
hị
ViệtH
oa, TrầnVănThạnh, ‘Bài
tậphoáhữucơ’, NXB
ĐạiHọcQuốc
Gia
–
HCM, 2004
[8] Thái
Doãn
Tĩnh, ‘Cơ
sở
lý
thuyết
hoá
hữucơ’,
NXB Khoa
Học
Kỹ
Thuật, 2000
[9] TrầnQuốcSơn, ‘Cơ
sở
lý
thuyếthóahữucơ’,
NXB Giáo
Dục,
1979
3
NỘI DUNG CHÍNH
• Đồng
phân
củahợpchấthữucơ
• Hiệu
ứng
trong
hợpchấthữucơ
• Cơ
chế
các
phản
ứng
củahợpchấthữucơ
• Alkane
• Alkene
• Alkyne
• Alkadiene
• Hợpchất
hydrocarbon thơm
• Dẫn xuất halogen
• Alcohol –
Phenol
• Aldehyde –
Ketone
• Carboxylic acid
• Amine
–
Hợpchấtdiazonium
4
Chương 1:
ĐỒNG PHÂN
• Đồng
phân: những
hợpchấthữucơ
có
công
thức
phân
tử
giống
nhau, công
thức
cấutạokhácnhauÆ tính chất hóa học, vật
lý, sinh học khác nhau
• Phân
loại:
+ Đồng
phân
cấutạo(phẳng)
+ Đồng
phân
lậpthể: đồng
phân
hình
học
(cis, trans), đồng
phân
quay (cấudạng),
đồng
phân
quang
học
5
I.
Đồng
phân
cấutạo
Do có
sự
sắpxếp
khác
nhau
của
các
nguyên
tử
trong
mạch
C
I.1. Đồng
phân
mạch
C
C
6
H
12
n-butane
iso-butane
methyl cyclopentane
cyclohexane
6
I.2. Đồng
phân
do vị
trí
các
liên
kếtbội, nhóm
chức
OH
OH
OH
OH
OH
OH
C
4
H
8
butene-1 butene-2
1,2- 1,3- 1,4-
dihydroxy benzene
7
I.3. Đồng
phân
có
nhóm
định
chức
khác
nhau
O
CHO
C
3
H
6
O
dimethyl ketone
propan-2-one
acetone
propionaldehyde
propanal
propionic aldehyde
C
3
H
6
O
2
COOH
O
O
Propionic acid
methyl acetate
8
I.4. Đồng
phân
có
nhóm
thế
khácnhauliênkếtvới
nhóm
định
chức
O
O
C
4
H
10
O
diethyl ether
methyl propyl ether
9
II. Đồng
phân
lậpthể
II.1. Đồng
phân
hình
học
II.1.1. Điềukiệnxuấthiện
đồng
phân
hình
học
• Xuấthiện
khi
phân
tử
có
1 bộ
phậncứng
nhắc
Æ cảntrở sự quay tự do của các nguyên tửở
đó
• 2 nguyên
tử
liên
kếtvới
cùng
1 nguyên
tử
của
bộ
phậncứng
nhắcphải
khác
nhau
10
H
Cl Cl
H
• Thường
xuấthiện
ở
các
hợpchấtcóchứa:
C=C, C=N, N=N, hệ
liên
hợp, vòng
phẳng
3
hay 4 cạnh
abC=Ccd: a ≠
b, c ≠
d
11
II.1.2. Danh
pháp
của
đồng
phân
hình
học
a. Hệ
cis-trans:abC=Cab
• Nhóm
thế
tương
đương
nằm
cùng
phía
mặtphẳng
liên
kết
π Æ cis
• Khác
phía Æ trans
H
H
3
C CH
3
H
H
H
3
C H
CH
3
cis-butene-2 trans-butene-2
12
b. Hệ
Z-E: abC=Ccd a>b
c>d
Quy
tắc
Kahn-Ingold-Prelog: dựatheothứ
tựưutiêntrongbảng
HTTH của
nhóm
thế
a, c cùng
phía
so vớimặtphẳng
nối
đôi:
Z
(zusammen)
a, c khác
phía
so vớimặtphẳng
nối
đôi: E
(entgegen)
13
I
Br Cl
F
I
Br F
Cl
(E)-1-Bromo-2-chloro-2-fluoro-1-iodoethene
35
53
17
9
(Z)-1-Bromo-2-chloro-2-fluoro-1-iodoethene
•Lưu
ý: Khi
dùng
Z-E, chú
ý Z, E
không
phải
luôn
trùng
với
cis, trans
H
Cl Cl
Br
E-, cis-
F
Cl Cl
H
Z-, cis-
14
II.1.3. Đồng
phân
hình
họccủaabC=Ndvà
aN=Nb
a.
abC=Nd
• Trước
đây, dùng
hệ
syn-, anti-,
nhưng
không
chính
xác
nên
hiện
nay dùng
hệ
Z-E
• a>b: a, d khác
phía
so vớimặtphẳng
nối
đôi Æ E, cùng phía Æ Z
• Đốivới
aldoxime
CN
H
H
3
COH
CN
H
H
3
C
OH
anti-acetaldoxime
(Z)-acetaldoxime
syn-acetaldoxime
(E)-acetaldoxime
15
• Đốivới
ketoxime: Cùng
1 chất, có
thể
gọilà
syn-
hay anti-
!!!
CN
OH
H
3
C
CN
OH
anti-phenyl-p-tolylketoxime
syn-p-tolyl-phenylketoxime
syn-phenyl-p-tolylketoxime
anti-p-tolyl-phenylketoxime
H
3
C
Æ hệ syn-anti không chính xác Æ
chuyển sang hệ Z-E
16
b. aN=Nb
NN
C
6
H
5
C
6
H
5
NN
C
6
H
5
C
6
H
5
anti-azobenzene
syn-azobenzene
17
II.1.4. Đồng
phân
hình
họccủahợpchấtchứaC=C
liên
hợp
a(HC=CH)
n
b
H
H
C
6
H
5
C
6
H
5
H
H
H
C
6
H
5
H
H
C
6
H
5
H
H
C
6
H
5
H
C
6
H
5
H
H
trans,trans-1,4-diphenyl-1,3-butadiene
cis,cis-1,4-diphenyl-1,3-butadiene
cis,trans-1,4-diphenyl-1,3-butadiene
* Sốđphìnhhọccủahệ
liên
hợpC=C
N = 2
n-1
+ 2
p-1
n: số
nối
đôi
liên
hợp
p = n/2 nếun chẵn
p = (n + 1)/2 nếun lẻ
18
II.1.5. Đồng
phân
hình
họccủa
vòng
no 3, 4
cạnh
• Đượcbố
trí
trên
1 mặtphẳng Æ các nhóm thế
không thể quay tự do Æ xuấthiện đồng phân
hình học
* Các
nhóm
thế
tương
đương
cùng
phía
mặtphẳng
Æ cis, khác phía Æ trans
HOOC
H
COOH
H
HOOC
H
H
COOH
cis-cyclopropane-1,2-dicarboxylic acid trans-cyclopropane-1,2-dicarboxylic acid
19
II.1.6. Cách
xác
định
và
so sánh
các
đồng
phân
hình
học
a. xác
định
khoảng
cách
giữa
các
nhóm
thế
Khoảng
cách
giữa
2 nhóm
thế
tương
đương
trong
đồng
phân
cis
< trans
Cl
H H
Cl
Cl
H Cl
H
3.7 Å
4.7 Å
20
b. Moment lưỡng
cực
• 2 nhóm
thế
giống
nhau
aHC=CHa
Cl
H H
Cl
Cl
H Cl
H
μcis
(1.89D) > μtrans
(0D)
• 2 nhóm
thế
khác
nhau
aHC=CHb
(a ≠
b)
•2 nhóm
thế
cùng
hút
hay cùng
đẩy
điệntử:
μcis
> μtrans
•2 nhóm
thế
có
tính
chất
điệntử
ngược
nhau:
μcis
< μtrans
21
c. Nhiệt
độ
nóng
chảy
• Đồng
phân
trans-: đốixứng Æ mạng lưới
tinh thể chặtchẽ
Æ
t
o
nc cis < t
o
nc trans
• Lưuý: mốiliênhệ
giữat
o
sôi
và
đồng
phânhìnhhọc
không
chặtchẽ
Ví
dụ:
CHCl=CHCl
t
o
sôi
của
cis-: 60.3
o
C, t
o
sôi
của
trans-: 48.4
o
C
CH
3
CH=CHCl
t
o
sôi
của
cis-: 32.8
o
C, t
o
sôi
của
trans-: 37.4
o
C
22
II.2. Đồng
phân
cấudạng
(đồng
phân
quay)
• Là
những
cấu
trúc
không
gian
sinh
ra
do 1 nhóm
thế
quay xung
quanh
trục
C-C (không
làm
đứtC-C)
so với
1 nhóm
nguyên
tử
khác
• Thường
cầnnăng
lượng
3-4 Kcal/mol
• Chỉ
tồntạinhững
cấudạng
tương
đốibền
• Không
thể
tách
thành
những
đồng
phân
riêng
rẽ!!!
• Đồng
phân
cấudạng
là
các
dạng
khác
nhau
trong
không
gian
củacùng1 cấu
hình!!!
23
II.2.1. Cách
biểudiễn
a. Công
thứcphốicảnh
(không
gian
3 chiều)
c
b
c
a
b
a
a
b
c
a
b
c
c
b
a
che
khuất
xen
kẽ
• Liên
kết
C-C: đường
chéo
trái
qua phải, xa
dầnngười
quan
sát
24
b. Công
thứcNewman
•
Quan
sát
dọctheoC-C Æ 2 nguyên tử C ở
dạng che khuất, biểudiễnbằng vòng tròn
Æ chiếu các nhóm thế lên mặtphẳng vuông
góc vớiC-C
a
a
bc
aa
b
b
c
c
c
b
che
khuất
xen
kẽ
25
II.2.2. Cấudạng
của
các
hợpchấtmạch
hở
a. Ethane
• Quay 1 nhóm
CH
3
& cốđịnh
nhóm
còn
lại Æ
2 đồng phân cấudạng tớihạn
• Che
khuất: khoảng
cách
giữa
các
H gần
nhau Æ năng lượng cao nhất Æ kém bền
nhất