BÀI 15 16 17: TÍNH CHẤT CỦA KIM LOẠI. DÃY HOẠT ĐỘNG HÓA HỌC CỦA KIM LOẠI
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (118.93 KB, 6 trang )
Ngày soạn:
Ngày giảng:
Tiết 22
BÀI 15, 16, 17: TÍNH CHẤT CỦA KIM LOẠI. DÃY HOẠT ĐỘNG
HÓA HỌC CỦA KIM LOẠI
I. Mục tiêu
1. Kiến thức
- Củng cố kiến thức về những tính chất vật lí, hóa học của kim loại, dãy hoạt
động hóa học của kim loại.
2. Năng lực
* Năng lực chung: Năng lực giao tiếp, năng lực tự học, năng lực hợp tác.
*Năng lực riêng: Năng lực sử dụng ngôn ngữ hóa học, năng lực thực hành hóa
học, năng lực vận dụng kiến thức hóa học vào cuộc sống.
3. Phẩm chất:
- u thích học tập bộ mơn. Chăm chỉ, trung thực trong học tập.
II. Thiết bị dạy học và học liệu
1. Giáo viên: Hệ thống bài tập
2. Học sinh: Ôn tập bài 15, 16, 17 Tính chất hóa học của kim loại, dãy hoạt
động hóa học của kim loại.
III. Phương pháp, kĩ thuật
- Thảo luận nhóm, vấn đáp gợi mở.
- Kĩ thuật chia nhóm, kĩ thuật đặt câu hỏi...
III. Tiến trình dạy học.
A. Hoạt động mở đầu ( 6p)
- Mục tiêu:
- Nội dung:
- Sản phẩm:
- Cách tổ chức thực hiện:
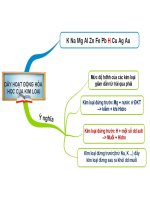
GV: tổ chức trò chơi thi giữa 2 đội: Yêu cầu HS viết sơ đờ tư duy về tính chất
của Kim loại và dãy hoạt động của kim loại, ý nghĩa dãy hoạt động
HS: Thực hiện theo yêu cầu của GV, cử 5 hs viết lên bảng lớp
HS: thảo luận nhóm viết câu trả lời vào phiếu học tập. Sau 3 phút cử 5 bạn viết
nhanh lên bảng, mỗi HS viết 1 lần
HS: nghe câu trả lời, nhận xét, bổ sung nếu có.
Gv: nhận xét, đánh giá điểm và nêu vấn đề
B. Hoạt động hình thành kiến thức
Hoạt động 1: Kiến thức cần nhớ: 7’
- Mục tiêu: - Củng cố kiến thức về những tính chất vật lí, hóa học của kim loại,
dãy hoạt động hóa học của kim loại.
- Nội dung:
- Sản phẩm:
- Cách tổ chức thực hiện:
Hoạt động của GV-HS
Nội dung ghi bảng
Gv: Sử dụng lại phần hoạt động
I. Kiến thức cần nhớ:
1. Tính chất của kim loại
nhóm trong phần khởi động
? Nhắc lại tính chất vật lí của kim
2. Dãy hoạt động hóa học của
loại
kim loại, ý nghĩa của dãy hoạt
HS: Trả lời cá nhân
động
GV: Nhắc lại tính chất hóa học của
kim loại
HS: Trả lời cá nhân
GV: Chốt lại qua sơ đờ tư duy của
các nhóm
GV: Nêu ý nghĩa của dãy hoạt động
hóa học của kim loại?
HS: Trả lời cá nhân
GV: Chiếu lại dãy hoạt đọng và ý
nghĩa cảu dãy hoạt động hóa học của
kim loại
Hoạt động 2: Bài tập: 15’
Mục tiêu: - Củng cố kiến thức về những tính chất vật lí, hóa học của kim loại,
dãy hoạt động hóa học của kim loại thơng qua hệ thống bài tập.
- Nội dung:
- Sản phẩm:
- Cách tổ chức thực hiện:
Hoạt động của GV-HS
GV chiếu các nhiệm vụ học tập
- HS chia nhóm, phân nhóm trưởng,
thư kí
BT1.Khi mới cắt, miếng natri có bề
mặt sáng trắng của kim loại. Sau khi
để một lát trong khơng khí thì bề mặt
đó khơng cịn sáng nữa mà bị xám
lại. Tại sao phải bảo quản Na trong
dầu hoả?
Nội dung ghi bảng
II. Bài tập
BT1.
Vì Na tác dụng mạnh với oxi ngồi
khơng khí tạo Natri oxit. Vì vậy cần
bảo quản Na trong dầu hoả.
BT2.
Vì nhơm có khối lượng riêng nhe
BT2.Nhôm được dùng làm dây dẫn hơn đồng được dùng làm dây dẫn
điện cao thế còn dây đồng lại được điện cao thế cịn dây đờng lại được
dùng làm dây dẫn điện trong nhà
dùng làm dây dẫn điện trong nhà vì
dẫn điện tốt hơn nhôm.
BT3..Tại sao không thể dập tắt đám BT 3:
cháy của các kim loại: K, Na, Mg Vì sản phẩm của chúng là K 2O,
bằng khí CO2
Các nhóm HS: chú ý lắng nghe, trả
lời câu hỏi, nhanh chóng ghi ra bảng
phụ
-GV tổ chức cho hs báo cáo kết quả
tìm được
Na2O, MgO dễ dàng tác dụng với khí
CO2
-HS: đại diện học sinh các nhóm lên
báo cáo kết quả, các nhóm
-GV nhận xét, chốt kiến thức, cho
điểm từng
Bài 1 Trang 54 SGK Hóa 9 Bài 17
Dãy các kim loại nào sau đây được
sắp xếp đúng theo chiều hoạt động
hoá học tăng dần?
a) K, Mg, Cu, Al, Zn, Fe;
b) Fe, Cu, K, Mg, Al, Zn;
c) Cu, Fe, Zn, Al, Mg, K;
d) Zn, K, Mg, Cu, Al, Fe;
e) Mg, K, Cu, Al, Fe.
HS: Trả lời cá nhân
Bài 2 Trang 54 SGK Hóa 9 Bài 17
Dung dịch ZnSO4 có lẫn tạp chất là
CuSO4. Dùng kim loại nào sau đây
để làm sạch dung dịch ZnSO4? Hãy
giải thích và viết phương trình hoá
học.
a) Fe; b) Zn; c) Cu; d) Mg.
HS: Thảo luận cặp đơi trả lời
Bài 3 Trang 54 SGK Hóa 9 Bài 17
Viết các phương trình hoá học:
a) Điều chế CuSO4 từ Cu.
b) Điều chế MgCl2 từ mỗi chất sau:
Mg, MgSO4, MgO, MgCO3.
(Các hố chất cần thiết coi như có
đủ).
HS: Thảo luận nhóm 2 bàn, trả lời
GV: nhận xét, chốt kiến thức đúng
Bài 1 Trang 54
c) gồm các kim loại: Cu, Fe, Zn, Al,
Mg, K được sắp xếp theo chiều hoạt
động hóa học tăng dần.
Bài 2 Trang 54
Dùng kim loại Zn vì có phản ứng:
Zn(r) + CuSO4(dd) -> ZnSO4(dd) +
Cu(r)
Nếu dùng Zn dư, Cu tạo thành không
tan được tách ra khỏi dung dịch và ta
thu được dung dịch ZnSO4 tinh khiết
Bài 3 Trang 54 SGK
a) Cu + 2H2SO4 đặc, nóng →
CuSO4 + SO2 + 2H2O
2Cu + O2 → 2CuO
CuO + H2SO4 → CuSO4 + H2O
b) Mg + 2НСl → MgCl2 + H2
Mg + CuCl2 → MgCl2 + Cu
MgSO4 + BaCl2 → MgCl2 + BaSO4
Bài 4 Trang 54 SGK Hóa 9 Bài 17
Hãy cho biết hiện tượng xảy ra khi
cho
a) Kẽm vào dung dịch đồng clorua.
b) Đồng vào dung dịch bạc nitrat.
c) Kẽm vào dung dịch magie clorua.
d) Nhôm vào dung dịch đồng clorua.
Viết các phương trình hố học, nếu
có.
HS: Trả lời cá nhân
Bài 5 Trang 54 SGK Hóa 9 Bài 17
Cho 10,5 gam hỗn hợp 2 kim loại
Cu, Zn vào dung dịch H2SO4 lỗng
dư, người ta thu được 2,24 lít khí
(đktc).
a) Viết phương trình hố học.
b) Tính khối lượng chất rắn cịn lại
sau phản ứng.
HS: nêu phương hướng giải bài tập
GV: Giúp HS hình thành sơ đồ giải
HS: làm bài cá nhân, chưa, nhận xét
GV: Chốt kiến thức và cho điểm
MgO + 2HCl → MgCl2 + H2O
MgCO3 + 2HCl → MgCl2 + CO2 +
H2O
Bài 4 Trang 54 SGK
a) Có chất rắn màu đỏ bám vào bề
mặt kẽm, màu xanh của dung dịch
nhạt dần:
CuCl2 (dd) + Zn(r) -> ZnCl2(dd) +
Cu(r)
b) Hiện tượng, PTHH trong bài học.
c) Khơng có hiện tượng xảy ra và
khơng có phản ứng.
d) Có chất rắn màu đỏ bám vào bề
mặt nhôm, màu xanh của dung dịch
nhạt dần.
2Al(r) + 3CuCl2(dd) -> 2AlCl3 +
Cu(r)
Xanh
đỏ
Bài 5 Trang 54 SGK
Số mol H2 = 2,24 : 22,4 = 0,1 mol.
a) Khi cho hỗn hợp (Zn, Cu) vào
dung dịch H2SO4 lỗng, chỉ có Zn
phản ứng:
Zn + H2SO4 → ZnSO4 + Н2
Phản ứng: 0,1 ← 0,1 (mol)
b) Chất rắn còn lại là Cu, mCu = 10,5
– 0,1 x 65 = 4 gam.
C. Hoạt động luyện tập: 10’
- Mục tiêu:
- Nội dung:
- Sản phẩm:
- Cách tổ chức thực hiện:
Bài 1: Kim loại nào sau đây dẫn điện tốt nhất:
A. Cu
B. Al
C. Pb
D. Ba
Bài 2: Dãy kim loại phản ứng được với nước ở nhiệt độ thường
A. Na, Fe, K
B. Na, K, Li
C. Na, Li, Mg
D. Na, li, Fe
Bài 3: Trong các kim loại sau, kim loại nào hoạt động mạnh nhất:
A. Cu
B. Al
C. Pb
D. Ba
Bài 4: Các cặp sau cặp nào xảy ra phản ứng:
A. Cu + ZnCl2
B. Zn + CuCl2
C. Ca + ZnCl2
D. Zn + ZnCl2
Bài 5: Nhóm kim loại nào có thể tác dụng với nước ở nhiệt độ thường:
A. Cu, Ca, K, Ba
C. Ca, Mg, Li, Zn
B. Zn, Li, Na, Cu
D. K, Na, Ca, Ba
Bài 6: Dung dịch ZnCl2 lẫn tạp chất là CuCl2. Có thể dùng chất nào sau đây để
loại bỏ được CuCl2 khỏi dung dịch muối ZnCl2
A. Fe
B. Zn
C. AgNO3
D. NaOH
Bài 7: Kim loại nào dưới đây hoạt động mạnh nhất
A. Na
B. Fe
C. Al
D. Zn
Bài 8: Dãy nào dưới đây được sắp xếp theo thứ tự tăng dần mức độ hoạt động
hóa học
A. Na, Al, Cu, Zn
B. Cu, Al, Zn, Na
C. Na, Al, Zn, Cu
D. Cu, Zn, Al, Na
Bài 9: Trong các kim loại Cu, Na, Mg, Ni, Ag, Zn. Hai kim loại nào dẫn điện
tốt nhất:
A. Cu, Na
B. Zn, Ag
C. Mg, Ni
D. Cu, Ag
Bài 10: Các nhóm kim loại nào sau đây phản ứng với HCl sinh ra khí H2:
A. Fe, Cu, K, Ag, Al, Ba
B. Cu, Fe, Zn, Al, Mg, K
C. Mg, K, Fe, Al, Na
D. Zn, Cu, K, Mg, Ag, Al, Ba
Đáp án và hướng dẫn giải
1. A
2. B
3. D
4. B
5. D
6. B
7. A
8. D
9. D
10. C
D. Hoạt động vận dụng: 4’
- Mục tiêu:
- Nội dung:
- Sản phẩm:
- Cách tổ chức thực hiện:
GV: trong đời sống, người thường dùng dây bạc để đánh cảm vậy tại sao có thể
đánh cảm bằng dây bạc và khi đó dây bạc bị hoá đen? Để dây bạc trắng sáng trở
lại, người ta sẽ ngâm vào nước tiểu?
HS: Giải thích:
Khi bị bệnh cảm, trong cơ thể con người sẽ tích tụ một lượng khí H2S tương đối
cao. Chính lượng H2S sẽ làm cho cơ thể mệt mỏi.
Khi ta dùng Ag để đánh gió thì Ag sẽ tác dụng với khí H2S. Do đó, lượng H2S
trong cơ thể giảm và dần sẽ hết bệnh. Miếng Ag sau khi đánh gió sẽ có màu đen
xám:
4Ag + 2H2S + O2 → 2Ag2S↓(Đen) + 2H2O
-GV:
+Đánh giá nhận xét tinh thần thái độ của HS trong tiết học.
+Chốt lại kiến thức đã học.
+Yêu cầu hs về nhà về sơ đồ tư duy về chủ đề kim loại.
*Hướng dẫn học sinh học ở nhà và chuẩn bị cho bài sau
- Làm nốt bài tập trong SGK
- Soạn bài 18: “ Nhôm”
V. Rút kinh nghiệm:
................................................................................................................................
.................................................................................................................................
.................................................................................................................................
................................................................................................................................