đánh giá tình hình chẩn đoán và điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (3.48 MB, 167 trang )
<span class="text_page_counter">Trang 1</span><div class="page_container" data-page="1">
<b>BỘ GIÁO DỤC VÀ ĐÀO TẠO BỘ Y TẾ</b>
</div><span class="text_page_counter">Trang 2</span><div class="page_container" data-page="2"><b>BỘ GIÁO DỤC VÀ ĐÀO TẠO BỘ Y TẾ</b>
<b>THÀNH PHỐ HỒ CHÍ MINH, NĂM 2023</b>
</div><span class="text_page_counter">Trang 3</span><div class="page_container" data-page="3"><b>MỤC LỤC... i</b>
LỜI CAM ĐOAN ... i
DANH MỤC THUẬT NGỮ ANH -VIỆT ... ii
1.2. Giải phẫu và sinh lý tuyến tiền liệt ... 7
1.3. Diễn tiến ung thư tuyến tiền liệt và sinh lý bệnh kháng cắt tinh hoàn ... 9
1.4. Định nghĩa ung thư tuyến tiền liệt kháng cắt tinh hoàn ... 15
1.5. Chẩn đoán ung thư tuyến tiền liệt kháng cắt tinh hoàn ... 16
1.6. Điều trị ung thư tuyến tiền liệt kháng cắt tinh hồn... 31
1.7. Tình hình nghiên cứu ung thư tuyến tiền liệt kháng cắt tinh hoàn ... 39
<b>CHƯƠNG 2: ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU ... 43</b>
2.1. Đối tượng nghiên cứu ... 43
2.2. Phương pháp nghiên cứu ... 43
4.1. Đặc điểm chung mẫu nghiên cứu ... 84
4.2. Đặc điểm lâm sàng và điều trị hỗ trợ ... 90
</div><span class="text_page_counter">Trang 4</span><div class="page_container" data-page="4">4.4. Một số yếu tố liên quan đến thời gian sống còn ... 113
<b>KẾT LUẬN ... 124</b>
<b>KIẾN NGHỊ ... 126</b>
<b>TÀI LIỆU THAM KHẢO ... 128</b>
<b>PHỤ LỤC ... 146</b>
</div><span class="text_page_counter">Trang 5</span><div class="page_container" data-page="5">LỜI CAM ĐOAN
―Tôi xin cam đoan đây là cơng trình nghiên cứu khoa học của riêng tôi. Các sốliệu và kết quả trong luận văn là trung thực và chưa ai công bố trong bất kỳ một cơngtrình nghiên cứu nào‖
Thành phố Hồ Chí Minh, ngày 20 tháng 9 năm2023
Nguyễn Ngọc Đông
</div><span class="text_page_counter">Trang 6</span><div class="page_container" data-page="6">Tiếng Anh Viết tắt Tiếng Việt
American Joint Committee on
Androgen receptor targeted agents ARTA <sup>Tác nhân nhắm mục tiêu thụ thể</sup>androgen
phẩm Hoa Kỳ
Hormone sensitive Prostate cancer HSPC UTTTL nhạy cảm nội tiết
Hormon giải phóng hormon hồngthể
Metastatic Castration resistant
</div><span class="text_page_counter">Trang 7</span><div class="page_container" data-page="7">National Comprehensive Cancer
Mạng lưới ung thư toàn diện quốcgia Hoa Kỳ
Non metastatic Castration resistant
Prostate specific antigen doubling
Radiographic progression free
Thời gian sống không tiến triển trênXquang
Radiation Therapy Oncology Group- American Society for TherapeuticRadiation and Oncology
RTOG
-ASTRO <sup>Hội Xạ trị và Ung thư Hoa Kỳ</sup>
Union for International Cancer
</div><span class="text_page_counter">Trang 8</span><div class="page_container" data-page="8">DANH MỤC VIẾT TẮT
</div><span class="text_page_counter">Trang 9</span><div class="page_container" data-page="9">Bảng 1. 1. Nhóm nguy cơ tái phát sinh hóa UTTTL theo EAU 2017... 24
Bảng 1. 2. Nhóm nguy cơ UTTTL theo NCCN 2022 ... 25
Bảng 1. 3. Phân loại di căn theo CHAARTED và LATITUDE ... 26
Bảng 3. 1. Tuổi và phân bố theo nhóm tuổi ... 53
Bảng 3. 2. Bệnh mạn tính, thể trạng và tiền sử bệnh lý... 53
Bảng 3. 3. Chỉ số sinh hóa ... 55
Bảng 3. 4. Lý do vào viện tại Khoa Ung bướu ... 57
Bảng 3. 5. Lý do vào viện tại Khoa Ngoại Tiết niệu ... 58
Bảng 3. 6. Liên quan giữa triệu chứng đau xương và di căn xương ... 61
Bảng 3. 7. Tỉ lệ ISUP ... 62
Bảng 3. 8. Tỉ lệ nồng độ Testosterone ... 62
Bảng 3. 9. Tỉ lệ xét nghiệm PSA chẩn đoán ... 63
Bảng 3. 10. Tỉ lệ tăng PSA qua các lần xét nghiệm ... 63
Bảng 3. 11. Các trường hợp xét nghiệm PSA cao ... 64
Bảng 3. 12. Trung vị PSA tại các thời điểm ... 64
Bảng 3. 13. Thời gian diễn tiến PSA ... 65
Bảng 3. 14. Tỉ lệ đáp ứng PSA sau điều trị ... 66
Bảng 3. 15. Chẩn đốn hình ảnh thực hiện từng giai đoạn ở khoa Ung bướu ... 67
Bảng 3. 16. Giai đoạn TNM theo AJCC 2017 ... 68
Bảng 3. 17. Tỉ lệ bệnh di căn và không di căn ... 69
Bảng 3. 18. Tỉ lệ các di căn tạng ... 70
Bảng 3. 19. Tỉ lệ các di căn xương ... 71
Bảng 3. 20. Tỉ lệ các di căn hạch ... 72
Bảng 3. 21. Số lượng các di căn xương, hạch, tạng ... 73
Bảng 3. 22. Tỉ lệ điều trị ở từng giai đoạn ... 74
Bảng 3. 28. Thời gian sống còn theo nhóm điều trị ... 79
Bảng 3. 29. Tỉ lệ điều trị hỗ trợ ở các chuyên khoa ... 79
Bảng 4. 1. Tỉ lệ phổ biến của bệnh ... 84
Bảng 4. 2. Tuổi mắc UTTTL KCTH ở các nghiên cứu... 85
</div><span class="text_page_counter">Trang 10</span><div class="page_container" data-page="10">Bảng 4. 4. Tỉ lệ di căn ở các nghiên cứu ... 100
Bảng 4. 5. Tỉ lệ số lượng di căn mới khi tiến triển ... 103
Bảng 4. 6. Điều trị giai đoạn NNT ... 104
Bảng 4. 7. Tỉ lệ sống còn theo điều trị ở từng thời điểm ... 109
Bảng 4. 8. Thời gian sống cịn theo nhóm điều trị và loại di căn ... 110
Bảng 4. 9. Thời gian sống còn trong một số nghiên cứu ... 114
Bảng 4. 10. Thời gian sống còn theo điểm Gleason ... 120
Bảng 4. 11. Thời gian sống cịn theo nhóm di căn ... 124
</div><span class="text_page_counter">Trang 11</span><div class="page_container" data-page="11">Hình 1. 1. Mạch máu tuyến tiền liệt ... 7
Hình 1. 2. Giải phẫu vùng tuyến tiền liệt ... 8
Hình 1. 3. Diễn tiến của ung thư tuyến tiền liệt ... 9
Hình 1. 4. Cơ chế kháng các chất ức chế thụ thể androgen ... 13
Hình 1. 5. Hệ thống phân độ Gleason ... 23
Hình 1. 6. Các thử nghiệm lâm sàng theo diễn tiến tự nhiên ... 31
Hình 1. 7. Androgen điều khiển sự phát triển của UTTTL ... 32
Hình 4. 1. Thời gian phê duyệt thuốc cho UTTTL KCTH di căn ở Châu Âu và Nhật ... 105
</div><span class="text_page_counter">Trang 12</span><div class="page_container" data-page="12">Biểu đồ 3. 1. Triệu chứng lâm sàng ... 58
Biểu đồ 3. 2. Triệu chứng tiết niệu dưới ... 59
Biểu đồ 3. 3. Diễn tiến của triệu chứng đường tiết niệu dưới ... 59
Biểu đồ 3. 4. Các vị trí đau xương ... 60
Biểu đồ 3. 5. Diễn tiến của triệu chứng đau xương ... 60
Biểu đồ 3. 6. Diễn tiến các triệu chứng khác ... 61
Biểu đồ 3. 7. Diễn tiến trung vị PSA ... 65
Biểu đồ 3. 8. Tỉ lệ đáp ứng PSA ... 66
Biểu đồ 3. 9. Tỉ lệ bệnh di căn và không di căn ... 69
Biểu đồ 3. 10. Tỉ lệ các di căn ... 70
Biểu đồ 3. 11. Đường cong sống cịn tồn bộ ... 78
Biểu đồ 3. 12. Đường cong sống còn theo phác đồ điều trị ... 79
Biểu đồ 4. 1. Tỉ lệ mô bệnh học ... 88
Biểu đồ 4. 2. Tỉ lệ điểm Gleason ... 89
Biểu đồ 4. 3. Tỉ lệ các lý do nhập viện ... 91
Biểu đồ 4. 4. Tỉ lệ nồng độ Testosterone tại các thời điểm ... 94
Biểu đồ 4. 5. Diễn tiến Testosterone và PSA ... 96
Biểu đồ 4. 6. Diễn tiến trung vị của PSA ... 98
Biểu đồ 4. 7. Diễn tiến PSA và các nhóm triệu chứng ... 99
Biểu đồ 4. 8. Tỉ lệ các điều trị bước 1 ... 106
Biểu đồ 4. 9. Tỉ lệ các điều trị bước 2 ... 107
Biểu đồ 4. 10. Tỉ lệ các điều trị bước 3 ... 108
Biểu đồ 4. 11. Đường cong sống cịn theo nhóm điều trị ... 110
Biểu đồ 4. 12. Đường cong sống cịn theo nhóm điều trị và loại di căn ... 112
Biểu đồ 4. 13. Đường cong sống cịn theo nhóm tuổi ... 116
Biểu đồ 4. 14. Đường cịn sống cịn theo nhóm Gleason ... 121
Biểu đồ 4. 15. Đường cong sống cịn theo nhóm di căn... 124
</div><span class="text_page_counter">Trang 13</span><div class="page_container" data-page="13"><b>ĐẶT VẤN ĐỀ</b>
Ung thư tuyến tiền liệt là một trong các bệnh ung thư hay gặp ở nam giới đặcbiệt tại các nước phát triển, đứng hàng thứ 2 sau ung thư phổi, là vấn đề sức khỏe quantrọng trên phạm vi toàn cầu làm giảm chất lượng sống của bệnh nhân và tăng gánhnặng y tế. Theo thống kê của GLOBOCAN 2020, trên thế giới có 1.414.259 trườnghợp mắc mới với tỉ suất 30,7/100.000 và 375.304 trường hợp tử vong do ung thư tuyếntiền liệt với tỉ suất 7,7/100.000, tại Việt Nam có 6.248 trường hợp mắc mới trong năm2020 với tỉ suất 12,1/100.000 và số trường hợp tử vong là 2.628 với tỉ suất5,1/100.000.<sup>1,2</sup>
Ung thư tuyến tiền liệt là bệnh phụ thuộc nội tiết, trong lịch sử tự nhiên củabệnh, giai đoạn đầu ung thư tuyến tiền liệt nhạy cảm với điều trị nội tiết. Năm 1941Huggins và Hodges cho thấy mối liên hệ của nội tiết tố androgen với sự phát triển khốiu tuyến tiền liệt, liệu pháp loại bỏ androgen đã trở thành phương pháp điều trị quantrọng trong đơn trị liệu hoặc kết hợp với các phương pháp khác ở các giai đoạn. Đápứng ban đầu với liệu pháp loại bỏ androgen khá thuận lợi, cải thiện lâm sàng và sinhhóa được đánh giá bằng sự giảm nồng độ PSA 80 - 90% bệnh nhân ở giai đoạn bệnh dicăn,<small>3-6</small>
nhưng tình trạng kháng nội tiết sẽ xảy ra dẫn đến kháng với điều trị nội tiết gọilà kháng cắt tinh hoàn,<sup>7</sup> ung thư tuyến tiền liệt kháng cắt tinh hoàn là nguyên nhânhàng đầu gây tử vong liên quan đến ung thư tuyến tiền liệt, đến 30.000 người hàng nămở Mỹ và 375.000 người hàng năm trên tồn thế giới.<small>1,8</small>
Có 10 đến 20% bệnh nhân ung thư tuyến tiền liệt tiến triển kháng với liệu phápnội tiết sau 18 đến 22 tháng điều trị nội tiết,<sup>4,9</sup> và 15 - 33% bệnh nhân ung thư tuyếntiền liệt kháng cắt tinh hoàn chưa di căn sẽ phát triển di căn trong 2 năm, 84% có di cănxương khi được chẩn đốn…. Con đường thụ thể androgen đóng vai trò cơ bản trongsự tiến triển của bệnh, tiên lượng bệnh sẽ xấu hơn và phải thay đổi liệu pháp điều trị.<small>10-12</small> Sự đáp ứng với điều trị, chất lượng cuộc sống và thời gian sống còn của bệnh nhân
</div><span class="text_page_counter">Trang 14</span><div class="page_container" data-page="14">ung thư tuyến tiền liệt kháng cắt tinh hồn khơng giống nhau giữa các cá thể. Vì vậytìm hiểu đặc điểm lâm sàng, các yếu tố tác động đến hiệu quả điều trị và thời gian sốngcòn của người bệnh ở giai đoạn này là cần thiết. Đối với bệnh nhân ung thư tuyến tiềnliệt kháng cắt tinh hoàn di căn, các lựa chọn điều trị còn hạn chế và thiếu sự đồng thuậntrong hướng dẫn điều trị của các quốc gia.<small>13</small>
Y văn đã có nhiều cơng trình nghiên cứu ung thư tuyến tiền liệt kháng cắt tinhhoàn như là cơ chế bệnh sinh, triệu chứng lâm sàng, cơ chế kháng nội tiết… nhiều yếutố tiên lượng về khả năng sống còn cũng như các biến số liên quan đến hiệu quả điềutrị đã được xác định để tối ưu hóa điều trị cho bệnh nhân, tuy vậy thời gian sống cònvẫn thấp chỉ từ 9 đến 30 tháng,<sup>10</sup> chất lượng sống chưa cao dù đã có nhiều tiến bộ.<sup>14</sup>
Gần đây, chiến lược điều trị cho bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hồnđã có nhiều thay đổi do hiểu biết nhiều hơn về sinh học phân tử trong cơ chế tiến triểncủa ung thư tuyến tiền liệt, các định nghĩa về bệnh cũng đã được thống nhất.<sup>15</sup> Một sốloại thuốc mới là kết quả của các thử nghiệm ngẫu nhiên giai đoạn III,<sup>16-22</sup> có thể tăng tỉlệ sống còn tổng thể đã được giới thiệu trong thực hành lâm sàng hàng ngày, để quản lýbệnh nhân ung thư tuyến tiền liệt kháng cắt tinh chưa di căn và di căn.
Tại Việt Nam, điều trị ung thư tuyến tiền liệt đã có từ nhiều thập kỷ trướcnhưng chưa có nhiều nghiên cứu về đặc điểm lâm sàng cũng như nghiên cứu về điều trịtrên bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hoàn; Do sự phát triển của cácphiên bản điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn, các bác sĩ lâm sàng hiệnđang phải đối mặt với những thách thức điều trị, chính là lựa chọn thuốc và trình tựđiều trị thích hợp cho từng bệnh nhân cụ thể, các yếu tố tác động đến chẩn đoán đếnkết quả điều trị, cũng như thời gian sống cịn của người bệnh. Vì vậy chúng tôi thực
<b>hiện đề tài này để trả lời câu hỏi: ―Tình hình chẩn đốn và điều trị ung thƣ tuyếntiền liệt kháng cắt tinh hoàn nhƣ thế nào?‖ Và chọn Bệnh viện Bình Dân và Bệnh</b>
viện Chợ Rẫy là hai trung tâm niệu khoa lớn để hoàn thành nghiên cứu với mục tiêu:
</div><span class="text_page_counter">Trang 15</span><div class="page_container" data-page="15"><b>MỤC TIÊU NGHIÊN CỨU TỔNG QT</b>
Đánh giá tình hình chẩn đốn và điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn
<b>MỤC TIÊU NGHIÊN CỨU CỤ THỂ</b>
1. Xác định đặc điểm lâm sàng và cận lâm sàng ở bệnh nhân ung thư tuyến tiền liệtkháng cắt tinh hoàn.
2. Xác định đặc điểm điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn tại thờiđiểm nghiên cứu.
3. Đánh giá kết quả điều trị ban đầu ở bệnh nhân ung thư tuyến tiền liệt kháng cắttinh hoàn tại thời điểm nghiên cứu.
</div><span class="text_page_counter">Trang 16</span><div class="page_container" data-page="16"><b>CHƯƠNG 1: TỔNG QUAN TÀI LIỆU</b>
1.1. Dịch tể học
1.1.1. Tỉ lệ bệnh
UTTTL là một trong những bệnh ung thư có tỉ lệ cao trên thế giới. Theo thốngkê của GLOBOCAN 2020, trên thế giới có 1.414.259 trường hợp mắc mới, với tỉ suất30,7/100.000 chiếm khoảng 7,3% tổng số trường hợp mắc ung thư ở cả nam và nữ. Vớitỉ lệ này, UTTTL đứng thứ 4 trong số các ung thư phổ biến nhất, sau ung thư vú, phổi,trực tràng.<sup>1,23</sup> Ở nam giới, UTTTL chiếm khoảng 14,1% tổng số ca ung thư và đứngthứ 2 sau ung thư phổi. Tỉ lệ mắc UTTTL có sự khác biệt giữa các khu vực trên thếgiới và giữa các chủng tộc có thể do nhiều yếu tố. Để giải thích cho sự khác biệt này,ngồi việc sàng lọc sớm bằng xét nghiệm PSA, các yếu tố như chủng tộc, thói quen ănuống và lối sống cũng có nghĩa quan trọng. Các tác giả Obinata và cộng sự <sup>24</sup> đã báocáo rằng người Pháp gốc Châu Phi có nguy cơ mắc UTTTL cao hơn người Pháp gốcChâu Á dù họ cùng sống ở quần đảo Guadeloupe. Chế độ ăn ở các nước phương tâyđược cho là có thể làm tăng nguy cơ mắc UTTTL,<small>25</small>
một nghiên cứu khác cũng chothấy rằng tỉ lệ mắc UTTTL ở người Việt Nam di cư sang Mỹ cao hơn nhiều lần so vớingười Việt Nam sống tại Hà Nội.<small>26</small>
Sự khác biệt cũng được ghi nhận giữa người Nhậtsống ở Mỹ và người Nhật sống tại nước Nhật.<sup>27,28</sup>
Tại Việt Nam, tỉ lệ mắc UTTTL ngày càng tăng, thống kê của GLOBOCAN2012, UTTTL đứng hàng thứ 11 về tỉ suất mắc mới ung thư ở nam giới. Tuy nhiên,theo số liệu GLOBOCAN 2020, ung thư này đứng hàng thứ 4.<sup>1,23</sup>
UTTTL KCTH được xem như là thất bại của việc điều trị UTTTL bằng ngănchặn sự ni dưỡng khối u bởi Testosteron trong tuần hồn, có liên quan đến tình trạngUTTTL trở nên xấu hơn.<sup>29</sup>
Năm 2011, Kirby và cộng sự đã nghiên cứu đánh giá có hệ thống về 12 nghiên
</div><span class="text_page_counter">Trang 17</span><div class="page_container" data-page="17">nghĩa không đồng nhất, bốn trong số năm nghiên cứu về tỉ lệ hiện mắc cho thấy 10 20% bệnh nhân UTTTL sẽ phát triển thành UTTTL KCTH trong khoảng 5 năm theodõi. Tại Mỹ, tỉ lệ hàng năm của UTTTL KCTH khơng di căn ước tính khoảng 60.000nam giới vào năm 2020, với tỉ lệ tiến triển di căn là 34% và tỉ lệ tử vong chung hàngnăm là 16%.<small>10,29</small>
-Theo Alemayehu và cộng sự, từ cơ sở dữ liệu y tế của Mỹ trong khoảng 6 nămcó 15.361 bệnh nhân (từ 40 tuổi trở lên) đã được chẩn đoán UTTTL điều trị bằng nộitiết có 2740 bệnh nhân UTTTL KCTH cho thấy mức độ phổ biến là 17,8%.<sup>30</sup> Nghiêncứu lớn nhất về UTTTL KCTH được MarketScan thực hiện trên 44.791 bệnh nhânUTTTL có 4266 (9,5%) đã phát triển thành UTTTL KCTH (trung bình theo dõikhoảng 2,1 năm cho mỗi bệnh nhân).<sup>29,31</sup> Nghiên cứu tương tự được thực hiện tại Anh,trong khoảng thời gian 5 năm với 8678 bệnh nhân ở độ tuổi 40 trở lên được chẩn đoánmắc bệnh UTTTL, trong số này 969 UTTTL KCTH chiếm tỉ lệ 11,2%.<sup>32</sup> Một nghiêncứu ở Ý trên 211 bệnh nhân UTTTL trong 55 tháng sau khi chẩn đốn, 53% bệnh nhân(trung bình 70 tuổi) có UTTTL KCTH.<sup>33</sup> Nghiên cứu do Bianco và cộng sự khảo sát1045 bệnh nhân UTTTL đã phẫu thuật cắt tuyến tiền liệt tận gốc, các tác giả báo cáorằng 19% bệnh nhân phát triển UTTTL KCTH trong thời gian theo dõi trung bình 55tháng.<sup>34</sup>
1.1.2. Tỉ lệ tử vong
Đã có nhiều tiến bộ trong điều trị và chăm sóc y tế, UTTTL vẫn là một trongnhưng nguyên nhân tử vong hàng đầu do ung thư ở nam giới, chiếm 6,7% tổng số tửvong do ung thư. Khác với tỉ suất mắc, tỉ suất tử vong do UTTTL không khác biệtnhiều giữa các quốc gia và khu vực trên thế giới, tỉ suất này dao động từ 5,2 ở các nướccó thu nhập trung bình thấp đến 13,1/100.000 ở các nước có thu nhập thấp, các nước cóthu nhập cao tỉ suất này là 8,6/100.000.<sup>23</sup> Sự khác biệt này có thể liên quan đến các yếutố di truyền hoặc do chất lượng chăm sóc và điều trị ở các nước phát triển tốt hơn cácnước đang phát triển.<small>35</small>
</div><span class="text_page_counter">Trang 18</span><div class="page_container" data-page="18">Bashar Matti và cộng sự phân tích 42.563 nam giới, từ 40 tuổi trở lên, đượcchẩn đoán mắc bệnh UTTTL từ năm 2000 đến năm 2016, sau 15 năm theo dõi xác suấtsống sót tích lũy chung lần lượt là 39,8%, 43,6%, 63,3% và 46,5% đối với nam giớiMaori, Thái Bình Dương, Châu Á và Châu Âu theo thứ tự tương tự, tỉ lệ sống sót doung thư cụ thể là 62,7%, 64,3%, 79,8% và 72,0%.<small>36</small>
Tuy nhiên khi bệnh nhân ở giai đoạn UTTTL KCTH thời gian sống còn đượcbáo cáo trong năm nghiên cứu tại Mỹ, Ý, Nhật, Canada, Hà Lan<small>11,37-40</small> chỉ còn 9 đến 30tháng, không đồng nhất giữa các nghiên cứu. Sự xuất hiện các triệu chứng di căn làmgiảm chất lượng sống, thời gian sống cịn ước tính khoảng 14 tháng được rút ra từnhững nhiên cứu này.<sup>10</sup>
Trong lịch sử diễn tiến của bệnh UTTTL, thời gian sống cịn tồn bộ củaUTTTL KCTH không di căn là 5 năm<sup>41</sup> và UTTTL KCTH di căn là dưới 2 năm.<sup>42,43</sup>1.1.3. Tuổi và nguy cơ UTTTL
Ba yếu tố tuổi, tiền sử gia đình và người gốc Châu Phi là yếu tố nguy cơ củaUTTTL đã được báo cáo.<sup>24,44</sup>
Tuổi là yếu tố nguy cơ quan trọng nhất của UTTTL. Rất ít nam giới dưới 40 tuổiđược chẩn đoán mắc UTTTL, từ 50 tuổi trở lên, nguy cơ mắc ung thư này tăng nhanh.Tỉ lệ này ở nhóm tuổi 45 - 54 là 10,6/100.000, nhưng ở nhóm tuổi 55 - 64 là72,9/100.000.<sup>16</sup> Tại Úc, 85% số trường hợp mắc ung thư có độ tuổi trên 65, và đến độtuổi 85, 25% nam giới Úc có nguy cơ được chẩn đốn mắc UTTTL.<sup>45</sup> Khi tuổi cao hơn,nồng độ PSA trong huyết thanh cao hơn, bệnh nhân cũng được chẩn đoán bệnh ở giaiđoạn muộn hơn.
Tuổi được chẩn đoán ban đầu ảnh hưởng đến kết quả của những bệnh nhân sauđó phát triển UTTTL KCTH với nguy cơ phân bố hai chiều, với tỉ lệ sống cịn ngắnnhất ở các nhóm >75 tuổivà < 55 tuổi.<sup>14,46</sup>
Người mang các gen: BRCA<small>1-2</small>, ATM, PALB<sub>2</sub>, CHEK<sub>1-2</sub> và HOXB13 .... được
</div><span class="text_page_counter">Trang 19</span><div class="page_container" data-page="19">1.2. Giải phẫu và sinh lý tuyến tiền liệt
Tuyến tiền liệt là cơ quan được cấu tạo bởi 3 thành phần: tuyến, cơ và sợi; nằmsâu trong khung chậu nam, hình tháp tứ giác, đỉnh ở dưới, đáy ở trên, ngay dưới cổbàng quang. Mặt sau hướng xuống dưới và ra trước, lồi, có rãnh giữa ngăn cách hai
thùy bên, ngăn cách phía sau với trực tràng bởi lớp cân Denonvilliers.
<i>(Nguồn: www.emedicine.com (2009), Transurethral resection of the prostate,</i>
eMedicine Specialties, Clinical Procedures)<sup>48</sup>
Tuyến tiền liệt là tuyến nội ngoại tiết: ngoại tiết tiết ra tinh dịch đổ vào niệu đạoở rãnh hai bên ụ núi, nội tiết tiết ra kháng nguyên đặc hiệu của tuyến tiền liệt. Tuyếntiền liệt ở người trưởng thành nặng khoảng 15 - 20g, kích thước khoảng 40x30x25mm.<sup>49</sup>
Tuyến tiền liệt được bao bọc bởi một lớp vỏ mỏng, chứa một phần niệu đạo saudài khoảng 2,5cm. Niệu đạo tuyến tiền liệt có một đoạn dãn gọi là xoang tuyến tiềnliệt, thành sau có một chỗ lồi ở giữa gọi là ụ núi. Ống phóng tinh xuyên qua tuyến tiềnliệt từ mặt sau, đi chếch lên đổ vào ụ núi gần cơ thắt vân niệu đạo.<sup>49</sup>
Hình 1. 1. Mạch máu tuyến tiền liệt
</div><span class="text_page_counter">Trang 20</span><div class="page_container" data-page="20">Máu cung cấp cho tuyến tiền liệt xuất phát từ động mạch bàng quang dưới vàđộng mạch trực tràng giữa. Máu tĩnh mạch được dẫn lưu qua đám rối tĩnh mạch quanhtuyến tiền liệt và sau đó kết hợp với tĩnh mạch lưng sâu dương vật và tĩnh mạch hạ vị.Thần kinh chi phối cho tuyến tiền liệt xuất phát từ đám rối thần kinh giao cảm và phógiao cảm. Hệ thống bạch mạch của tuyến tiền liệt dẫn về qua các hạch chậu ngoài, hạchbàng quang, hạch cùng và hạch hạ vị.<sup>49</sup>
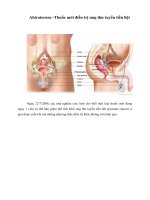
Hình 1. 2. Giải phẫu vùng tuyến tiền liệt
<i><small>Transition zone: vùng chuyển tiếp, Central zone: vùng trung tâm,</small></i>
<i><b><small>Anterior zone: vùng trước, Pheripheral zone: vùng ngoại vi</small></b></i>
<i>(Nguồn: PD. Grimm (2004),"The foundation", The prostate cancer treatment book,McGraw Hill, p. 60-3)<sup>50</sup></i>
Theo Grimm tuyến tiền liệt được chia thành 4 vùng khác nhau:
Vùng ngoại vi nằm phía sau tuyến tiền liệt, liên hệ chặt chẽ với trực tràng, đượctạo thành chủ yếu là mô tuyến, khoảng 70%, là nơi xuất phát của khoảng 70% cáctrường hợp carcinoma tuyến tiền liệt.
Vùng chuyển tiếp nằm trong cùng, bao quanh niệu đạo, chiếm khoảng 5% mô
</div><span class="text_page_counter">Trang 21</span><div class="page_container" data-page="21">Vùng trung tâm là phần trên gần bàng quang, có khoảng một phần ba là môtuyến, tiết ra tinh dịch. Cũng như vùng chuyển tiếp, sau 40 tuổi, vùng này phát triểnlớn dần. Vùng này xuất phát của khoảng 10% các trường hợp carcinoma tuyến tiền liệt.Vùng trước tuyến tiền liệt chủ yếu là mô cơ, carcinoma tuyến tiền liệt ít xảy ra tạiđây.<small>50</small>
1.3. Diễn tiến ung thư tuyến tiền liệt và sinh lý bệnh kháng cắt tinh hồn
Hình 1. 3. Diễn tiến của ung thư tuyến tiền liệt
<i><small>ADT: Liệu pháp triệt androgen, Localised or locally advanced prostate cancer: UTTTL khu trú, tiến triển tạichỗ, Definitive Therapy: điều trị triệt căn, Biochemical recurrence: tái phát sinh hóa, CRPC: UTTTL KCTH,nonmetastatic: không di căn, Termianl disease: bệnh giai đoạn cuối</small></i>
<i>(Nguồn: Scher HI, et al. J Clin Oncol. 2016;34:1402-18.</i>
<i>Available from: Accessed April 2018)<sup>51</sup></i>
<i>Ung thư tuyến tiền liệt sớm</i>
UTTTL có thể được phát hiện sớm khi PSA tăng cao trong thời gian tầm sốt, vìbệnh nhân thường khơng có triệu chứng. Trong trường hợp này, bệnh ở giai đoạn sớm
</div><span class="text_page_counter">Trang 22</span><div class="page_container" data-page="22">(T<sub>1-2a</sub>N<sub>0</sub>M<sub>0</sub> và mức PSA dưới 10 ng/mL) hoặc bệnh khu trú (T<sub>2a</sub> và, hoặc mức PSA hơn10 ng/mL) sẽ được điều trị bằng liệu pháp triệt căn.<sup>12</sup>
Những bệnh nhân được đánh giá là có nguy cơ thấp hoặc rất thấp (PSA <10ng/mL, điểm Gleason <6 và T<sub>1-2a</sub>) có thể được điều trị bằng phẫu thuật hoặc xạ trịngoài.<sup>52,53</sup> Phẫu thuật được ưu tiên ở những bệnh nhân có nguy cơ thấp rất thấp, trongkhi xạ trị là lựa chọn ưu tiên cho những bệnh nhân cân nhắc có nguy cơ tái phát trungbình (PSA từ 10 - 20 ng/mL, T<sub>2b-2c </sub>và điểm Gleason 7). Ở nhóm bệnh nhân thứ hai,ADT bổ trợ có thể được sử dụng trong thời gian tối đa là 6 tháng,<sup>54,55</sup> ―cắt tinh hoàn‖bằng các chất tương tự LHRH hoặc Bicalutamide hoặc cả hai. Các đặc điểm của bệnhbiểu hiện xấu hơn được xếp vào nhóm nguy cơ cao là giai đoạn lâm sàng lớn hơn T<sub>2b</sub>,điểm Gleason hơn 7 và PSA hơn 20 ng/dL, nhóm này có tỉ lệ tái phát sinh hóa là 32% -70% trong vòng 5 năm kể từ khi điều trị.<small>12</small>
Sau khi điều trị bệnh tái phát có thể xảy ra những người được điều trị bằng phẫuthuật hoặc xạ trị đơn thuần, có thể cịn nhạy với điều trị nội tiết, bởi vì độ nhạy cảm củahọ với ADT vẫn chưa được biết đến. Một số bệnh nhân có nguy cơ tái phát trung bình,trước đây đã trải qua ADT bổ trợ trong giai đoạn đầu của bệnh sử độ nhạy của họ vớiADT có thể thấp. Một nhóm bệnh nhân khác được chẩn đoán mắc bệnh nguy cơ caođược coi là bệnh tiến triển vùng.<small>12</small>
UTTTL có nguy cơ tái phát cao có ít nhất một trong các đặc điểm sau: T<sub>3</sub> trởlên, điểm Gleason hơn 7 và mức PSA hơn 20 ng/mL. Đối với những bệnh nhân này,không nên phẫu thuật và phải lựa chọn phương pháp xạ trị. ADT bổ trợ đáp ứng sẽ kéodài khoảng 24 tháng.<sup>56,57</sup>
Xạ trị sau phẫu thuật được sử dụng khi có một hoặc nhiều yếu tố nguy cơ (bệnhpT<sub>3</sub> và cắt bỏ biên trong phẫu thuật).<sup>58</sup> Ngoài sau phẫu thuật phát hiện các hạch di căn,ADT bổ trợ điều trị trong khoảng 24 tháng.<sup>59,60</sup>
Chẩn đoán bệnh tái phát khi tăng PSA cao, vì ở giai đoạn này bệnh nhân khơng
</div><span class="text_page_counter">Trang 23</span><div class="page_container" data-page="23">Tái phát sinh hóa có thể được xác định khi nồng độ PSA hơn 0,4 ng/mL ở những bệnhnhân đã phẫu thuật cắt tuyến tiền liệt tận gốc. Bệnh nhân điều trị bảo tồn như xạ trị,mức PSA phải vượt quá PSA nadir ít nhất 2 ng/mL.<sup>62,63</sup>
<i>Ung thư tuyến tiền liệt chưa di căn</i>
Những bệnh nhân nói trên, có mức PSA tăng nhưng khơng có bằng chứng lâm sàngvề ung thư, điều trị liên quan đến vai trò của ADT. Dữ liệu y văn ủng hộ ADT sớm,thay vì chậm, mặc dù một số bệnh nhân chỉ tái phát sinh hóa sẽ khơng chết vì UTTTL,giải pháp thay thế tốt có thể là theo dõi cho đến khi ung thư tiến triển.<sup>64</sup> Những bệnhnhân có lợi với ADT như những bệnh nhân được chẩn đoán với giá trị PSA cao, nhữngngười có thời gian tăng gấp đơi PSA ngắn (dưới 6 tháng), đặc biệt nếu họ có tuổi thọcao, nên nhận ADT sớm.<sup>65-67</sup>
ADT bằng phương pháp cắt bỏ tinh hoàn hoặc bằng các chất tương tự LHRH,kháng androgens (Bicalutamide), hoặc chất đối kháng GnRH (Degarelix). ADT thườngsử dụng các chất đồng vận LHRH, có thể được sử dụng riêng hoặc kết hợp với cáckháng androgen không steroid như Bicalutamidde.<small>68-70</small>
Điều thú vị là chỉ CAB dựa trênBicalutamide mới cải thiện khả năng sống cịn đã nói trên, vì vậy các kháng nguyênkhác như cyproterone và ketoconazole không được sử dụng trong thực hành lâmsàng.<sup>71</sup>
Tuy nhiên, tác dụng phụ của ADT có thể làm giảm chất lượng cuộc sống của bệnhnhân. Do đó, sử dụng ADT khơng liên tục có thể làm giảm độc tính và có thể làm chậmsự xuất hiện của sự phát triển khối u độc lập với androgen.<sup>72-74</sup>
<i>Ung thư tuyến tiền liệt di căn</i>
Bệnh nhân M<sub>0</sub> tiến triển di căn có thể phát hiện được. Trong giai đoạn này,bệnh vẫn nhạy cảm với ADT trong một thời gian dài nhưng ở giai đoạn cuối bệnh trởnên kháng. UTTTL di căn được cấu tạo bởi các dòng tế bào khối u nhạy cảm với ADThoặc không nhạy cảm với ADT và tỉ lệ phần trăm của những tế bào này tăng lên khi
</div><span class="text_page_counter">Trang 24</span><div class="page_container" data-page="24">tăng gánh nặng khối u và thời gian dùng ADT. Đáp ứng tốt ban đầu với ADT trongUTTTL di căn có thể phản ánh việc loại bỏ các dịng khơng nhạy với ADT.<sup>12</sup>
Trong giai đoạn này phải phân biệt giữa ung thư chỉ lan đến một hoặc một vài vịtrí trong cơ thể (Oligometastatic) là bệnh được đánh giá có kết quả tốt hơn với tổng sốdi căn nhỏ hơn hoặc bằng ba (chỉ xương hoặc hạch bạch huyết) và bệnh ung thư di cănkhối lượng lớn. Đối với những trường hợp này, ADT có thể được kết hợp với các liệupháp điều trị theo vùng như xạ trị giảm nhẹ trên các tổn thương có triệu chứng và liệupháp nhắm mục tiêu tế bào xương như axit Zoledronic và Denosumab.<sup>75,76</sup>
Bệnh di căn khối lượng lớn được định nghĩa là một khối u có biểu hiện di căntạng và hoặc từ bốn tổn thương xương trở lên, trong đó ít nhất một tổn thương ở xươngchậu hoặc ở cột sống.<sup>77</sup> Hai thử nghiệm lâm sàng GETUG15 và CHARTEED đã thửnghiệm việc bổ sung Docetaxel vào ADT tiêu chuẩn ở UTTTL di căn khối lượng lớn.Kết quả là, phối hợp Docetaxel và ADT kéo dài thời gian điều trị có nghĩa nếu sosánh với ADT đơn thuần.<sup>78-80</sup> Dữ liệu thu được từ hai thử nghiệm này chứng tỏ sự thayđổi nhanh chóng tiêu chuẩn của liệu pháp, mang lại vai trò quan trọng của hóa trị sớmđối với thể bệnh di căn khối lượng lớn.
<i>Ung thư tuyến tiền liệt kháng cắt tinh hoàn</i>
Mặc dù tỉ lệ đáp ứng ban đầu sau khi ADT tăng lên 80 - 90%, nhưng tình trạngmất hiệu lực luôn xảy ra dẫn đến sự phát triển của bệnh UTTTL xấu hơn được gọi làUTTTL KCTH biểu hiện bằng sự gia tăng liên tục của các giá trị PSA và mứcTestosterone dưới 50 ng/dL, ba lần tăng liên tiếp PSA cách nhau một tuần, dẫn đến hailần tăng 50% so với nadir, với PSA hơn 2 ng/mL.<sup>80</sup> Từ UTTTL KCTH không di cănphát triển thành UTTTL KCTH di căn trung bình của quá trình chuyển đổi này từ khibắt đầu ADT là 19 tháng. Cho đến gần đây, chỉ có hóa trị là lựa chọn lâm sàng chínhvà Docetaxel là tác nhân cho thấy lợi thế về khả năng sống còn, nếu so sánh với thuốchỗ trợ khác.<sup>81</sup>
</div><span class="text_page_counter">Trang 25</span><div class="page_container" data-page="25">Sự phát triển của UTTTL luôn phụ thuộc vào sự kích thích của thụ thểandrogen, nhưng trong UTTTL KCTH nội tiết tố androgen trong tuần hồn khơng cịnkhả năng ni khối u. Trong một thời gian dài, người ta đã đưa ra giả thuyết rằng sựphát triển của khối u trong UTTTL KCTH không phụ thuộc vào sự kích thích của thụthể androgen, nhưng quan niệm này đã bị bác bỏ và việc truyền tín hiệu thơng qua thụthể androgen được cho là rất quan trọng đối với sự phát triển của khối u, cả trong điềukiện thiếu androgen. Do đó sự kích hoạt lại thụ thể androgen được xác định là mộtđộng lực quan trọng của hiện tượng kháng ADT.<small>82</small>
Hình 1. 4. Cơ chế kháng các chất ức chế thụ thể androgen
<i><small>AR: thụ thể androgen, ARPI: thuốc ức chế AR, AR-V: biến thể mối nối AR, GR: thụ thể Glucocorticoid, PR: thụthể Progesteron, Persitent androgen/AR signaling: tín hiệu androgen/AR liên tục, AR bypass pathways: khôngqua thụ thể androgen, Androgen/AR independent mechanisms: cơ chế độc lập androgen/AR</small></i>
</div><span class="text_page_counter">Trang 26</span><div class="page_container" data-page="26"><i>(Nguồn:Novel Insights into Molecular Indicators of Response and Resistance toModern Androgen-Axis Therapies in Prostate Cancer. Curr Urol Rep. Apr 2016)<sup>83</sup></i>
Trên thực tế, nhiều nghiên cứu đã chứng minh nồng độ Testosterone ở khối utrong UTTTL KCTH được phục hồi về mức tương đương hoặc thậm chí cao hơn sovới những người không bị cắt tinh hoàn<sup>84,85</sup> và việc mất phản ứng với ADT có liênquan đến cơ chế bù trừ sau kích hoạt thụ thể androgen. Những thay đổi di truyền xảy ratrong các tế bào khối u làm cho chúng có thể tạo ra các nội tiết tố androgen một cáchđộc lập hoặc các tế bào trở nên nhạy cảm hơn với nội tiết androgen và hoặc bắt đầu bịkích thích bởi các steroid không phải là nội tiết tố androgen, như glucocorticoids.<sup>86</sup>Trong tình huống này, ADT khơng cịn hiệu quả nữa và cần có các chiến lược khác canthiệp vào các cơ chế trên.<sup>12</sup>
Trong số các cơ chế gây ra phản ứng ―kháng cắt tinh hồn‖, có các đột biến thụthể androgen, được mô tả trong 10-30% UTTTL KCTH, bị kích hoạt mạnh bởi nội tiếttố tuyến thượng thận, các hormon steroid khác và các kháng androgens nhưBicalutamide, việc lựa chọn liệu pháp phụ thuộc vào đột biến AR, trong đó các khối uthối triển sau khi dừng kháng androgens.<sup>87-90</sup>
Một đột biến khác tạo ra biến thể mối nối thụ thể (ARV), là những biến thể genmã hóa cho các thụ thể bị thay đổi, thiếu miền liên kết androgen nhưng vẫn duy trì vịtrí liên kết DNA, dẫn đến kích hoạt thụ thể ngay cả khi khơng có androgen.<sup>91-93</sup>Hornberg và cộng sự<sup>94</sup> đã chứng minh mức độ biểu hiện ARV cao hơn trong di cănxương ở UTTTL KCTH so với di căn xương trong UTTTL nhạy cảm với hormone, vàbiểu hiện ARV có liên quan đến tiên lượng kém hơn. Đặc biệt, việc loại bỏ trong ốngnghiệm của biến thể mối nối thụ thể androgen AR-V7 đã lưu giữ lại khả năng đáp ứngvới kháng androgen, khiến đây trở thành mục tiêu quan trọng cho các liệu pháp điều trịtrong tương lai.<small>47,95</small>
Khoảng 25% số ca tiến triển sau ADT có khuếch đại gen thụ thểandrogen và tăng ái lực với dihydroTestosterone.<small>84,85</small>
</div><span class="text_page_counter">Trang 27</span><div class="page_container" data-page="27">thuộc androgen, có thể là do những thay đổi tế bào thích nghi cho phép tế bào UTTTLsống sót trong mơi trường androgen thấp. Vì vậy phương pháp tiếp cận lâm sàng tối ưucó thể bao gồm việc triệt tiêu tồn bộ mơi trường vi mơ androgen ở tuyến tiền liệt bằngcác tác nhân mới làm mờ trục tín hiệu androgen.<sup>44,47</sup>
Gần đây thế hệ nội tiết tố mới đã được phát triển và phê duyệt, hai trong số cáctác nhân này là Abiraterone và Enzalutamide, có thể được sử dụng sau ADT thất bại, vìchúng hoạt động như chất ức chế tín hiệu AR (Enzalutamide) và ức chế tạo steroidCYP17A1 (Abiraterone).<sup>12</sup>
Giai đoạn cuối của lịch sử tự nhiên UTTTL được biểu hiện bằng sự phát triển củabệnh rất mạnh các tế bào nhân bản không hoặc đáp ứng với điều trị hormone. Bệnhnhân trong giai đoạn này thường được điều trị bằng một hoặc nhiều dịng hóa trị.
Giai đoạn này, 90% bệnh nhân UTTTL KCTH có bằng chứng xquang di cănxương là nguyên nhân chính gây giảm chất lượng cuộc sống và tử vong. Các triệuchứng liên quan đến di căn xương có thể được quản lý bằng liệu pháp nhắm mục tiêu tếbào hủy xương dựa trên Denosumab và axit Zoledronic; liên quan đến đau cũng có thểđược điều trị bằng xạ trị.<small>96</small>
1.4. Định nghĩa ung thư tuyến tiền liệt kháng cắt tinh hoàn
Năm 1999, PCWG1 đã đưa ra các khuyến nghị để chuẩn hóa kết quả PSA trongcác thử nghiệm UTTTL KCTH giai đoạn II.<small>97</small>
Thuật ngữ UTTTL KCTH do PCWG2 đề xuất vào năm 2008 để mơ tả diễn tiếnlâm sàng và, hoặc sinh hóa trong môi trường thiếu Testosterone.<small>98</small> Tiến triển lâm sàngcủa khối u đặc dựa trên tiêu chuẩn đánh giá đáp ứng trong khối u rắn (RECIST 1.1),trong đó tiêu chí cho sự tiến triển là tăng ít nhất 20% đường kính dài nhất của tổnthương đích, đường kính được ghi nhận kể từ khi bắt đầu điều trị hoặc khi xuất hiệnmột hoặc nhiều tổn thương mới.<small>99</small>
Tiêu chí cụ thể hiện tại để xác định sự tiến triển củaUTTTL là những tiêu chí do PCWG3 đề xuất năm 2016, trong đó sự tiến triển sinh hóađược xác định là sự gia tăng hơn 25% của PSA trong hai lần liên tiếp cách nhau ít nhất
</div><span class="text_page_counter">Trang 28</span><div class="page_container" data-page="28">một tuần, với mức tăng tối thiểu 2,0 ng/mL so với giá trị ban đầu, và thời gian tăng gấpđôi PSA cũng được kết hợp để dự đoán mức độ của tiến triển.<small>100</small>
Đối với sự tiến triểncủa di căn hạch, tạng theo tiêu chuẩn RECIST 1.1, hạch phải có chiều dài ít nhất 10mm trên MSCT hoặc MRI. Tiến triển xương được định nghĩa là hai hoặc nhiều tổnthương mới xuất hiện trong xạ hình 99mTC, cần xác nhận bằng chụp MSCT hoặc MRIkhi kết quả không rõ ràng. Cuối cùng, mơi trường ―cắt tinh hồn‖ được định nghĩa lànồng độ Testosterone trong huyết thanh dưới 50 ng/dL hoặc 1,7 nmol/dL.<small>98</small> Định nghĩaUTTTL KCTH hiện tại của EAU dựa trên diễn tiến sinh hóa và, hoặc lâm sàng theotiêu chí PCWG3 và RECIST 1.1 với Testosterone huyết thanh dưới 50 ng/dL.<sup>51</sup>
<b>Theo AUA: tái phát sinh hóa với PSA tăng và, hoặc tiến triển của bệnh theo</b>
tiêu chuẩn chụp Xquang mặc dù mức Testostenrone máu dưới 50 ng/dL.
<b>Theo NCCN: tiến triển lâm sàng, Xquang hoặc sinh hóa của UTTTL mặc dù</b>
mức Testosterone máu dưới 50 ng/dL.<small>101</small>
<b>Theo ESMO: M</b><sub>0</sub> được xác định nếu xạ hình xương và MSCT (chậu, bụng) làbình thường và Testosterone máu dưới 0,5 ng/ml (dưới 50 ng/dL).<small>102</small>
<b>Theo EAU: </b>Mức Testosterone trong máu ở bệnh nhân đã được cắt bỏ tinh hoàncả hai bên là dưới 50ng/dL hoặc dưới 1,7 nmol/L. Và một trong hai tiêu chí sau:
+ Tiến triển sinh hóa: có ba lần tăng PSA liên tiếp, cách nhau ít nhất một tuần dẫnđến 2 lần tăng mức PSA, mỗi lần tăng thêm 50% so với PSA nadir và PSA hơn 2ng/mL hoặc,
+ Tiến triển về hình ảnh học: xuất hiện từ hai tổn thương xương trên xạ hìnhxương hoặc một tổn thương mơ mềm theo tiêu chuẩn RECIST.<small>103</small>
+ Tiến triển triệu chứng đơn thuần không đủ để chẩn đoán UTTTL KCTH.<sup>16,19,102</sup>
1.5. Chẩn đoán ung thư tuyến tiền liệt kháng cắt tinh hoàn
1.5.1. Triệu chứng lâm sàng
</div><span class="text_page_counter">Trang 29</span><div class="page_container" data-page="29">Bệnh nhân được chẩn đoán UTTTL và đã điều trị bằng nội tiết hoặc cắt tinhhoàn ngoại khoa, chẩn đoán UTTTL KCTH là chẩn đoán giai đoạn lâm sàng củaUTTTL.<sup>104</sup>
Hầu như khơng có triệu chứng ở bệnh nhân chưa di căn, khi triệu chứng xuấthiện bệnh đã ở giai đoạn di căn, triệu chứng rối loạn tiểu tiện, triệu chứng u xâm lấn,triệu chứng ở cơ quan di căn...<sup>104</sup>
Có thể có biểu hiện chèn ép, gây tắc nghẽn ở trực tràng hoặc đau dương vật.<sup>104</sup>
<i>1.5.1.2. Bệnh giai đoạn tiến triển</i>
Biểu hiện di căn xương: đau xương, gãy xương bệnh l …
Các hội chứng về thần kinh do ung thư di căn cột sống gây chèn ép tuỷ sốngnhư yếu, tê hoặc liệt hai chi dưới, rối loạn cơ vịng…
Muộn hơn có thể gặp di căn não, phổi, gan, dạ dày, tuyến thượng thận, xuấthuyết tiêu hố.
Bệnh nhân có thể đến viện trong tình trạng suy thận với các biểu hiện gầy sút,phù nề, xanh nhợt, thiếu máu.
Hội chứng cận ung thư, hội chứng Cushing, hội chứng kháng hormon chống bàiniệu, hội chứng tăng hoặc giảm can xi huyết.
Hội chứng thiếu máu, đông máu nội mạc rải rác…<sup>104-106</sup>1.5.2. Triệu chứng cận lâm sàng
<i>1.5.2.1. Xét nghiệm sinh hóa</i>
Urê, creatinin máu tăng có thể do tắc nghẽn niệu quản hai bên hoặc bướu xâmlấn đến vùng tam giác bàng quang hoặc chèn ép từ hạch vùng sau phúc mạc.
</div><span class="text_page_counter">Trang 30</span><div class="page_container" data-page="30">Thiếu máu có thể xuất hiện trong bệnh di căn.
Phosphatase kiềm có thể tăng cao khi có di căn xương. Phosphatase axit huyếtthanh có thể tăng cao với bệnh vượt ngồi giới hạn của tuyến tiền liệt.
Các xét nghiệm này mang tính chất tiên lượng.<small>104</small>
<i>1.5.2.2. Vai trị của Testosterone</i>
UTTTL là một bệnh phụ thuộc vào androgen<sup>107,108</sup> và Testosterone là yếu tốtăng trưởng tự nhiên của nó.<small>109</small> Hoạt động Testosterone qua trung gian bởi thụ thểandrogen, một yếu tố phiên mã được kích hoạt bằng hormone đóng vai trị trung tâmtrong sinh học và sự tiến triển của UTTTL.<small>108,110</small>
Các nghiên cứu tiền lâm sàng đã chứng minh rằng Testosterone kích thích sựphát triển của UTTTL,<small>111</small>giảm đáng kể nồng độ Testosterone trong huyết thanh, có thểkéo dài thời gian sống còn cho bệnh nhân UTTTL KCTH.<small>108,112,113</small>
Tuy nhiên bằng chứng hiện tại cho rằng nồng độ androgen nội sinh khơng làmtăng nguy cơ chẩn đốn UTTTL,<small>114,115</small>
liệu pháp Testosterone ở nam giới bị thiếu hụtTestosterone không làm tăng nguy cơ UTTTL<sup>116,117</sup> những người đàn ông được điều trịbằng Testosterone sau khi điều trị UTTTL khu trú không tăng tỉ lệ tái phát cao hơnhoặc có kết quả xấu hơn; mặc dù số lượng các nghiên cứu được công bố cho đến nayvẫn còn hạn chế.<small>118</small> Những nghịch l này được giải thích bởi mơ hình bão hịa. Nó đãđược chứng minh trên thực tế, sự tăng trưởng của UTTTL đó chỉ phụ thuộc vàoandrogen ở mức thấp của nồng độ Testosterone, đạt đến điểm bão hòa mức nồng độTestosterone huyết thanh tương đối thấp và trở nên trơ với những thay đổi trong huyếtthanh androgen ở nồng độ cao hơn.<small>119</small>
AR là động lực chính cho sự phát triển và tiến triển của UTTTL,<small>108,110</small> mứcTestosterone thấp nhất trong ADT dịng đầu tiên thường có được lợi ích lớn hơn từ liệupháp này và lợi thế sinh tồn; tuy nhiên ở giai đoạn KCTH, mức Testosterone thấp hơncó thể là dấu hiệu của tình trạng tiên lượng kém.<small>120</small>
</div><span class="text_page_counter">Trang 31</span><div class="page_container" data-page="31">Đánh giá mức Testosterone từ 3 đến 6 tháng đã được đề xuất để đảm bảo việccắt tinh hoàn đạt ngưỡng (đặc biệt là trong quá trình dùng ADT) và duy trì. Trongtrường hợp khơng đạt được ngưỡng, nên cân nhắc chuyển sang một chất đồng vận hoặcchất đối vận hoặc cắt bỏ tinh hồn. Ở những bệnh nhân có PSA tăng đã được xác nhậnvà, hoặc tiến triển lâm sàng, Testosterone huyết thanh phải được đánh giá trong mọitrường hợp để xác nhận tình trạng UTTTL KCTH.<sup>121,122</sup>
<i>1.5.2.3. Vai trò của PSA</i>
Năm 1987, Stamey đã báo cáo một nghiên cứu lâm sàng, nêu lên vai trò củaPSA trong UTTTL. Từ đó, xét nghiệm PSA huyết thanh tạo ra cuộc cách mạng vàđóng vai trị quan trọng trong việc chẩn đoán và theo dõi điều trị UTTTL.<sup>123</sup>
PSA là kháng nguyên đặc hiệu của tuyến tiền liệt có ở mơ tuyến tiền liệt bìnhthường và tân sinh, mức ―bình thường‖ là ≤4 ng/mL, những năm qua khơng có ngưỡng―bình thường‖ duy nhất cho PSA; PSA thay đổi như một biến liên tục, phản ánh tuổitác, kích thước tuyến tiền liệt và nguy cơ UTTTL.<small>124</small>
Ngồi vai trò là dấu ấn sinh học chỉ điểm cho các phương pháp chẩn đốn, PSAcịn có vai trị báo hiệu ung thư hình thành, xâm lấn và di căn. PSA là trọng tâm đểtheo dõi hiệu quả của các liệu pháp điều trị UTTTL gợi tiến hành các chẩn đốn hìnhảnh, là dấu ấn sinh học chẩn đoán theo dõi và tiên lượng cho sự tiến triển củaUTTTL.<sup>125</sup>
Mức PSA xác định sự thất bại điều trị phụ thuộc vào phương pháp điều trịchính. Bệnh nhân có PSA tăng sau cắt tuyến tiền liệt tận gốc hoặc xạ trị tuyến tiền liệttriệt căn có các nguy cơ khác nhau về bệnh di căn có triệu chứng dựa trên các giá trịkhác nhau mức PSA. Sau cắt tuyến tiền liệt tận gốc nồng độ PSA thường bằng 0 sauphẫu thuật ba tuần, ngưỡng dự đoán tốt nhất về sự di căn xa là PSA hơn 0,4 ng/mL.<small>126</small>Sau xạ trị tuyến tiền liệt triệt căn có hoặc khơng có liệu pháp nội tiết tố bổ trợ, địnhnghĩa của RTOG-ASTRO về thất bại là 'bất kỳ mức tăng PSA nào cao hơn 2 ng/mL(giá trị nadir), không phụ thuộc vào nồng độ trong huyết thanh của nadir.<sup>127</sup>
</div><span class="text_page_counter">Trang 32</span><div class="page_container" data-page="32">Nhóm cơng tác lâm sàng về UTTTL 3 xác định điểm cuối cho thiết kế thửnghiệm lâm sàng là tăng 25% so với nadir (xét giá trị ban đầu là ≥1 ng/mL), với mứctăng tối thiểu là 2ng/mL, trong bối cảnh ―cắt tinh hoàn‖ (Testosterone < 50 ng/mL) làdấu hiệu của sự tiến triển.<small>128</small>
Sau điều trị nội tiết, nồng độ PSA sau 3 tháng có giá trị tiên lượng thời giansống còn. Đo sự gia tăng PSA theo cấp số nhân qua thời gian tức là PSADT càng ngắncó nghĩa là PSA tăng càng nhanh. PSADT ít có giá trị trong chẩn đốn, nhưng có giátrị trong theo dõi sau điều trị UTTTL. PSADT càng ngắn là thơng số dự đốn ung thưtái phát tại chỗ hoặc di căn, đặc biệt sau điều trị triệt căn bằng phẫu thuật hay xạ trị.<small>51</small>
Sự gia tăng mức PSA thường trước khi bắt đầu các triệu chứng lâm sàng vàitháng. PSA tăng cao nên đánh giá mức Testosterone, đây là điều bắt buộc để xác định
UTTTL KCTH. Tuy nhiên, hiện nay người ta đã thừa nhận rằng PSA ổn định trongthời gian ADT không đủ để mô tả một tình huống khơng tiến triển.<sup>129</sup>
Chỉ số PSA được đo trước khi điều trị UTTTL và cần được theo dõi định kì.Khoảng cách giữa mỗi lần đo l tưởng là 4 tuần, nhưng có thể thay đổi từ 3 - 6 tháng,tùy theo mỗi cá nhân và quá trình theo dõi của từng trung tâm niệu khoa.<sup>130</sup>
<i>1.5.2.4. Vai trị của chẩn đốn hình ảnh</i>
Khi có sự tiến triển của PSA việc phát hiện UTTTL, di căn phụ thuộc rất nhiềuvào hình ảnh từ đó có thể xem xét điều chỉnh liệu pháp điều trị.
Chụp cắt lớp vi tính có tiêm thuốc cản quang cung cấp thông tin về mức độ xâmlấn các tạng lân cận, hạch bạch huyết hoặc di căn xương, các tổn thương kèm theo nếucó ở vùng tầng sinh mơn và tiểu khung.<sup>131</sup>
Chụp cắt lớp vi tính và chụp cộng hưởng từ là những xét nghiệm tốn kém, nênthực hiện chọn lọc trên một số bệnh nhân. Chuỗi xung T2W được sử dụng để đánh giágiai đoạn UTTTL. Ở từ trường 1,5T MRI có độ nhạy thấp trong việc phát hiện ung thưxâm lấn ra khỏi tuyến tiền liệt (22-88%) hoặc xâm lấn túi tinh (0-71%) nhưng lại có độ
</div><span class="text_page_counter">Trang 33</span><div class="page_container" data-page="33">xâm lấn túi tinh).<sup>132</sup> Ngồi ra, MRI chỉ có thể phân biệt giai đoạn T<sub>1-2</sub>, T<sub>3</sub> với độ chínhxác khoảng 50-85% do MRI không thể phát hiện ung thư xâm lấn ra khỏi tuyến tiềnliệt về mặt vi thể.<sup>133</sup>
MSCT và MRI đánh giá di căn hạch gián tiếp qua đo đường kính hạch bạchhuyết. Với ngưỡng 10mm, độ nhạy của MSCT và MRI trong đánh giá di căn hạch nhỏhơn 40%. Độ nhạy, độ đặc hiệu, giá trị tiên đoán âm và giá trị tiên đoán dương của
MSCT lần lượt là 7%, 100%, 85% và 100%.<sup>134</sup> MRI có độ nhạy thấp trong việc pháthiện ung thư xâm lấn về mặt vi thể, không được khuyến cáo để phân giai đoạn ở nhữngbệnh nhân nguy cơ thấp, MRI nên thực hiện ở những bệnh nhân có nguy cơ cao và rấtcao.<sup>135</sup>
Để đánh giá tính tồn vẹn của vỏ xương tại vị trí đã biết có di căn xương, MSCT
được ưu tiên sử dụng. MSCT có thể phát hiện tổn thương di căn xương trước khi tổnthương thấy được trên Xquang. Ưu điểm khác của MSCT so với Xquang là nó chophép phát hiện bệnh mơ mềm liên quan và cung cấp hình ảnh ba chiều.<sup>106</sup>
MRI nhạy hơn MSCT trong việc phát hiện di căn, cho phép xác định rõ hơnphạm vi của khối u, đặc biệt hữu ích cho bệnh nhân di căn cột sống để đánh giá mức độcủa bệnh lý tủy và ngoài tủy. Tủy xương bình thường chứa một tỉ lệ mỡ cao và cócường độ tín hiệu cao trên xung T1. Tổn thương di căn hiển thị giảm tín hiệu trên xungT1, ngược lại trên xung T2W nó có tín hiệu cao hơn so với tủy bình thường xungquanh.<sup>106</sup>
MRI tồn thân và xương trục nhạy hơn xạ hình xương và chụp Xquang thôngthường trong việc phát hiện di căn xương ở UTTTL có nguy cơ cao. MRI tồn bộ cơthể cũng có thể phát hiện di căn tạng và hạch bạch huyết; nó được chứng minh là nhạyvà đặc hiệu hơn so với kết hợp chụp Xquang nhắm mục tiêu và MSCT bụng chậu.<small>136</small>
<i>1.5.2.5. Vai trị của xạ hình xương</i>
Chỉ riêng PSA là không đủ tin cậy để theo dõi hoạt động của bệnh trong UTTTL
KCTH tiển triển vì di căn tạng có thể phát triển mà khơng tăng PSA.<sup>137</sup> Do đó, PCWG2
</div><span class="text_page_counter">Trang 34</span><div class="page_container" data-page="34">khuyến nghị kết hợp xạ hình xương và chụp MSCT, đo PSA và lâm sàng trong việcđánh giá UTTTL KCTH.<sup>138</sup>
Xạ hình xương là cơng cụ hữu ích để phát hiện ung thư di căn xương. Xạ hìnhxương có giá trị tiên đốn âm từ 87-100%. Tuy nhiên, lợi ích của việc chẩn đoán lạiphụ thuộc nhiều vào trị số PSA, giai đoạn T và điểm số Gleason. Trong một phân tíchgộp, tỉ lệ xạ hình xương dương tính lần lượt là 2,3%; 5,3%; 16,2%; 39,2% và 73,4%với PSA huyết thanh lần lượt là 0- 9,9; 10-19,9; 20-49,9; và hơn 100 ng/mL.<small>106,139</small>
Di căn xương hiếm khi xảy ra ở những bệnh nhân không triệu chứng. Hầu hếtcác khuyến cáo thực hiện xạ hình xương khi có PSA từ 20 ng/mL trở lên, điểm sốGleason 8-10, giai đoạn cT<sub>3-4</sub>, hoặc có triệu chứng nghi ngờ di căn xương.<small>19,139</small>
Tuy nhiên, xạ hình xương bị giới hạn bởi hiện tượng 'bùng phát', được xác địnhlà sự phát triển của các hình ảnh mới do điều trị gây ra trong lần xạ hình theo dõi đầutiên. Bùng phát được quan sát thấy trong vòng 8 - 12 tuần kể từ khi bắt đầu điều trị vàcó thể dẫn đến chẩn đốn dương tính giả về sự tiến triển của bệnh.
<i>1.5.2.6. Vai trị của chẩn đốn phân tử</i>
Tất cả bệnh nhân di căn nên được xét nghiệm soma để tìm khiếm khuyết sửachữa gen tương đồng và các khuyết tật MMR, nhất là trên mô ung thư biểu mô di cănnhưng cũng có thể thực hiện xét nghiệm trên khối u nguyên phát. Ngoài ra, xét nghiệmdi truyền trên DNA tế bào khối u lưu hành là một lựa chọn đã được sử dụng trong mộtsố thử nghiệm. Thử nghiệm FoundationOne<small>®</small> Liquid CDx đã được FDA chấp thuận,<sup>140</sup>MMR bị lỗi có thể được thực hiện bằng IHC đối với các protein MMR (MSH2, MSH6,MLH1, PMS2) và, hoặc bằng các xét nghiệm giải trình tự thế hệ mới.<sup>141</sup> Nên xétnghiệm tế bào mầm để tìm BRCA<sub>1-2</sub>, ATM và MMR đối với những trường hợp cónguy cơ cao và đặc biệt là UTTTL di căn nếu có triệu chứng lâm sàng.
Antonarakis và cộng sự<small>142</small>
đã chứng minh AR-V7 trong CTC (các tế bào khối ulưu hành) và kháng ARPI ở bệnh nhân UTTTL KCTH di căn. Thử nghiệm được sử
</div><span class="text_page_counter">Trang 35</span><div class="page_container" data-page="35">trên CTC phát hiện RNA thông tin AR-V7. Các phương pháp khác để đánh giá CTCcủa AR-V7 đã được phát triển với kết quả tương tự.<small>143</small>
Các khối u từ phần lớn bệnhnhân mắc UTTTL KCTH di căn chứa đột biến gen liên quan đến con đường truyền tínhiệu của thụ thể androgen. Xét nghiệm biến thể ghép AR-V7 trong CTC có thể hướngdẫn lựa chọn điều trị trong môi trường UTTTL KCTH di căn sau Abiraterone hoặcEnzalutamide.
<i>1.5.2.7. Vai trị của mơ bệnh học</i>
Hơn 95% UTTTL là carcinoma tế bào nang tuyến hay carcinoma tuyến, 5%
UTTTL gồm 2 nhóm ung thư tế bào biểu mơ và ung thư khơng có nguồn gốc từ tế bàobiểu mơ. UTTTL khơng có nguồn gốc từ tế bào biểu mô gồm sarcoma cơ trơn,sarcoma mạch máu, sarcoma cơ vân, lymphoma... UTTTL là ung thư tế bào biểu môgồm carcinoma tế bào nhẫn, carcinoma tế bào chuyển tiếp, carcinoma biểu mơ tế bàovảy...<sup>144</sup>
Hình 1. 5. Hệ thống phân độ Gleason
<i><small>A. Sơ đồ hệ thống Gleason</small></i>
<i><small>B. Độ 1: Nang tuyến đơn, đồng dạng, sắp xếp chặt chẽ</small></i>
<i><small>C. Độ 2: Nang tuyến đơn, không đồng dạng, sắp xếp không chặt chẽD. Độ 3: Nang nhỏ rời rạc, thâm nhiễm giữa các tuyến lành</small></i>
<i><small>E. Độ 4: Ngang tuyến và tế bào hòa vào nhau không theo quy luật, dạng sàng</small></i>
</div><span class="text_page_counter">Trang 36</span><div class="page_container" data-page="36"><i><small>F. Độ 5: Những ổ tế bào bướu đặc với hoại tử trung tâm</small></i>
<i>(Nguồn: Epstein, J. I. (2016), Pathology of Prostatic Neoplasia, in CampbellWalshUrology).<sup>145</sup></i>
Phân độ mô học theo thang điểm Gleason, điểm Gleason là tổng độ mô học ácthứ nhất và thứ hai trên mẫu bệnh phẩm. Hệ thống phân loại mô bệnh học mới nhất củaUTTTL dựa trên hội nghị đồng thuận của Hiệp hội Quốc tế về Bệnh học Tiết niệu 2014(ISUP) chia ra 5 nhóm dựa trên điểm Gleason như sau:<sup>146</sup>
Nhóm 1: ≤ 6 điểmNhóm 2: 3 + 4 = 7 điểmNhóm 3: 4 + 3 = 7 điểmNhóm 4: 8 điểm
Nhóm 5: 9 – 10 điểm
Hệ thống phân độ Gleason cho UTTTLsử dụng hiện nay được báo cáo lần đầutiên năm 1966, sau đó được Hiệp hội Giải phẫu bệnh Tiết niệu quốc tế (ISUP) đồngthuận áp dụng cho phân loại mức độ biệt hóa UTTTL. Hệ thống phân độ Gleason đượcnghiên cứu và cải biên nhiều lần (năm 2005, năm 2008, năm 2014) nhằm tăng giá trịtiên lượng nguy cơ tái phát sau điều trị.
Điểm số Gleason là một tiêu chuẩn về mô học đánh giá độ ác tính của UTTTL
là một trong những yếu tố tiên lượng bệnh, phân độ mô học theo điểm Gleason từ độ 1đến độ 5 có mức độ tiên lượng xấu dần. Tiên lượng thời gian sống còn 15 năm kể từkhi chẩn đoán UTTTL ở nhóm có điểm Gleason 5-7 tốt hơn so với nhóm có điểmGleason 8-10 hay nhóm có độ mơ học 1-3 tốt hơn so với nhóm có độ mơ học 4 và 5.<sup>146</sup>
Cần lưu có một số dạng mô học UTTTL không phân độ mô học được theo hệthống phân độ Gleason, đặc biệt là các ung thư có nguồn gốc trung mơ và một số biếnthể carcinoma hiếm khác của tuyến tiền liệt (phụ lục 4).
1.5.3. Chẩn đoán giai đoạn ung thư tuyến tiền liệt
</div><span class="text_page_counter">Trang 37</span><div class="page_container" data-page="37">Nguy cơthấp
Nguy cơ
cT<sub>1-2a </sub> vàGS < 7 vàPSA ≤ 10ng/mL
cT<sub>2b</sub> hoặcGS = 7 hoặcPSA10-20ng/mL
cT<sub>2c</sub> hoặcGS > 7 hoặcPSA > 20ng/mL
PSA bất kỳGS bất kỳcT<sub>3-4</sub> hoặcN<sub>1</sub>
PSA bất kỳGS bất kỳcT bất kỳ
cN bất kỳ,M<sub>1</sub>
Giai đoạn khu trú <sup>Tiến triển tại</sup>
UTTTL KCTH là giai đoạn cuối trong lịch sử diễn tiến của bệnh nhân UTTTL,được phân giai đoạn dựa trên các yếu tố TNM theo AJCC 2017,<small>147,148</small> (phụ lục 3) phângiai đoạn và nguy cơ tiến triển sinh hóa theo yếu tố T, nồng độ PSA, điểm Gleasontheo EAU 2017<sup>132</sup> (bảng 1.1)và NCCN 2022.<sup>135,149,150</sup>
Bảng 1. 2.
Nhóm nguy cơ UTTTL theo NCCN 2022Nguy cơ rất thấp cT1c, GS ≤ 6, PSA < 10 ng/mLNguy cơ thấp cT<small>1-2a, GS ≤ 6, PSA < 10 ng/mL</small>Nguy cơ trung bình cT<sub>2b-2c, </sub>GS = 7, PSA 10-20 ng/mLNguy cơ cao cT<sub>3a</sub> hoặc GS 8-10 hoặc PSA > 20 ng/mLNguy cơ rất cao <sup>cT</sup><sup>3b-4 , </sup><sup>độ mô học đầu tiên trong GS là 5 hoặc > 4</sup>mẫu sinh thiết, GS 8-10
Di căn tại chổ T bất kỳ, N<sub>1</sub>, M<sub>0</sub>Di căn xa T bất kỳ, N bất kỳ, M<sub>1</sub>
UTTTL KCTH là giai đoạn tiến triển của UTTTL, được chia thành 2 giai đoạn:+ M<sub>0</sub>: khi không phát hiện di căn trên hình ảnh học
</div><span class="text_page_counter">Trang 38</span><div class="page_container" data-page="38">+ M<sub>1</sub>: khi có di căn hạch, tạng hoặc xương trên hình ảnh học
Bảng 1. 3.
Phân loại di căn theo CHAARTED và LATITUDECHAARTED<sup>19,151,152</sup>(khối lượng)
- Có từ 4 di căn xương trở lên và hơn một bênngoài cột sống hoặc xương chậu
- Di căn tạng<sup>a</sup>
Khơng cao
LATITUDE<sup>19,153</sup>(nguy cơ)
(có 2 trong 3 yếu tố)- Gleason từ 8 trở lên
- Ba tổn thương xương trở lên- Di căn tạng
Không cao
<i><small>: Hạch không được coi là di căn tạng</small></i>
1.5.4. Theo dõi điều trị
Theo dõi bao gồm theo dõi các tác dụng phụ hoặc biến chứng của liệu pháp điềutrị, kết quả chức năng và phát hiện sự tiến triển
<i>a. Diễn biến lâm sàng và tác dụng phụ của thuốc điều trị</i>
Bệnh nhân cần được tái khám định kì để theo dõi các triệu chứng lâm sàng. Cácdấu hiệu sớm của chèn ép tủy, bế tắc đường tiết niệu, tổn thương hủy xương cần đượckhám và đánh giá kĩ...<small>132</small>
Theo dõi creatinine khi bệnh nhân có suy thận do UTTTL chèn ép 2 niệu quảnhay gây bế tắc đường tiểu dưới. Theo dõi chức năng gan định kì để đánh giá tác dụngphụ của các thuốc điều trị nội tiết.<sup>132</sup>
Bệnh nhân khơng có triệu chứng lâm sàng, với chỉ số PSA khơng tăng, khơngcần thực hiện các xét nghiệm hình ảnh học định kì.<sup>154</sup> Xạ hình xương được thực hiệnkhi có sự tiến triển chỉ số PSA, xuất hiện các triệu chứng gãy xương bệnh lý.
Các xét nghiệm hình ảnh học thực hiện khi cần đánh giá sự tiến triển của bệnh
</div><span class="text_page_counter">Trang 39</span><div class="page_container" data-page="39"><i>b. Theo dõi Testosterone huyết thanh</i>
Sau cắt 2 tinh hồn ngoại khoa Testosterone nhanh chóng giảm xuống mức dưới50 ng/dL, chỉ trong 24 giờ, Testosterone còn lại xuống dưới 10% so với trước mổ.Bệnh nhân UTTTL khi được điều trị với nội tiết sẽ đạt được nồng độ Testosterone ởmức cắt tinh hoàn sau 2 - 4 tuần. Mục tiêu của bệnh nhân UTTTL khi điều trị nội tiết làduy trì nồng độ Testosterone huyết thanh ở mức cắt tinh hoàn. Trong thời gian dài,mức cắt tinh hoàn được định nghĩa khi nồng độ Testosterone huyết thanh dưới50ng/dL. Tuy nhiên, vào năm 1996, khi xét nghiệm miễn dịch huỳnh quang được ápdụng trên lâm sàng đã đo được nồng độ Testosterone huyết thanh chính xác với độnhạy là 0,1 ng/dL. Dựa vào đó, Oefelein và cộng sự đã thực hiện một nghiên cứu đánhgiá lại mức Testosterone huyết thanh đạt được với phẫu thuật cắt 2 tinh hoàn đối vởi 35bệnh nhân UTTTL tiến triển. Kết quả ghi nhận nồng độ Testosterone huyết thanh trungbình sau phẫu thuật cắt hai tinh hồn là 15 ng/dL (10-30).<sup>155</sup> Vì vậy, hiện nay một địnhnghĩa mới về mức cắt tinh hoàn là nồng độ Testosterone huyết thanh nhỏ hơn 20ng/dL, dù chưa thống nhất.<sup>132</sup> Klotz và cộng sự đã thực hiện nghiên cứu PR7 theo dõi626 bệnh nhân điều trị nội tiết trong vòng 8 năm và rút ra kết luận chỉ số Testosteronehuyết thanh nhỏ hơn 20 ng/dL trong năm đầu sẽ làm giảm tỉ lệ tử vong do bệnh và kéodài thời gian trước khi bệnh tiến đến giai đoạn KCTH.<sup>156</sup> Ngoài ra tác giả Perachino vàcộng sự nghiên cứu ở 129 bệnh nhân UTTTL di căn xương được điều trị nội tiết đãtìm thấy sự liên quan của nguy cơ tử vong do UTTTL và nồng độ Testosterone đạtđược khi điều trị nội tiết. Nồng độ Testosterone huyết thanh duy trì càng thấp thì càngtốt cho bệnh nhân.<sup>157</sup>
Testosterone huyết thanh là một mục tiêu quan trọng khi điều trị UTTTL tiếntriển, giúp đánh giá hiệu quả của liệu pháp nội tiết, diễn tiến của UTTTL trên lâm sàng.Do đó theo dõi nồng độ Testosterone là cần thiết khi điều trị nội tiết. Theo dõiTestosterone ở các thời điểm sau:<sup>158</sup>
+ Trước khi điều trị nội tiết
</div><span class="text_page_counter">Trang 40</span><div class="page_container" data-page="40">+ Đo cùng với chỉ số PSA đầu tiên sau khi bắt đầu điều trị nội tiết+ Mỗi 6 tháng
+ Khi chỉ số PSA tăng hay có diễn tiến trên lâm sàng+ Khi thay đổi phương pháp điều trị
Nồng độ Testosterone nên được đo tại cùng một trung tâm xét nghiệm trongsuốt quá trình điều trị của bệnh nhân
Thay đổi phương pháp điều trị khác khi không đạt nồng độ Testosterone mongmuốn trước khi đánh giá lại trên lâm sàng UTTTL tiến triển đến giai đoạn KCTH.
<i>c. Theo dõi chỉ số PSA huyết thanh</i>
Tuy phần lớn bệnh nhân UTTTL tiến triển sẽ đáp ứng tốt với điều trị nội tiếttrong giai đoạn đầu, hầu hết bệnh nhân UTTTL sẽ tiến tới giai đoạn KCTH. Do đó,theo dõi chỉ số PSA huyết thanh thường xuyên giúp đánh giá đáp ứng điều trị và tiênlượng sự tiến triển của UTTTL. Chỉ số PSA nadir là yếu tố quan trọng giúp chúng tadự đoán khả năng tiến triển của UTTTL. Bệnh nhân UTTTL đạt được chỉ số PSA nadirdưới 0,2 ng/mL sau thời gian theo dõi trung bình 7 tháng thì thời gian sống cịn trungbình dài nhất (75 tháng), với PSA nadir từ 0,2- 4 ng/mL (44 tháng) hay PSA nadir trên4ng/mL (13 tháng)<sup>159</sup>. Gần đây một số nghiên cứu đã chứng minh PSA nadir thấp(ngưỡng 0,2 ng/mL) và thời gian từ khi điều trị đến khi đạt PSA nadir dài (ngưỡng 10tháng) sẽ làm tăng tỉ lệ sống còn và kéo dài thời gian tiến triển.<sup>160</sup>
Chỉ số PSA được đo trước khi điều trị UTTTL và được theo dõi định kì. Khoảngcách giữa mỗi lần đo l tưởng là 4 tuần,<sup>130</sup> nhưng có thể thay đổi từ 3 - 6 tháng, tùytheo mỗi cá nhân và quá trình theo dõi của từng trung tâm niệu khoa. Các biến số PSAcần quan tâm khi theo dõi PSA huyết thanh là:
- PSA nền: chỉ số PSA khi bắt đầu điều trị nội tiết.
- PSA nadir: là giá trị PSA thấp nhất, gần như triệt tiêu sau khi kết thúc một liệupháp điều trị (xạ triệt căn, phẫu thuật triệt căn, nội tiết).
</div>