giáo trình bài giảng về acetone
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (325.38 KB, 18 trang )
1
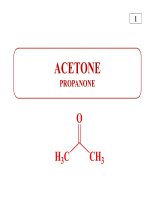
ACETONE
PROPANONE
H
3
C CH
3
O
2
TÍNH CHẤT VẬT LÝ
-
Chất lỏng không màu, trong suốt, có màu đặc trưng
- Tỉ trọng: 0.791 g/cm
3
- Nhiệt độ đông đặc: -95
o
C
- Nhiệt độ sôi: 56 – 57
o
C
- Tan vô hạn trong nước
- Áp suất hơi: 24.46 - 24.60 kPa (20
o
C)
- Độ nhớt: 0.3075 cP (20
o
C)
3
H
3
C
C
C H
3
O
+ H
2
C H
3
-C H O H -C H
3
+ N aH SO
3
H
3
C C C H
3
O H
+ C H (O E t)
3
H
3
C C C H
3
O E t
SO
3
N a
O E t
+ H C N
H
3
C C C H
3
O H
C N
+ 2 C
6
H
5
O H
H
3
C C C H
3
C
6
H
4
O H
C
6
H
4
O H
+ H
2
O
+ (C H
3
)
2
C O
H
3
C C
H
2
C
O H
C H
3
C C H
3
O
TÍNH CHẤT HÓA HỌC
4
Phản ứng thế nguyên tử O của nhóm carbonyl
H
3
C
C
H
3
C
O
H N
X
H
+
C
H
3
C
H
3
C
OH
N-H-X
C
H
3
C
H
3
C
N-X
- H
2
O
H
3
C
C
CH
3
O
+ PCl
5
+ POCl
3
H
3
C
C
CH
3
Cl Cl
5
ỨNG DỤNG
Axeton là hoá chất thông dụng, được dùng trong hầu
hết các ngành sản xuất như:
• Chất dẻo
• Các loại sợi
• Dược phẩm
• Sơn, mực in, keo, nhựa, thuốc nhuộm, thuốc rửa,…
• Dung môi
• Nguyên liệu để tổng hợp methylisobutyl ketone,
methyl methacrylate, ketene, and diacetone alcohol.
6
TÌNH HÌNH SẢN XUẤT
Thế giới
- 2010: 6.7 triệu tấn acetone (USA – 1.56 triệu tấn)
- INEOS Phenol 17% tổng sản lượng acetone thế giới
- 2011: giá 1100 – 1250 $/ton
Việt Nam
Chủ yếu là nhập khẩu từ Trung Quốc.
7
CÁC LƯU Ý KHI SỬ DỤNG ACETONE
Dễ cháy
Tạo hợp chất gây nổ (acetone peroxide)
Tính độc
- Nồng độ cao (khoảng 9200 ppm) có thể gây kích ứng
ở cổ họng trong khoảng 5 phút.
- Nồng độ 1000 ppm sẽ gây kích ứng ở mắt và cổ họng
trong vòng 1 giờ.
DEHYDROGENATION OF
ISOPROPANOL
OXIDATION OF CUMENE
OXIDATION OF PROPYLENE
8
PRODUCTION OF ACETONE
9
2 CH
3
-CH=CH
2
+ O
2
H
o
298
= -255 kJ/mol
2 CH
3
-CO-CH
3
OXIDATION OF PROPYLENE
HOECHST-WACKER CHEMIE
TECHNOLOGY
10
Xúc tác: Hỗn hợp PdCl
2
– CuCl
2
trong pha lỏng
Cơ chế quá trình oxy hóa propylene bởi xúc tác phức kim loại:
Tái sinh xúc tác:
Pd + 2 CuCl
2
PdCl
2
+ 2 CuCl
2 CuCl + 2 HCl + 1/
2
O
2
2 CuCl
2
+ H
2
O
CH
3
CH=CH
2
+ PdCl
2
+ 2 HCl PdCl
3
CH
3
CH=CH
2
+ Cl
-
+ 2 H
+
+ H
2
O
CH
3
COCH
3
+ Pd + H
+
+ 2 Cl
-
CH
3
CH(OH)CH
2
PdCl
2
)
PdCl
3
CH
3
CH=CH
2
(CH
3
CH(OH)CH
2
PdCl
2
) + Cl
-
+ H
+
OXIDATION OF PROPYLENE
50
o
C
0.1 MPa
120
o
C
0.5 MPa
110
o
C
1.2 MPa
H
2
O, CH
3
COOH, ClCH
2
COCH
3
, ClCH-CO-CH
2
Cl,
CH
3
-CHCl-CHO, CH2Cl-CHCl-CHO
115
o
C
1.2 MPa
C
3
H
6
C
3
H
8
OXIDATION OF PROPYLENE
ACETONE
C
2
H
5
CHO
12
- Copper catalyst on porous (SiO
2
, Al
2
O
3
-SiO
2
,…)
- Vapor phase reaction
DEHYDROGENATION OF
ISOPROPANOL
H
C
OH
CH
3
H
3
C
CH
3
-CO-CH
3
+ H
2
400-500
o
C
3 - 4 atm
Cu
H
o
298
= 55 kJ/mol
13
- First, isopropanol is heated using steam to vaporize the same.
Then, isopropanol is compressed to 4 – 5 atms
- The compressed isopropanol then enters a catalytic shell and
tube reactor in the tube side. The tube is packed with the
porous copper catalyst.
The reactor is operated at 400 – 500
o
C using flue gas for
heating. The flue gas is passed in the shell side of the shell and
tube reactor.
After reaction, the gases are condensed using cooling water
condenser:
- The condensed isopropanol and acetone are sent for
fractionation.
- The gases consisting of the remaining quantities of
isopropanol and acetone are absorbed into water using a
water scrubber.
DEHYDROGENATION OF
ISOPROPANOL
14
The acetone + isopropanol + water obtained from the
condenser are sent to an acetone fractionator that
separates acetone as the top product and isopropanol +
water as bottom product.
- The bottom product isopropanol + water from the
acetone fractionators is sent to a isopropopanol column.
- This column produces water as the bottom product and
isopropanol as the top product.
- The water is cooled using a water condenser and sent to
the water scrubber as fresh water solvent.
DEHYDROGENATION OF
ISOPROPANOL
15
Flow sheet of acetone manufacture from isopropanol
DEHYDROGENATION OF
ISOPROPANOL
16
OXIDATION OF CUMENE
+ CH
3
CH=CH
2
AlCl
3
/ HF
50
o
C, 1-10 bar
C
H
3
C
CH
3
CH
H
3
C
CH
3
+ O
2
salt of Co
120
o
C
CH
H
3
C
CH
3
O OH
C
H
3
C
CH
3
O OH
H
2
SO
4
50
o
C
OH
C
CH
3
H
3
C
O
+
H
o
298
= -112 kJ/mol
H
o
298
= -116 kJ/mol
H
o
298
= -253 kJ/mol
17
• Nhiệt độ: 120
0
C
• Áp suất: 1 atm
• Quá trình phản ứng trong pha lỏng
• Độ chọn lọc của cumene là 90%
• Tỉ lệ sản phẩm là 60% phenol và 40% aceton
OXIDATION OF CUMENE
18
OXIDATION OF CUMENE
Cumylphenol / acetophenone residues
7 kPa
Cumene
70-80
o
C
0.1-0.2 Mpa
20-30 min.