Bài 13. Luyện tập chương 1: Các loại hợp chất vô cơ
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (783.06 KB, 9 trang )
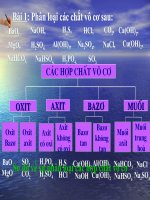
Bài 1: Phân loại các chất vô cơ sau:
BaO,
NaOH,
H2S,
HCl,
H2SO4, Al(OH)3, Na2SO4,
MgO,
NaHCO3,
NaHSO4,
H3PO4,
SO3.
CO2, Ca(OH)2,
NaCl, Cu(OH)2,
C¸c hîp chÊt v« c¬
oxit
Axit
Baz¬
Muèi
Muèi
Axit
Baz¬
Oxit Oxit
Muèi
Baz¬
Axit
trung
kh«ng
kh«ng
Baz¬ axit cã oxi
axit
tan
hoµ
cã oxi
tan
H3PO4 H2S Ca(OH)2 Al(OH)3 NaHCO NaCl
SO3
BaO
3
Sơ
đồ
về
sự
phân
loại
các
hợp
chất
vô
cơ
MgO
H2SO4 HCl NaOH Cu(OH)2 NaHSO Na2SO4
CO2
4
2. Tính chất hoá học của các loại hợp chất
vô cơ:
OXIT AXIT
OXIT BAZƠ
?
+ Axit
+ Oxit axit
Nhiệt
+ H2O phân
huỷ
?
Muối + kim loại
?
+ H2O
+ Bazơ
?
?
+ Axit
+
Kim
loại
+ Axit
+ Oxit axit + Bazơ
+ Oxit bazơ
+ Muối
+ Muối
?
Chú thích:
Muối + Muối
?
MUốI
?
BAZƠ
+ Bazơ
+ Oxit bazơ
?
AXIT
Hai muối mới.
Kim loại mới + Muối mới.
Muối nhiệt phân huỷ sinh ra nhiều chất khác.
Bài tập 2:
Căn cứ vào sơ đồ biểu thị những tính chất hóa học của chất vô cơ,
hãy chọn các chất thích hợp để viết các phương trình hóa học cho
mỗi loại hợp chất
Làm việc theo nhóm trong 5 phút
Nhóm 1: làm phần 1.Oxit
Hết Nhóm
giờ 2:! làm phần 2. Bazơ
Nhóm 2: làm phần 3.Axit
Nhóm 4: làm phần 4.Muối
BẢN ĐỒ TƯ DUY
HÓA HỌC
II-Bài tập :
Bài 3:Em hãy chọn phơng án đúng để nhận biết các dung dịch sau: H2SO4,
HCl, Na2SO4, NaOH.
A. Quỳ tím và dd Ba(OH)2
B. Dung dịch phenolphtalein và dd Ba(OH)2
C. Chỉ cần dùng dd Ba(OH)2.
D. Chỉ cần dùng dd BaCl2.
Đáp án: A.
H2SO4, HCl, Na2SO4, NaOH
+ Quỳ tím
Màu
đỏ
Màu xanh
H2SO4, HCl
+ dd Ba(OH)2
Có kết tủa
H2SO4
Không kết
tủa
HCl
NaOH
Không
màu
Na2SO4
Bài tập 4: Để 1 mẩu NaOH ngoài không
khí, sau vài ngày thấy có chất rắn màu
trắng phủ ngoài. Nếu nhỏ vài giọt dd HCl
vào chất rắn thấy có khí thoát ra, khí này
làm đục vôi trong. Chất rắn màu trắng là
sản phẩm phản ứng của NaOH với:
a) O2 trong không khí
b) Hơi H2O trong không khí
c) CO2 và O2 trong không khí
d) CO2 và hơi H2O trong không khí
e) CO2 trong không khí
Giải thích và viết PTHH
NaOH
CO2
+CO2
Narắn
Chất
trắng
2COmàu
3
dd HCl
CO2
Bµi 5 : Trung hoµ 300 ml dung dÞch Ca(OH)2 1M b»ng 200ml dung
dÞch HCl 0,2M.
a) TÝnh khèi lîng muèi t¹o thµnh.
b) TÝnh nång ®é mol cña dung dÞch t¹o thµnh sau ph¶n øng (coi thÓ
tÝch dung dÞch kh«ng thay ®æi).
=> Các bớc tiến hành để giải bài toán theo PTHH khi có thể tính đợc
số mol của hai chất tham gia phản ứng:
B1: Đổi tất cả các dữ kiện đề bài ra số mol.
B2: Viết PTHH.
So sánh tỉ lệ số mol
=> Chất nào d, chất nào hết.
B3: Tính tất cả các yêu cầu đề bài theo số mol chất hết.
Gợi ý bài 3:
Đề bài : Trộn một dung dịch có hoà tan 0,2 mol CuCl2 với một dung dịch
có hoà tan 20g NaOH. Lọc hỗn hợp các chất sau phản ứng thu đợc kết
tủa và nớc lọc. Nung kết tủa đến khi khối lợng không đổi.
a. Viết các phơng trình hoá học.
b. Tính khối lợng chất rắn thu đợc sau khi nung.
c. Tính khối lợng các chất tan có trong nớc lọc.
Hớng dẫn :
-Đổi mNaOH ra nNaOH
-Viết PTHH : CuCl2 + 2NaOH Cu(OH)2 + 2NaCl
(1)
Cu(OH)2 CuO + H2O
( 2)
-So sánh tỉ lệ số mol suy ra chất hết,chất d. Tính toán yêu cầu theo
chất hết.
-Theo PTHH suy ra: chất rắn là gì?
- Chất rắn là: Cu(OH)2
-Nớc lọc gồm những chất gì ?
- Nớc lọc gồm: NaCl, chất còn d trong phơng trình số (1)