Bai 13 Luyen tap chuong 1 Cac loai hop chat vo co
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (214.74 KB, 12 trang )
Luyện tập các hợp chất vô cơ
I – Kiến thức cần nhớ
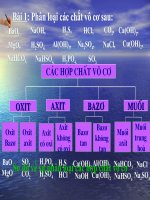
1. Phân loại các hợp chất vơ cơ
2. Tính chất của các hợp chất vô cơ
13
3
1
BaO
K2 O
6
2
4
P2O5
HNO3
SO3
H2SO4
9
5
HCl
H2S
7
NaOH
12
8
Cu(OH)2
Ba(OH)2 Fe(OH)3
10
11
NaHSO4 Na2SO4
Ba(HCO3)2 K2SO4
Các hợp chất vơ cơ
Oxit
Axit
Bazơ
Oxit
Bazơ
Oxit
axit
Axit
có oxi
Axit
Khơng
có oxi
BaO
P2O5
HNO3
HCl
SO3
H2SO4
K2 O
H2S
Bazơ
tan
NaOH
Ba(OH)2
Muối
Bazơ
khơng
tan
Cu(OH)2
Fe(OH)3
Muối
axit
Muối
trung
hịa
NaHSO4
Na2SO4
Ba(HCO3)2
K2SO4
2. Tính chất hóa học của các hợp chất vơ cơ
Hãy chọn những chất thích hợp vào dấu chấm
2. Bazơ
1. Oxit
a) Oxit bazơ +Nước
….
Bazơ
Axit
a) Bazơ + ……..
Muối + nước
Oxit axit
Muối + Nước b) Bazơ + ……..
Muối
c) Bazơ + ……..
Axit
Axit
b) Oxit bazơ + …..
Nước
c) Oxit axit + ……
d) Oxit axit +Bazơ
…. (dd)
Muối + nước
Muối + Bazơ
Muối + Nước
e) Oxi bazơ + Oxit axit
Muối
4. Muối
3. Axit
Kim loại
a) Axit + ……
muối + hidro
Bazơ
b) Axit + ……
muối + nước
Oxi bazơ
c) Axit + ……
muối + nước
d) Axit + ……
Muối
muôi + axit
Axit
a) Muối + ……..
Axit + Muối mới
Bazơ
b) Muối + ……..
Muối + bazơ
Muối
c) Muối + ……..
Muối + muối
loại
d) Muối + Kim
……..
e) Muối
t0
Muối + kim loại
Nhiều chất mới
……..+ …….
2. Tính chất hóa học của các hợp chất vơ cơ
Mối liên hệ giữa các hợp chất vô cơ
Oxit bazơ
+ Bazơ
+ Oxit bazơ
+ Axit
(3)
+ Oxit axit
(1)
+ Nước
(4)
(2)
Nhiệt
phân
hủy
(bazơ
không
tan)
(9)
Muối
+ Nước
(5)
+ Bazơ
(6)
+ Axit
+ Oxit axit
+ Muối
Bazơ
Oxit axit
(8)
(7)
+ Kim loại
+ Axit
+ Bazơ
+ Oxit bazơ
+ Muối
Axit
Chú thích: Ngồi những tính chất của muối được trình
bày trong sơ đồ, muối cịn có những tính chất sau.
- Muối có thể tác dụng với muối sinh ra hai muối mới
- Muối có thể tác dụng với kim loại sinh ra kim loại mới
và muối mới
- Muối có thể bị nhiệt phân hủy sinh ra nhiều chất mới
Ví dụ :
t0
CaCO3 → CaO + CO2
t0
2 KClO3 → 2 KCl + O2
t0
Ca(HCO3 )2→ CaCO3 + CO2 + H2O
II. Bài tập
1.Cho các chất sau: Mg(OH)2, K2SO4, HCl, NaOH, P2O5, CaO
- Chất nào tác dụng được với dung dịch KOH?
Đáp án: HCl, P2O5.
2. Cho các chất sau: Mg(OH)2, K2SO4, HCl, NaOH, P2O5, CaO
- Chất nào tác dụng được với axit H2SO4?
Đáp án: CaO, Mg(OH)2, NaOH.
3. Cho các chất sau: Mg(OH)2, K2SO4, HCl, NaOH, P2O5, CaO
- Chất nào tác dụng được với dung dịch BaCl2 ?
Đáp án: K2SO4
II. Bài tập
4.
Bằng phương pháp hóa học hãy nhận biết dung dịch mất nhãn
sau:
H2SO4, HCl , Na2SO4 , NaOH
Bài giải
H2SO4 , HCl, Na2SO4 , NaOH
+ Qùy tím
Màu đỏ
H2SO4 ., HCl
+ Dung dịch Ba(OH)2
Có kết
tủa
H2SO4
Khơng có kết tủa
HCl
Màu xanh
NaOH
Khơng đổi màu
Na2SO4
II. Bài tập
5. 200ml dung dịch HCl có nồng độ 3,5mol/lit hòa tan vừa đủ 20g hỗn hợp CuO và
Fe2O3.
a) Viết các phương trình phản ứng hóa học.
b) Tính khối lượng của mỗi oxit bazơ có trong hỗn hợp ban đầu.
Bài giải
VHCl = 200ml = 0,2 lít ;
nHCl = 3,5 x 0,2 = 0,7 mol.
- Gọi x, y lần lượt là số mol của CuO và Fe2O3 (điều kiện x,y > 0)
a) Phương trình phản ứng hóa học
CuO + 2 HCl
CuCl2 +
x
2x
Fe2O3
y
+ 6 HCl
6y
2 FeCl
3
H2O
+ 3H2O
b) Từ phương trình phản ứng trên ta có:
nHCl = 2x + 6y = 0,7 mol (1)
Theo bài: mhỗn hợp = mCuO + mFe2O3
= (64 + 16).x + (56.2 + 16.3).y
=80x + 160y = 20g (2)
Cách 1: Từ phương trình (1) và (2) ta có hệ phương trình sau:
x =......
2x + 6y = 0,7
⇒
80x + 160y = 20 y = ....
Cách 2: Từ phương trình (2)⇒ x + 2y = 0,25 ⇒ x = 0,25 – 2y (3)
Thay x vào (1) ta được: 2(0,25 – 2y) + 6y = 0,7
⇒ 0,5 - 4y + 6y = 0,7 ⇒ 2y = 0,2 ⇒ y = 0,1 mol
Thay y vào (3) ta được: x = 0,25 - 2.0,1 = 0,05 mol
⇒ mCuO =
mFe2O3 =
0,05 x 80 = 4g
0,1 x 160 = 16g
III. Bài tập về nhà
- Ơn lại tồn bộ kiến thức chương 1
- Viết phương trình phản ứng bài tập 1, 2, 3, 4
- Bài tập bổ sung:
Bài 6: Hoà tan 4,88g hỗn hợp A gồm MgO và FeO trong 200ml dung
dịch H2SO4 0,45M(lỗng) thì phản ứng vừa đủ.
a/ Viết pương trình phản ứng hóa học xảy ra.
b/ Tính khối lượng mỗi oxit có trong hỗn hợp A.
Bài 7: Khử 2,4g hỗn hợp gồm CuO và Fe2O3 bằng H2 ở nhiệt độ cao
thì thu được 1,76g hỗn hợp 2 kim loại. Đem hỗn hợp 2 kim loại hoà
tan bằng dd axit HCl thì thu được V(lit) khí H2.
a/ Xác định % về khối lượng của mỗi oxit trong hỗn hợp.