Les troubles de l’intégration visuelle - part 3 docx
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (718.22 KB, 19 trang )
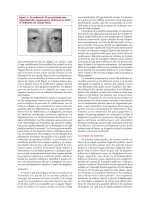
Cas n° 2 — Une mélanose acquise primaire (MAP) avec atypie
Figure 4 : Coloration à l’hématoxyline-éosine
de la biopsie-exérèse d’une lésion située dans
le limbe
Figure 3 : Lésion pigmentaire à la position « 12
heures »
La flèche pointe des mélanocytes atypiques.
La calibration indique 125 µm. (encadré)
Une femme blanche âgée de 37 ans présente
4 lésions brun doré dans la conjonctive bulbaire
de son œil gauche. Ces lésions sont une source
de préoccupations parce qu’elles ont changé au
cours d’une période de plusieurs années. On
effectue plusieurs biopsies-exérèses, et les spéci-
mens sont soumis à un examen pathologique. La
figure 3 montre une lésion pigmentaire à la posi-
tion « 12 heures ».
La figure 4, sur coloration à l’hématoxyline-
éosine, montre la biopsie-exérèse d’une lésion
située dans le limbe, à la position « 12 heures »;
on y voit l’épithélium conjonctival (flèche) et la
substantia propria. L’épithélium conjonctival
présente un épaississement de la membrane
basale et des nids de mélanocytes atypiques
(sous la flèche), ainsi que les manifestations d’un
rapport noyau/cytoplasme élevé et un manque
de cohésion (voir la microphotographie à fort
grossissement, dans l’encadré). On n’observe pas
d’invasion franche de la substantia propria. Des
données similaires ont été notées pour toutes les
autres lésions excisées, et les marges de résection
ont montré une conjonctive normale. Selon le
diagnostic pathologique, il s’agit d’une mélanose
acquise primaire (MAP) avec atypie.
Commentaire : La MAP avec atypie a un
potentiel de malignité et se présente habituelle-
ment sous la forme d’une lésion unilatérale plate
et d’un brun irrégulier chez des patients blancs
âgés ou d’âge moyen. On doit la distinguer de la
MAP sans atypie, et l’examen histopathologique
est donc nécessaire
5
. La MAP sans atypie est une
affection bénigne caractérisée par la présence de
pigments de mélanine dans la conjonctive avec
ou sans épaississement de mélanocytes cyto-
logiquement bénins. Les lésions désignées
comme étant des MAP sans atypie n’ont pas
évolué vers un mélanome
5
. La MAP avec atypie
se caractérise par des mélanocytes conjonctivaux
cytologiquement atypiques. Une étude des
lésions classées comme des MAP avec atypie a
démontré que 46 % d’entre elles évoluent
jusqu’au mélanome
5
. La présence de mélanocytes
atypiques dans l’épithélium n’importe où ailleurs
que dans la couche basale de l’épithélium est
associée à une évolution vers un mélanome dans
90 % des cas, alors que la présence de mélano-
cytes atypiques intraépithéliaux avec cytoplasme
abondant (cellules épithélioïdes) est associée
à une évolution vers un mélanome dans 75 %
des cas
5
. Le taux de récidive de la MAP avec
atypie est d’approximativement 60 %, et il est
relié à une exérèse incomplète ou à une atteinte
de la cornée
5
.
Ophtalmologie
Conférences Scientifiques
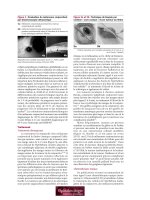
Figure 5 : Lésion bulbaire temporale
pigmentaire s’étendant à la cornée
Figure 6 : Coloration à l’hématoxyline-
éosine d’une section du limbe et de la
cornée
Une femme âgée de 70 ans présente à
l’œil droit une lésion conjonctivale pigmen-
taire, bulbaire temporale récurrente. Onze
mois plus tôt, la lésion a déjà été réséquée
du limbe inféro-temporal, et le diagnostic
pathologique a alors été un mélanome nodu-
laire. La lésion récurrente atteint à présent la
cornée à partir du limbe et mesure 3 x 2,5
mm (figure 5). On pratique l’exentération
de l’œil droit et on demande un examen
pathologique du spécimen.
La coloration à l’hématoxyline-éosine
(figure 6) montre le limbe à gauche, et le
centre de la cornée à droite. À partir du
limbe, la tumeur (T) envahit la cornée péri-
phérique et la substantia propria superficielle
et intermédiaire. Le tissu cicatriciel (S) corres-
pond au site de la résection antérieure et à la
membrane de Bowman qui a été altérée
(pointe de flèche). La flèche pointe la mem-
brane de Descemet, ce qui signifie que l’on
voit une section de cornée de pleine épais-
seur. On note l’absence de cellule tumorale
dans l’épithélium. Selon le diagnostic patho-
logique, il s’agit d’un mélanome conjonctival
malin récurrent, avec envahissement de la
cornée.
La microphotographie à fort grossisse-
ment (figure 7) montre les cellules du méla-
nome malin, qui sont en feuillets. On peut
voir les noyaux ovoïdes avec cytoplasme
éosinophile; plusieurs des cellules tumorales
présentent des nucléoles proéminents. On
note aussi la présence de rares dépôts de
pigments de mélanine (pointes de flèche).
Commentaire : Le mélanome conjonctival
est rare, mais il est associé à un taux de
mortalité d’environ 30 %. Selon des études
démographiques réalisées dans les pays occi-
dentaux, l’incidence annuelle du mélanome
conjonctival atteint 0,02 à 0,05 cas par
100 000, et touche autant les hommes que
les femmes
6
. Jusqu’à 75 % des cas de
mélanomes conjonctivaux sont associés à la
MAP, alors que jusqu’à 20 % des cas de
mélanomes sont associés à des nævi conjonc-
tivaux
7
. Les mélanomes conjonctivaux
migrent souvent par les vaisseaux lympha-
tiques jusqu’aux ganglions lymphatiques les
plus proches, où l’examen histopathologique
révèle souvent la présence de métastases
8-12
.
Ceci contraste avec les mélanomes du tractus
uvéal, qui migrent par la voie hématogène,
de préférence vers le foie.
Suite à la page 5
Cas n° 3 — Un mélanome conjonctival malin
T
S
T = tumeur du limbe S = tissu cicatriciel
Pointe de flèche = membrane de Bowman altérée
Flèche = membrane de Descemet
La calibration indique 250 µm.
Conclusion
Les renseignements cliniques pertinents au
sujet des lésions, tels que le nombre de lésions,
leur localisation, leur pré-existence, leur taille,
leur couleur et tout changement documenté,
aident le pathologiste à poser un diagnostic
pathologique. Ces cas de lésions conjonctivales
illustrent l’importance de la relation entre le
pathologiste et le chirurgien-ophtalmologiste
pour le traitement des patients qui présentent des
lésions apparemment inoffensives, et pour
prévenir des conséquences potentiellement
dévastatrices.
Références
1. Shields JA, Shields CL. Tumors and pseudotumours of the
conjunctiva. In: Atlas of Eyelid and Conjunctival Tumors.
Philadelphia, PA: Lippincott Williams & Wilkins Co.;
1999:199-334.
2. Myles M, Brownstein S. Cystic subepithelial nevus of the
caruncle. Ophthalmic Practice 1990;8:160-162.
3. Folberg R, Jakobiec FA, Bernardino VB, Iwamoto T. Benign
conjunctival melanocytic lesions. Clinicopathologic
features. Ophthalmology 1989;96(4):436-61.
4. Luxenberg MN. Compound nevus of the conjunctiva. Arch
Ophthalmol 1986;104(12):1842.
5. Folberg R, McLean IW, Zimmerman LE. Primary acquired
melanosis of the conjunctiva. Hum Pathol 1985;16(2):129-
35.
6. Seregard S. Conjunctival melanoma. Surv Ophthalmol 1998;
42(4):321-50.
7. F olberg R, McLean IW, Zimmerman LE. Malignant
melanoma of the conjunctiva. Hum Pathol 1985;16(2):
136-43.
8. Paridaens AD, Minassian DC, McCartney AC, Hungerford JL.
Prognostic factors in primary malignant melanoma of the
conjunctiva: a clinicopathological study of 256 cases. Br J
Ophthalmol 1994;78(4):252-9.
9. Norregaard JC, Gerner N, Jensen OA, Prause JU. Malignant
melanoma of the conjunctiva: occurrence and survival fol-
lowing surgery and radiotherapy in a Danish population.
Graefes Arch Clin Exp Ophthalmol 1996;234(9):569-72.
10. Seregard S, Kock E. Conjunctival malignant melanoma in
Sweden 1969-91. Acta Ophthalmol (Copenh) 1992;70(3):
289-96.
11. Esmaeli B, Wang X, Youssef A, Gershenwald JE. Patterns of
regional and distant metastasis in patients with conjunctival
melanoma: experience at a cancer center over four decades.
Ophthalmology 2001;108(11):2101-5.
12. Shields CL, Shields JA, Gunduz K, et al. Conjunctival
melanoma: risk factors for recurrence, exenteration, metas-
tasis, and death in 150 consecutive patients. Arch Ophthal-
mol 2000;118(11):1497-507.
13. De Potter P, Shields CL, Shields JA, Menduke H. Clinical pre-
dictive factors for development of recurrence and metastasis
in conjunctival melanoma: a review of 68 cases. Br J Oph-
thalmol 1993;77(10):624-30.
14. Stefani FH. A prognostic index for patients with malignant
melanoma of the conjunctiva. Graefes Arch Clin Exp
Ophthalmol 1986;224(6):580-2.
15. Benderitter T, Berard M, Bonerandi JJ, Lebreuil G. [Melanic
proliferations of the conjunctiva. Histopathologic study of a
series of 40 cases]. J Fr Ophtalmol 1985;8(5):411-22.
16.Crawford JB. Conjunctival melanomas: prognostic factors a
review and an analysis of a series. Trans Am Ophthalmol Soc
1980;78:467-502.
Ophtalmologie
Conférences Scientifiques
Cas n° 3
(suite)
Figure 7 : Microphotographie des
cellules d’un mélanome malin
Lors de la surveillance d’un patient
atteint d’un mélanome conjonctival après
le traitement primaire, il ne faut pas oublier
que les récidives locales sont fréquentes et
qu’elles surviennent chez plus de 50 % des
patients. Les récidives sont habituellement
évidentes dans les premiers cinq ans après
l’épisode initial
13
. Il est indiqué d’exercer un
suivi attentif, puisqu’approximativement
30 % des patients présenteront des métas-
tases aux ganglions lymphatiques
10
.
Les prédicteurs cliniques d’un mauvais
pronostic comprennent une atteinte de la
conjonctive aux marges des paupières, une
atteinte de la conjonctive palpébrale, du
fornix, du pli et de la caroncule, ainsi
qu’une distribution multifocale. Les pré-
dicteurs pathologiques d’une aggravation
du pronostic comprennent la présence de
mélanocytes atypiques intraépithéliaux
(une migration pagétoïde)
7
, ou un diagnos-
tic de tumeur à cellules mixtes (cellules
épithélioïdes et fusiformes)
8
. Des signes
histologiques d’un envahissement lym-
phatique sont associés à un taux de morta-
lité quatre fois plus grand, comparativement
aux patients dont le système lympha-
tique n’est pas atteint
8
. L’augmentation de
l’épaisseur de la tumeur
7, 8
et de l’activité
mitotique
7,10,14-16
est également un prédic-
teur d’un pronostic moins favorable.
Pointes de flèche : de rares dépôts de pigments de
mélanine
La calibration indique 25 µm.
Événements à venir au
Département d’ophtalmologie
22 avril 2004
PPI – D
r
Donald Fletcher, Birmingham, Alabama
Advances in Low Vision Rehabilitation
29 avril 2004
PPI – D
r
Douglas Coster, Australie
Development in corneal therapeutics
6 mai 2004
PPI – Dr Kathleen Digre, Salt Lake City, Utah
Neuro-ophthalmic changes in pregnancy
13 mai 2004
PPI – Dr Shaun Singer, Toronto, Ontario
Quality Assurance Rounds
20 mai 2004
PPI – Dr David Apple, Charleston, Caroline du Nord
U of T & TOS Combined Rounds
27 mai 2004
PPI – D. Marian Macsai, Glenview, Illinois
Refractory blepharomeibomitis – The bread & butter
of your clinical practice
Note : Programme à l’intention des professeurs invités (PPI)
Adresse du centre : Toronto Western Hospital,
Aile Ouest, Salle 2-401, 399 Bathurst Street, Toronto
Réunions scientifiques à venir
4 au 5 juin 2004
Age-related Macular Degeneration Update 2004
Baltimore, Maryland
Renseignements : Tél. : 410-955-5880
Courriel :
16 au 19 juin 2004
Canadian Ophthalmological Society Annual Meeting
Vancouver, Colombie-Britannique
Renseignements :
Site web : www.eyesite.ca
Résumés d’intérêt connexe
Les tumeurs de la conjonctive et de la cornée
S HIELDS CL, SHIELDS JA; PHILADELPHIE, PA
Dans cet article, les auteurs présentent une révision des tumeurs de la
conjonctive et de la cornée, qui constituent un spectre de tumeurs
nombreuses et variées. On regroupe ces tumeurs en deux grandes
catégories : les lésions congénitales et acquises. Les lésions acquises se
divisent quant à elles en plusieurs catégories, selon l’origine de la
masse : ce sont les tumeurs épithéliales de surface, mélanocytaires,
vasculaires, fibreuses, neurales, histiocytaires, myxoïdes, myogènes,
lipomateuses, lymphoïdes, leucémiques, métastatiques et secondaires.
Les lésions mélanocytaires comprennent le nævus, la mélanose d’ori-
gine ethnique, la mélanose acquise primaire, le mélanome et d’autres
affections de la surface oculaire comme la mélanocytose oculaire et
le dépôt pigmentaire secondaire. Les lésions néoplasiques non
mélanocytaires les plus fréquentes comprennent l’épithélioma spino-
cellulaire et le lymphome, qui ont tous deux des manifestations qui
peuvent être décelées lors de l’examen clinique. La caroncule est
touchée par une gamme de tumeurs légèrement différente de celle
qui touche le reste de la conjonctive; si le nævus et le papillome sont
les plus fréquentes tumeurs touchant la caroncule, cette dernière peut
aussi présenter un oncocytome et une hyperplasie des glandes
sébacées, un adénome ou un carcinome. Les auteurs donnent une
description et une illustration clinique des nombreuses tumeurs de la
conjonctive et de la cornée, et ils discutent du traitement des tumeurs.
Surv Ophthalmol 2004;49:3-24.
Le nævus conjonctival : manifestations cliniques et
évolution naturelle chez 410 patients consécutifs
S HIELDS CL, FASIUDDEN, A, MASHAYEKHI A,
SHIELDS JA; PHILADELPHIE, PA
Cette étude rétrospective avait pour but de décrire les manifestations
cliniques d’un nævus conjonctival et d’évaluer les changements de
couleur et de taille du nævus dans le temps. Les deux principaux
critères d’évaluation ont été les changements de couleur et de taille.
Les nævi étaient bruns dans 65 % des cas, ocre dans 19 % des cas et
complètement dénués de pigments dans 16 % des cas. Les nævi
étaient situés sur la conjonctive bulbaire dans 72 % des cas, sur la
caroncule dans 15 % des cas, sur le pli semi-lunaire dans 11 % des
cas, sur le fornix dans 1 % des cas, sur le tarse dans 1 % des cas et sur
la cornée dans <1 % des cas. Les lésions de la conjonctive bulbaire
étaient le plus souvent contiguës au limbe cornéo-scléral. Le nævus
se trouvait dans le quadrant temporal (46 % des cas), nasal (44 % des
cas), supérieur (6 % des cas) et inférieur (5 % des cas). Les autres
manifestations comprenaient des kystes intralésionnels (65 % des
cas), des vaisseaux nourriciers (33 % des cas) et des vaisseaux intrin-
sèques visibles (38 % des cas). Des kystes ont été décelés lors de
l’examen clinique dans 70 % des cas de nævus mixte, 58 % des cas
de nævus sous-épithélial, 40 % des cas de nævus jonctionnel, et 0 %
des cas de nævus bleu confirmés par l’histopathologie.
Chez 149 patients qui ont subi des examens périodiques pendant
une moyenne de 11 ans, la couleur de la lésion est graduellement
devenue plus foncée chez 5 % des patients (7 patients), plus pâle
chez 8 % des patients (12 patients) et est restée la même chez 87 %
des patients (130 patients). La taille de la lésion a augmenté chez 7 %
des patients (10 patients), a semblé diminuer chez 1 % des patients (1
patient) et est restée la même chez 92 % des patients (137 patients).
Chez trois patients, un mélanome malin s’est développé à partir d’un
nævus mixte (deux cas) ou d’un nævus bleu (un cas) préexistants sur
un intervalle moyen de 7 ans. Les auteurs ont conclu que le nævus
conjonctival est une tumeur bénigne le plus souvent située dans le
limbe nasal ou temporal et rarement au niveau du fornix, du tarse ou
de la cornée. Avec le temps, un changement de la couleur de la
tumeur a été décelé dans 13 % des cas (20/149), et un changement
de la taille de la tumeur a été décelé dans 8 % des cas (12/149).
Arch Ophthalmol 2004;122:167-175.
© 2004 Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto, seul responsable du contenu de cette publication. Édition : SNELL Communication
Médicale Inc. avec la collaboration du Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto.
MD
Ophtalmologie – Conférences scientifiques est une marque
de commerce de SNELL Communication Médicale Inc.Tous droits réservés. L’administration d’un traitement thérapeutique décrit ou mentionné dans Ophtalmologie – Conférences scientifiques doit
toujours être conforme aux renseignements d’ordonnance approuvés au Canada. SNELL Communication Médicale se consacre à l’avancement de l’éducation médicale continue de niveau supérieur.
L’élaboration de cette publication a bénéficié d’une subvention à l’éducation de
Novartis Ophthalmics
130-006F
La version française a été révisée par le professeur Pierre Lachapelle,
Montréal.
Les avis de changement d’adresse et les demandes d’abonne-
ment pour Ophtalmologie – Conférences Scientifiques doivent
être envoyés par la poste à l’adresse C.P. 310, Succursale H,
Montréal (Québec) H3G 2K8 ou par fax au (514) 932-5114 ou
par courrier électronique à l’adresse
Veuillez vous référer au bulletin Ophtalmologie – Conférences
Scientifiques dans votre correspondence. Les envois non
distribuables doivent être envoyés à l’adresse ci-dessus.
Poste-publications #40032303
SNELL
Ophtalmologie
Confộrences scientifiques
AVRIL 2004
Volume 2, numộro 4
COMPTE RENDU DES CONFẫRENCES
SCIENTIFIQUES DU DẫPARTEMENT
DOPHTALMOLOGIE ET
DES SCIENCES DE LA VISION,
FACULTẫ DE MẫDECINE,
UNIVERSITẫ DE TORONTO
Dộpartement dophtalmologie
et des sciences de la vision
Facultộ de mộdecine
Universitộ de Toronto
60 Murray St.
Bureau 1-003
Toronto (Ontario) M5G 1X5
Le contenu rộdactionnel dOphtalmologie
Confộrences scientiques est dộterminộ
exclusivement par le Dộpartement
dophtalmologie et des sciences de la vision,
Facultộ de mộdicine, Universitộ de Toronto.
Dộpartement dophtalmologie
et des sciences de la vision
Jeffrey Jay Hurwitz, M.D., Rộdacteur
Professeur et prộsident
Martin Steinbach, Ph.D.
Directeur de la recherche
The Hospital for Sick Children
Elise Heon, M.D.
Ophtalmologiste en chef
Mount Sinai Hospital
Jeffrey J. Hurwitz, M.D.
Ophtalmologiste en chef
Princess Margaret Hospital
(Clinique des tumeurs oculaires)
E. Rand Simpson, M.D.
Directeur, Service doncologie oculaire
St. Michaels Hospital
Alan Berger, M.D.
Ophtalmologiste en chef
Sunnybrook and Womens College
Health Sciences Centre
William S. Dixon, M.D.
Ophtalmologiste en chef
The Toronto Hospital
(Toronto Western Division and
Toronto General Division)
Robert G. Devenyi, M.D.
Ophtalmologiste en chef
Techniques de la phacoộmulsication
et innovations
PAR
ROSA BRAGA
-MELE, M.ED
, MD, FRCSC
La chirurgie de la cataracte et les techniques de la phacoộmulsification ont
ộvoluộ considộrablement au cours des 10 derniốres annộes. La tendance est une
chirurgie moins traumatique en utilisant la phaco-aspiration par ultrasons au lieu
de la phacoộmulsication par le vide. Grõce aux progrốs rộcents effectuộs dans la
modulation de la puissance, la plupart des chirurgiens ont recours des techniques
utilisant une ộnergie de phacoộmulsication moindre, rộduisant ainsi lộnergie
thermique utilisộe dans lil et les lộsions oculaires
1,2
. Une telle rộduction est possi-
ble en utilisant des forces mộcaniques pour fragmenter le noyau, un niveau de vide
plus ộlevộ pour aspirer les fragments ou une association des deux. Dans ce numộro
dOphtalmologie Confộrences scientifiques, nous dộcrivons les techniques de
phacoộmulsication ô par dộcoupage rapide ằ et de phacoộmulsication micro-
incisionnelle bimanuelle qui visent simplier chaque ộtape de la chirurgie de la
cataracte, an de minimiser le traumatisme et obtenir un rộsultat optimal.
La technique de phacoộmulsication par ô dộcoupage rapide ằ
Le chirurgien spộcialisộ dans la cataracte peut rencontrer de nombreux scộnarios
qui posent un dộ lorsquil effectue une chirurgie par phacoộmulsication. Il est impor-
tant de savoir quoi sattendre lorsque lon fait face un cas difcile et de prộparer un
plan pour faciliter la chirurgie. Bien que la plupart des chirurgiens soient trốs laise
avec une technique en particulier, il est essentiel quils fassent preuve de souplesse et
utilisent des techniques diffộrentes selon la situation. Lộvaluation prộopộratoire du
patient et la dộtermination du type de cataracte et de la morphologie de lil (p. ex.
longueur axiale, instabilitộ zonulaire, cataracte post-traumatique, post-chirurgicale)
peuvent aider dộterminer comment procộder avec le cas.
Le traitement prộopộratoire avec des mộdicaments topiques peut rendre lộvolution
peropộratoire et postopộratoire plus prộvisible. Les anti-inammatoires non stộroùdiens
(AINS) topiques sont utiles pour maintenir la mydriase peropộratoire et pour maợtriser
linflammation postopộratoire, rộduisant ainsi la nộcessitộ dutiliser des stộroùdes
topiques long terme. Les AINS aident ộgalement prộvenir ldốme maculaire
chronique
3
. Les AINS prộopộratoires peuvent ờtre administrộs 4 fois par jour, en com-
menỗant le jour avant lopộration et en continuant le traitement immộdiatement aprốs
lopộration pendant un mois. Lutilisation dantibiotiques prộopộratoires, tels que les
uoroquinolones, peut ộgalement aider prộvenir les infections postopộratoires. Les
uoroquinolones peuvent ờtre amorcộes un jour avant la chirurgie et le traitement peut
ờtre poursuivi pendant 2 semaines aprốs lopộration conjointement des stộroùdes sous
forme de collyre.
La chirurgie est rộalisộe en utilisant une approche temporale oự la cornộe est trans-
parente. La tộtracaùne topique fournit gộnộralement une anesthộsie satisfaisante.
MC
Dộpartement
dophtalmologie et des
sciences de la vision
FACULTY OF MEDICINE
University of Toronto
Disponible sur Internet :
www.ophtalmologieconferences.ca
Cependant, si l’on prévoit la manipulation de l’iris ou
si le patient est particulièrement sensible, de la lido-
caïne à 1 %, sans agent de conservation, peut être
injectée dans la chambre antérieure au début de l’in-
tervention. Une incision latérale est effectuée sur la
gauche avec une lame métallique à 15
o
. La chambre
antérieure est ensuite remplie d’une substance visco-
élastique (p. ex. une substance viscoélastique cohé-
sive telle que Amvisc Plus
®
, Bausch and Lomb,
Rochester, NY), qui assure une stabilité maximale de
la chambre et de l’iris. Cependant, en présence de
lésion corné-enne, la technique d’Arshinoff
4
est
préférable, utili-sant une substance viscoélastique
plus dispersive (p. ex. Viscoat
®
Alcon, Fort Worth,
Texas) comme revêtement de l’endothélium cornéen.
Avec la technique d’Arshinoff, la substance viscoélas-
tique dispersive est injectée initialement pour rem-
plir environ la moitié de la chambre antérieure,
suivie d’une substance viscoélastique cohésive qui
forcera la substance dispersive à remonter contre la
cornée. Si l’œil a une chambre antérieure peu pro-
fonde ou si la pupille est petite, une des nouvelles
substances viscoadaptatives (p. ex. Healon 5, Ivisc
phaco) peut aider à approfondir la chambre
antérieure et à étirer la pupille en raison de sa capa-
cité à mieux conserver un espace donné. Une inci-
sion de la cornée transparente temporale, mesurant
2 mm de long, peut ensuite être réalisée au moyen
d’une lame métallique de 2,65 mm.
Un capsulorhexis circulaire continu est réalisé au
moyen d’une pince à capsulorhexis Utrata tout en
maintenant l’œil au niveau de l’orifice latéral au
moyen d’une pince de 0,12. On utilise ensuite la
technique de Fine d’hydrodissection par clivage
cortical
5
dans laquelle une canule de Gimbel est
introduite au-dessous du bord de la capsule, la
soulevant initialement, puis injectant un petit bolus
de liquide. La rotation du cristallin dans le sac capsu-
laire est toujours évaluée avant de commencer la
phacoémulsification.
En ce qui concerne la phacoémulsification, il est
important de comprendre la dynamique des fluides
associée à la machine utilisée pour mieux prédire la
progression de la chirurgie. La technique de phaco-
émulsification par découpage rapide a été introduite
pour la première fois par Nagahara. Avec cette tech-
nique, une aiguille biseautée de phacoémulsification
de calibre 30 est introduite dans l’œil avec le côté
biseauté vers le bas. Il est important de rétracter le
manchon de silicone pour exposer davantage l’aiguille
métallique, afin de maximiser la profondeur de l’inci-
sion lorsqu’on utilise la technique de découpage
rapide. Un couteau de Koch (Storz, St. Louis, MO) est
ensuite placé à proximité du centre du noyau (figure
1). Le côté biseauté placé vers le haut, l’aiguille de
phacoémulisification pénètre profondément dans la
partie centrale du noyau en salves de 100 msec à
20 % de puissance. La modulation de la puissance en
salves utilise un pourcentage fixe de puissance en
mode salves utilise d’un intervalle programmé (durée
de la puissance) et un intervalle linéaire entre les
salves . Le noyau est initialement transpercé au
moyen d’un débit plus faible et dans un milieu sous
vide qui est ensuite augmenté lorsque celui-ci est
maintenu en place. Au même moment, le couteau est
placé juste devant ou sur le côté de l’aiguille de pha-
coémulsification introduite dans le noyau (figure 1).
Une pression sur l’extrémité distale du couteau est
exercée vers le bas et vers la gauche alors que l’aigu-
ille de phacoémulsification est déplacée légèrement
vers le haut et vers la droite (figure 2). Le couteau
doit être dirigé sur le côté de l’aiguille de façon à
assurer l’occlusion de l’extrémité de l’aiguille sur le
fragment de noyau. Le couteau et l’extrémité de
l’aiguille sont ensuite séparés latéralement pour
assurer que le plan de clivage se propage entière-
ment d’une extrémité du noyau à l’autre et à travers
la plaque postérieure, qui est une partie plus épaisse
de l’épinoyau présente dans les cataractes plus
denses. Il est important de vérifier que la segmenta-
tion soit complètement propagée avant de procéder
à l’étape suivante.
On effectue ensuite la rotation du noyau et l’on
introduit à nouveau l’extrémité de l’aiguille le côté
biseauté vers le côté (afin de permettre un aligne-
ment parallèle et une couverture maximale du
noyau) et le découpage vertical vers le bas est répété.
Le segment du noyau qui a été découpé est ensuite
extrait de l’espace supracapsulaire avec l’aiguille de
Figure 1 : Position initiale pour le découpage
rapide vertical
hydratée et l’on vérifie son intégrité et son
étanchéité.
Chirurgie de la cataracte
microincisionnelle bimanuelle
Les progrès technologiques ont permis des
améliorations passionnantes dans les techniques
de la chirurgie de la cataracte. C’est un domaine en
rapide évolution et les chirurgiens recherchent tou-
jours des moyens de réaliser l’intervention la moins
traumatique possible en réduisant la puissance de
l’énergie thermique utilisée dans l’œil, en diminuant
la dimension de l’incision ou en réduisant le trauma-
tisme de la cornée, favorisant ainsi une récupération
visuelle plus rapide. Les améliorations de la modula-
tion
1
et du contrôle de la puissance ont permis de
réduire la quantité totale d’énergie ultrasonique utili-
sée dans l’œil et par conséquent, ont diminué le
risque de lésions de l’endothélium de la cornée et de
la région de l’incision.
L’utilisation de salves d’activité électrique est l’un
des progrès les plus récents. En raison des salves
plus courtes de puissance de phacoémulsification,
suivies d’intervalles linéaires où seul le vide permet
de retirer les fragments, cette modalité améliore cer-
tainement la phacoaspiration ultrasonique, car elle
minimise l’énergie ultrasonique dans l’œil et maxi-
mise l’aspiration des fragments de noyau. Lorsqu’elle
est utilisée conjointement au double contrôle
linéaire du vide, cette technique est idéale avec la
technique de découpage rapide, car elle permet un
découpage plus efficace et un meilleur suivi de la
profondeur. Une étude récente
2,8
a examiné la durée
absolue de la phacoémulsification en comparant le
mode en salves (160 msec) et le mode pulsé (5 pps),
avec un niveau de vide réglé par un contrôle linéaire
à 180-325 mm Hg et la hauteur du flacon à 120 cm.
Chaque groupe de 25 patients présentait une
sclérose de 2+ ou 3+ (classification de Wilmer) et
l’extraction de leur cataracte a été réalisée avec la
technique de découpage rapide en utilisant le mode
en salves ou le mode pulsé. On a noté une réduction
significative de 50 % du temps total et absolu de la
phacoémulsification dans le groupe où l’on avait uti-
lisé le mode en salves .
La tendance la plus récente dans la phacoémulsi-
fication est à la réalisation d’une petite incision,
d’une phacoémulsification bimanuelle, sans man-
chon (aiguille nue), anticipant l’avènement des
lentilles intraoculaires plus petites, pliables, roulables
ou même injectables. Bien qu’il n’existe pas actuelle-
ment de lentilles que l’on puisse insérer par une
petite incision, l’extraction du cristallin au moyen de
phacoémulsification et un débit et un niveau de vide
élevé sont utilisés, aidés par de courtes salves de
phacoémulsification, afin de diriger les fragments
de noyau vers l’extrémité de l’aiguille. L’extrémité de
l’aiguille peut ainsi demeurer en position centrale et
dans une zone sûre. Il vaut mieux garder le couteau
ou le manipulateur sur le côté derrière le fragment
de noyau évacué pour protéger la capsule posté-
rieure. De plus, si le segment initial qui est découpé
est trop grand, il doit être découpé à nouveau en
plus petits fragments qui sont plus faciles à mani-
puler. Lorsque les derniers segments de noyau sont
émulsifiés, le niveau de vide et le débit doivent être
réduits, car cela permet d’avoir davantage de con-
trôle sur la stabilité de la chambre antérieure et
moins de poussées soudaines. Cette démarche doit
être répétée jusqu’à l’extraction complète du noyau.
Après l’évacuation du noyau, l’extrémité de
l’aiguille est dirigée sur le bord épinucléaire sous
faible vide ou débit. À mesure que l’on commence à
tirer le bord épinucléaire à l’extérieur du sac capsu-
laire, le deuxième instrument, un couteau ou un
manipulateur, est utilisé pour pousser sur le fond du
noyau avec un léger mouvement de roulement vers
le haut pour aider à diriger l’extraction du noyau.
S’il y a du cortex restant, il est retiré avec un dis-
positif manuel d’irrigation/d’aspiration à 45
o
, en
créant un vide allant jusqu’à 500 mm Hg. Si du cor-
tex sous l’incision est difficile à extraire, il est utile de
séparer l’irrigation et l’aspiration et d’utiliser une
technique bimanuelle pour l’extraction.
Le sac capsulaire est ensuite rempli de substance
visco-élastique et une lentille intraoculaire est
insérée dans le sac capsulaire. Une fois que la sub-
stance visco-élastique est retirée de l’œil, la plaie est
Figure 2 : Propagation de la fragmentation de
l’endonoyau. La flèche indique le mouve-
ment des instruments.
deux plus petites incisions présente 4 avantages
importants
1,6
:
• L’irrigation par l’instrument comportant des
orifices latéraux peut aider à déplacer les frag-
ments de noyau vers l’extrémité de l’aiguille de
phacoémulsification, car lorsque le liquide d’irri-
gation est délivré par le manchon, il peut poten-
tiellement créer un courant qui peut pousser les
fragments de cristallin loin de l’extrémité de
l’aiguille. La séparation de l’irrigation et de l’aspi-
ration devrait théoriquement
diriger les frag-
ments détachés vers l’orifice d’aspiration.
• On peut approcher les fragments de noyau
à partir de deux sites d’incision différents si
nécessaire.
• Le cortex sous l’incision peut être extrait
plus facilement.
• Des petites incisions permettent de main-
tenir une chambre antérieure stable et étanche.
Agarwal
9
a rapporté l’utilisation avec succès
de la méthode Phaconit d’extraction bimanuelle
du cristallin par une incision de 0,9 mm avec
une aiguille de phacoémulsification sans man-
chon. Des travaux de recherche récents sur le
Millenium Microsurgical System (Bausch & Lomb,
Rochester, New York) et l’appareil de phacoémul-
sification Sovereign, AMO, Californie) ont
démontré que la « microphacoémulsification »,
au moyen d’une aiguille de phacoémulsification
nue par une incision relativement petite pourrait
être réalisée en utilisant des paramètres spéci-
fiques sur ces appareils
10,11,12
.
Une étude clinique est actuellement en cours
utilisant la technique de découpage rapide
décrite antérieurement sur des cataractes dont la
sclérose du noyau varie de 2+ à 4+. La phaco-
émulsification avec le Millenium Microsurgical
System (Rochester, New York) en utilisant un
réglage en salves d’intervalles de 100 msec est
réalisée avec une aiguille de phacoémulsifica-
tion MicroFlow de calibre 20 sans manchon
biseautée à 30
o
par une incision de 1,4 mm faite
avec un couteau diamant. Cette dimension d’in-
cision permet d’introduire l’extrémité du phar-
macoémulsificateur de 1,1 mm dans l’œil sans
forcer sur la plaie et une petite quantité de
liquide évacuée permet le refroidissement de la
plaie sans compromettre l’intégrité de la cham-
bre (figure 3a). L’irrigation est également utilisée
par une incision latérale de 1,4 mm faite avec un
couteau d’irrigation de calibre 19 comportant
deux orifices d’irrigation latéraux (figure 3b). On
estime qu’un couteau d’irrigation avec deux
orifices latéraux plutôt qu’un orifice central prin-
cipal améliore la dynamique du liquide dans la
chambre antérieure, permettant aux courants de
diriger les fragments de noyau vers l’extrémité
du phacoémulsificateur plutôt qu’un jet direct
de liquide pouvant écarter les fragments loin de
l’extrémité de l’aiguille. Les niveaux de vide sont
réglés sur le Millennium System au moyen du
mode venturi pour qu’ils varient entre 180 et
325 mm Hg en utilisant une technologie linéaire
double et une hauteur de flacon de 125 cm. La
capacité d’utiliser différents niveaux de vide pro-
cure au chirurgien le contrôle nécessaire durant
la phacoémulsification bimanuelle pour régler le
niveau de vide selon la fluidique et minimiser
ainsi l’instabilité de la chambre antérieure. Par
exemple, le chirurgien pourrait utiliser un
niveau de vide élevé lorsque l’extrémité de
l’aiguille est totalement occluse et que la stabilité
est nécessaire pour assurer une technique
de découpage efficace. Cependant, lorsque
l’extrémité de l’aiguille n’est plus occluse, le
Ophtalmologie
Conférences scientifiques
Figure 3b : Irrigation et aspiration bimanuelles Figure 3a : Phacoémulsification
microincisionnelle sans manchon
chirurgien peut réduire le niveau de vide élevé à
un niveau qui permet une élimination suffisante
des segments, mais qui assure néanmoins la
stabilité de la chambre antérieure.
En utilisant les paramètres et la technique
décrits ci-dessus, la phacoémulsification peut
être réalisée efficacement et en toute sécurité
avec une technique bimanuelle sans manchon
et sans occasionner de traumatisme ou de
brûlure de la plaie. La durée absolue de la pha-
coémulsification varie de 1 à 7 secondes dans
ces cas et la durée moyenne du début à la fin est
2 minutes plus longue qu’avec les techniques de
phaco-émulsification conventionnelles. Les
plaies sont invariablement fermées le premier
jour suivant l’intervention avec un œdème
cornéen négligeable.
Conclusion
Le fait de pouvoir définir la puissance, modu-
ler les liquides et utiliser davantage de force
mécanique avec des techniques telles que le
découpage rapide pour extraire la cataracte a
permis d’utiliser une énergie ultrasonique moin-
dre dans l’œil et finalement d’obtenir de
meilleurs résultats pour les patients. La chirurgie
de la cataracte est devenue un domaine inno-
vateur et passionnant et la créativité des
chirurgiens spécialisés dans la cataracte entraî-
nera indubitablement encore davantage d’amélio-
rations dans les techniques et la technologie,
afin de perfectionner encore l’une des interven-
tions les plus réussies dans toute la médecine.
Rosa Braga-Mele, M.Ed, M.D., FRCSC, est professeure
adjointe, Université de Toronto, et directrice de l’Unité
de la cataracte et de l’enseignement chirurgical, Mount
Sinai Hospital.
Références
1. Fine IH, Packer M, Hoffman R. New phacoemulsifica-
tion technologies. J Cataract Refract Surg 2002;28:
1054-1060.
2. Fine IH, Packer M, Hoffman R. Use of power modula-
tions in phacoemulsification-Choo-choo chop and flip
phacoemulsification. J Cataract Refract Surg 2001;27:
188-197.
3. McColgin AZ, Heier JS. Control of intraocular inflam-
mation associated with cataract. Curr Opin Ophthalmol
2000;11(1):3-6.
4. Arshinoff SA. Dispersive-cohesive viscoelastic soft shell
technique. J Cataract Refract Surg 1999;25:167-173.
5. Fine IH. Cortical cleaving hydrodissection. J Cataract
Refract Surg 1992;18:508-512.
6. Tsuneoka H, Shiba T, Takahashi Y. Ultrasonic
phacoemulsification using a 1.4 mm incision: Clinical
results. J Cataract Refract Surg 2002;28:81-86.
7. Braga-Mele R. Control of vacuum and phaco power for
safe, efficient emulsification; Ocular Surgery News
2002;20(23):13-14.
8. Braga-Mele R. A presentation at the American Society
of Cataract and Refractive Surgery Meeting, June 2002,
Philadelphia, PA.
9. Agarwal A, Agarwal S, Agarwal A. Phakonit and laser
phakonit lens removal through 0.9 mm incision. In:
Agarwal A, Agarwal S. Sachdev MS, et al. Phacoemusifi-
cation, Laser Cataract Surgery and Foldable IOLs. New
Delhi: Jaypee Brothers;1999.
10. Braga-Mele R, Lui E. Feasibility of sleeveless bimanual
phacoemulsification on the Millennium Microsurgical
System; J Cataract Refract Surg 2003;29:2199-2203.
11. Braga-Mele R. Sleeveless bimanual phaco with Millen-
nium system delivers less thermal energy to the eye.
Ocular Surgery News 2003;21(7):43.
12. Soscia W, Howard J, Olson R. Bimanual phacoemulsifi-
cation through 2 stab incisions. A wound temperature
study. J Cataract Refract Surg 2002;28:1039-1043.
Résumés scientifiques d’intérêt connexe
Faisabilité de la phacoémulsification
bimanuelle sans manchon avec le système
microchirurgical Millennium
BRAGA-MELE R, LIU E, TORONTO, ONTARIO
OBJECTIF : Évaluer la faisabilité de la phacoémulsifi-
cation bimanuelle sans manchon en utilisant le Millen-
nium Microsurgical System (Bausch and Lomb
Surgical) en mesurant la température de la plaie
durant la phacoémulsification.
LIEU : Laboratoire, in vitro.
MÉTHODOLOGIE : Le système Millennium a été util-
isé dans 6 yeux provenant d’une banque des yeux au
moyen du mode pulsé et du mode en salves avec des
salves à des intervalles de 80 millisecondes et 160 mil-
lisecondes. La température des plaies a été mesurée et
les plaies ont été observées, afin de détecter toute
lésion thermique.
RÉSULTATS : Dans le mode pulsé et l’état de non
occlusion à une puissance de 100 %, la température
maximale était de 43,8 degrés C. Dans l’état d’occlu-
sion à une puissance de 30 %, la température maxi-
male était de 51,7 degrés C après 70 secondes
d’occlusion. Lorsqu’on utilise des salves de phacoémul-
sification d’un intervalle de 160 millisecondes, la tem-
pérature maximale était de 41,4 degrés C (état de non
occlusion à une puissance de 100 %). À une puissance
de 80 %, la température maximale était de 53,2 degrés
C dans les 60 secondes de l’occlusion totale pendant
l’aspiration, la pédale de commande à pied étant totale-
ment relâchée. Avec un intervalle entre les salves de
80 millisecondes durant les états de non occlusion et
d’occlusion (puissance de 100 %, pédale de commande
à pied totalement relâchée pendant 3 minutes), il n’y
avait pas d’augmentation significative de la tempéra-
ture. La température maximale était de 33,6 degrés C
Ophtalmologie
Conférences scientifiques
Événements futurs dans le département
6 mai 2004
PPI – D
r
Kathleen Digre, Salt Lake City, Utah
Neuro-ophthalmic changes in pregnancy
13 mai 2004
PPI – D
r
Shaun Singer, Toronto, Ontario
Quality Assurance Rounds
20 mai 2004
PPI – D
r
David Apple, Charleston, Caroline du Nord
Réunions scientifiques combinées de l’Université de Toronto
et de TOS, Vaughan Estate
27 mai 2004
PPI – D
r
Marian Macsal, Glenview, Illinois
Refractory blepharomeibomitis – The bread & butter
of your clinical practice
4 juin 2004
Journée de la recherche –
Auditorium Koffler de l’Université de Toronto
Renseignements : Sertina Law (416) 603-5663
16 au 19 juin – COS, Vancouver
Note : Adresse du site du Programme pour les professeurs
invités (PPI)
Toronto Western Hospital, West Wing, Room 2 – 401,
399 Bathurst Street, Toronto
pendant la non occlusion et de 41,8 degrés C pendant
l’occlusion. Dans tous les cas, la plaie cornéenne est
demeurée intacte. On n’a pas noté de brûlure ou de
contracture de la plaie.
CONCLUSIONS : Les augmentations de la température
démontrées se sont produites lors de l’utilisation de
paramètres cliniquement inhabituels. La phacoémulsifica-
tion avec une aiguille sans manchon par une petite incision
peut être réalisée en toute sécurité avec le système Millen-
nium en utilisant le mode traditionnel en salves de phaco-
émulsification à l’intérieur de certains paramètres.
J Cataract Refract Surg 2003 ;29(11):2199-203.
Nouvelles technologies de phacoémulsification
FINE
I H, PACKER
M, HOFFMAN R S, E
UGENE
, OR EGON
Pour examiner les progrès récents dans le domaine de la
phacoémulsification, une revue de la littérature a été effec-
tuée pour chacun des systèmes décrits. La revue incluait
des articles examinés par les pairs, des renseignements des
fabricants et des présentations faites à des réunions par des
chirurgiens. Notre expérience personnelle des systèmes
que nous avons utilisés constitue le fondement de notre
évaluation. Données pour le laser erbium : les données sur
la phacoémulsification avec le laser YAG provenaient d’un
résumé provisoire d’une étude surveillée par la Food and
Drug Administration américaine. Les données pour
NeoSoniX provenaient d’une évaluation prospective de la
phacoémulsification réalisée dans 25 yeux à l’Oregon Eye
Surgery Center. L’élaboration d’une nouvelle technologie a
permis une phacoémulsification plus sûre et plus efficace.
Chaque chirurgien doit évaluer les nouveaux progrès pour
obtenir les meilleurs résultats possibles pour chaque
patient.
J Cataract Refract Surg 2002;28(6):1054-60.
Réunions scientifiques à venir
4 au 5 juin 2004
Age-related Macular Degeneration Update 2004
Baltimore, Maryland
Renseignements : Tél. : 410-955-5880
Courriel :
16 au 19 juin 2004
Réunion annuelle de la Société canadienne d’Ophtalmologie
Vancouver, Colombie-Britannique
CONTACT:
Site web : www.eyesite.ca
© 2004 Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto, seul responsable du contenu de cette publication. Édition : SNELL Communication
Médicale Inc. avec la collaboration du Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto.
MD
Ophtalmologie – Conférences scientifiques est une marque
de commerce de SNELL Communication Médicale Inc.Tous droits réservés. L’administration d’un traitement thérapeutique décrit ou mentionné dans Ophtalmologie – Conférences scientifiques doit
toujours être conforme aux renseignements d’ordonnance approuvés au Canada. SNELL Communication Médicale se consacre à l’avancement de l’éducation médicale continue de niveau supérieur.
L’élaboration de cette publication a bénéficié d’une subvention à l’éducation de
Novartis Ophthalmics
130-007F
La version française a été révisée par le professeur Pierre Lachapelle,
Montréal.
Les avis de changement d’adresse et les demandes d’abonne-
ment pour Ophtalmologie – Conférences Scientifiques doivent
être envoyés par la poste à l’adresse C.P. 310, Succursale H,
Montréal (Québec) H3G 2K8 ou par fax au (514) 932-5114 ou
par courrier électronique à l’adresse
Veuillez vous référer au bulletin Ophtalmologie – Conférences
Scientifiques dans votre correspondence. Les envois non
distribuables doivent être envoyés à l’adresse ci-dessus.
Poste-publications #40032303
SNELL
Ophtalmologie
Conférences scientifiques
MAI 2004
Volume 2, numéro 5
COMPTE RENDU DES CONFÉRENCES
SCIENTIFIQUES DU DÉPARTEMENT
D’OPHTALMOLOGIE ET
DES SCIENCES DE LA VISION,
FACULTÉ DE MÉDECINE,
UNIVERSITÉ DE TORONTO
Département d’ophtalmologie
et des sciences de la vision
Faculté de médecine
Université de Toronto
60 Murray St.
Bureau 1-003
Toronto (Ontario) M5G 1X5
Le contenu rédactionnel d’Ophtalmologie –
Conférences scientifiques est déterminé
exclusivement par le Département
d’ophtalmologie et des sciences de la vision,
Faculté de médicine, Université de Toronto.
Département d’ophtalmologie
et des sciences de la vision
Jeffrey Jay Hurwitz, M.D., Rédacteur
Professeur et président
Martin Steinbach, Ph.D.
Directeur de la recherche
The Hospital for Sick Children
Elise Heon, M.D.
Ophtalmologiste en chef
Mount Sinai Hospital
Jeffrey J. Hurwitz, M.D.
Ophtalmologiste en chef
Princess Margaret Hospital
(Clinique des tumeurs oculaires)
E. Rand Simpson, M.D.
Directeur, Service d’oncologie oculaire
St. Michael’s Hospital
Alan Berger, M.D.
Ophtalmologiste en chef
Sunnybrook and Women’s College
Health Sciences Centre
William S. Dixon, M.D.
Ophtalmologiste en chef
The Toronto Hospital
(Toronto Western Division and
Toronto General Division)
Robert G. Devenyi, M.D.
Ophtalmologiste en chef
Le traitement chirurgical de la cataracte
et du glaucome coexistants
PAR
YVONNE
M. BUYS, M.D., FRCSC
Le glaucome et la cataracte sont des maladies associées au vieillissement et par
conséquent, il n’est pas rare qu’elles coexistent chez le même patient. Cependant,
dans le passé, la chirurgie combinée de la cataracte et du glaucome n’était pas une
intervention très pratiquée, étant donné que ces deux interventions visent des résul-
tats opposés, à savoir la fermeture de la plaie dans la chirurgie de la cataracte et le
maintien d’une plaie filtrante dans la chirurgie du glaucome. Les techniques chirurgi-
cales antérieures, telles que la chirurgie du glaucome en pleine épaisseur – dans
laquelle l’aplatissement de la chambre antérieure était fréquent et était également
une indication de succès - étaient fondamentalement en désaccord avec la chirurgie
de la cataracte, où cette situation était spécifiquement évitée. L’amélioration des tech-
niques chirurgicales de la cataracte (comprenant la phacoémulsification par petite
incision cornéenne et l’implantation d’une lentille intraoculaire), la conversion à la
chirurgie filtrante protégée (dans laquelle l’aplatissement de la chambre antérieure
est rare) et l’utilisation d’antimétabolites ont contribué à l’amélioration des résultats
en ce qui concerne la vision et la pression intraoculaire (PIO). L’évolution de la
chirurgie de la cataracte, des méthodes d’implantation d’une lentille intraoculaire et
de la chirurgie filtrante est telle que la chirurgie combinée est maintenant relative-
ment fréquente. Dans ce numéro d’Ophtalmologie – Conférences scientifiques, nous
examinons le traitement chirurgical des patients atteints de cataracte et de glaucome
coexistants.
Stratégies chirurgicales
De nombreux facteurs doivent être pris en considération lorsque l’on détermine la
stratégie chirurgicale optimale pour les patients souffrant de cataracte et de glaucome.
L’approche est individualisée en prenant en considération le type spécifique de glaucome,
la gravité de la neuropathie optique, le contrôle de la pression, le nombre de médicaments
utilisés pour le glaucome, la vitesse de progression, la PIO cible, le degré de cataracte et
finalement, les questions relatives à la qualité de vie. La littérature publiée peut fournir
d’autres données concernant le traitement, mais la qualité de ces publications varie. Par
exemple, selon une revue systématique de publications anglaises de 1964 à juillet 2000,
on a jugé que seulement 36 études randomisées et contrôlées, 7 études contrôlées non
randomisées et 38 études de cohortes avaient une valeur suffisante pour être incluses
dans une revue de ce thème fondée sur des preuves scientifiques
1
. On a attribué un score
de 0 % à vingt-cinq de ces études (31 %) en ce qui concerne les biais et les variables
confondantes, ce qui signifie qu’il faut faire preuve de prudence lorsqu’on interprète les
résultats de ces études et leur applicabilité dans la pratique individuelle.
Le traitement chirurgical d’un patient atteint de cataracte et de glaucome coexistants
peut être envisagé dans l’une des deux situations suivantes :
• une cataracte entraînant une atteinte significative de la vision avec un glaucome
médicalement contrôlé ou
• un glaucome non contrôlé malgré un traitement médical/chirurgical et une opacité
du cristallin.
MC
Département
d’ophtalmologie et des
sciences de la vision
FACULTY OF MEDICINE
University of Toronto
Disponible sur Internet à :
www.ophtalmologieconferences.ca
Actuellement, les stratégies chirurgicales de choix
pour les patients atteints de cataracte et de glaucome
coexistants comprennent la phacoémulsification
seule, la phacoémulsification suivie d’une chirurgie fil-
trante, la trabéculectomie suivie de la phacoémulsifi-
cation et la phacotrabéculectomie combinée. De
nouvelles alternatives telles que la phacoémulsifi-
cation associée à l’aspiration trabéculaire
2
, la vis-
cocanalostomie
3
, la sclérectomie profonde
4
et la
cycloablation endoscopique au laser
5
ou la trabéculo-
tomie
6
peuvent modifier les normes actuelles. Cepen-
dant, actuellement, les données sont insuffisantes
pour que l’on recommande d’adopter systématique-
ment l’une ou l’autre de ces techniques.
La phacoémulsification seule
Une étude menée par Freidman et coll. a signalé
une baisse temporaire de la PIO de 2-4 mm Hg 1 à 2
ans après une phacoémulsification seule chez des
patients atteints de glaucome
7
. Il est important de se
rappeler que le « glaucome » est un terme qui com-
prend un groupe hétérogène de maladies et la phacoé-
mulsification seule peut produire une baisse encore
plus prononcée de la PIO chez des sous-groupes spéci-
fiques de patients atteints de glaucome. Hayashi et
coll. ont signalé une baisse moyenne de la PIO de 6,4
mm Hg à 1 an dans 77 yeux atteints de glaucome à
angle fermé (GAF) et une baisse de 4,1 mm Hg dans 73
yeux atteints de glaucome à angle ouvert (GAO)
8
.
Shingleton et coll. ont étudié l’extraction de la
cataracte chez des patients atteints ou non du syn-
drome de pseudo-exfoliation capsulaire (PEXC)
9
. Après
deux ans, leur PIO avait baissé de 2,9 mm Hg par rap-
port aux valeurs avant l’intervention (p < 0,00001) et
un nombre significativement moins élevé de médica-
ments pour le glaucome était nécessaire chez 297
patients atteints du syndrome du PEXC, alors que chez
427 patients n’en étant pas atteints, on a noté une
réduction de 1,9 mm Hg de la PIO
9
.
D’autres sous-groupes spécifiques de glaucome (p.
ex. glaucome secondaire à un mauvais trajet de
l’humeur aqueuse, glaucome phacomorphique, glau-
come phacolytique, glaucome secondaire à la
sphérophakie
10
) sont des exemples où la phacoémul-
sification seule peut réduire temporairement la PIO.
Cependant, il faut faire preuve de prudence avec cette
approche, étant donné que la baisse de la PIO peut ne
pas être maintenue à long terme. Hayashi et coll. ont
signalé qu’après deux ans, la probabilité cumulative
de maintien du contrôle de la PIO était de 91,9 %
chez 74 patients atteints de GAF et de 72,1 % chez 68
patients atteints de GAO (p = 0,0012) ; la PIO a été
contrôlée sans médicament dans 30 yeux dans le
groupe atteint de GAF et dans 13 yeux dans le groupe
atteint de GAO (p = 0,0055)
11
. Un résultat semblable a
été obtenu par Pohjalainen et coll. qui ont signalé que
2,8 années après la phacoémulsification seule, le con-
trôle de la PIO s’était amélioré ou était demeuré
inchangé pour 86 % et s’était aggravé pour 14 % des
yeux atteints de GAO
12
. Le mécanisme de la baisse
de la PIO après une chirurgie de la cataracte a été
attribué à une amélioration de l’écoulement de
l’humeur aqueuse
13
.
La phacoémulsification suivie
de la chirurgie filtrante
Grâce à l’amélioration de la phacotrabéculectomie
combinée, la phacoémulsification planifiée suivie de la
chirurgie filtrante n’est pas indiquée. Cette approche
est réservée aux cas où la PIO n’est pas médicalement
contrôlée après une chirurgie de la cataracte pendant
la période postopératoire initiale ou tardive.
La chirurgie filtrante suivie de
la phacoémulsification
Il existe des données concluantes indiquant que la
PIO est plus basse après la trabéculectomie seule
qu’après la chirurgie combinée. Les auteurs d’une
revue de la littérature de 1964 à 2000 ont conclu que
l’on peut s’attendre à une baisse supplémentaire de 2-4
mm Hg de la PIO lorsque la trabéculectomie seule est
réalisée comparativement à la chirurgie combinée
7
.
La question suivante demeure : La PIO sera-t-elle
plus basse après une chirurgie échelonnée (tra-
béculectomie suivie de phacoémulsification) ou après
une chirurgie combinée ? Il n’existe actuellement pas
d’études randomisées et contrôlées traitant de cette
question.
L’effet de la chirurgie de la cataracte subséquente
sur la PIO et la fonction de la bulle de filtration (après
la trabéculectomie) varie
14-20
. Le tableau 1 résume les
résultats de six études rétrospectives
14-19
et d’une
étude prospective
20
qui ont évalué l’effet positif de la
chirurgie filtrante après la phacoémulsification sub-
séquente sur la PIO. Deux études ont comparé le taux
de succès avec un groupe témoin apparié qui a subi
une trabéculectomie seule et n’ont pas constaté une
différence statistiquement significative en ce qui con-
cerne le taux de succès
14,18
. Cela semble indiquer que
le taux d’échec de la trabéculectomie après une pha-
coémulsification subséquente est le même qu’avec la
trabéculectomie seule.
Les résultats relatifs aux facteurs possibles associés
aux taux accrus d’échec du contrôle post-opératoire
de la PIO étaient contradictoires. Dans une étude,
lorsque l’extraction de la cataracte a été effectuée
après la trabéculectomie, les facteurs suivants ont été
associés à un moins bon contrôle de la PIO : âge ≤ 50
ans, PIO préopératoire > 10 mm Hg, manipulation de
l’iris peropératoire et PIO pendant la période
postopératoire initiale > 25 mm Hg
15
. Dans une autre
étude
18
, on a constaté un résultat semblable en ce qui
concerne la manipulation de l’iris. Cependant, dans 2
autres études
19,20
, on n’a pas constaté d’association
entre la manipulation de l’iris et le succès de la
chirurgie filtrante.
• L’étude AGIS (Advanced Glaucoma Intervention
Study) a signalé la présence de la cataracte dans 4 %
des yeux après la trabéculectomie initiale et dans 7 %
après une seconde trabéculectomie, comparativement
à 1 % après la trabéculectomie au laser à argon après
des périodes moyennes de suivi de 9,8, 6,6 et 10,0 ans,
respectivement
22
.
• Dans l’étude CIGTS (Collaborative Initial Glau-
coma Treatment Study)
23
, à trois ans, on a noté un taux
de cataracte trois fois plus élevé dans le groupe ayant
subi une intervention chirurgicale (17 %) que dans le
groupe ayant reçu un traitement médical (6 %).
Les divers taux de cataracte dans ces études sont
dus aux définitions différentes de la cataracte et peu-
vent être liés à la modification de la technique de la
trabéculectomie. La tendance actuelle de la tra-
béculectomie à éviter l’hypotonie précoce et
l’aplatissement de la chambre antérieure peut réduire
le taux de formation de la cataracte. Ainsi, 52 % à
96 % des yeux n’ont pas développé la cataracte après
la trabéculectomie pendant un suivi allant jusqu’à
10 ans. Pour les patients atteints de glaucome et souf-
frant de cataracte légère à modérée uniquement, la
trabéculectomie peut donc être suffisante et nombre
d’entre eux peuvent ne jamais avoir besoin d’une
chirurgie de la cataracte.
La phacotrabéculectomie combinée
Il existe peu d’études portant sur les questions
liées à la qualité de vie dans le traitement du glau-
On ne connaît pas l’intervalle de temps optimal
entre la trabéculectomie et la phacoémulsification
subséquente. Chen et ses collaborateurs ont constaté
qu’un intervalle > 6 mois entre les interventions était
associé à un succès significativement supérieur
15
.
Deux autres études n’ont pas constaté que l’intervalle
de temps entre les interventions influençait le succès
de la chirurgie filtrante
17,20
. Dans une étude, les inter-
valles étudiés étaient < 1 an, 1-3 ans et > 3 ans
17
, alors
que dans l’autre, l’intervalle le plus court entre la tra-
béculectomie et la phacoémulsification était de
13 mois
20
. Derbolav et coll. ont constaté que bien que
des intervalles < 6 mois entre la trabéculectomie et la
phacoémulsification aient été associés à une augmen-
tation statistiquement semblable du nombre de
médicaments, la PIO avait significativement augmenté
lorsqu’un intervalle supérieur à 6 mois s’était écoulé
entre les interventions
19
.
Il existe des données concluantes indiquant que la
trabéculectomie peut accélérer la formation de la
cataracte (tableau 2).
• Dans l’étude CNTGS (Collaborative Normal Ten-
sion Glaucoma Study), la cataracte (définie comme la
perte de 2 lignes de Snellen attribuée à l’opacité du
cristallin) s’est développée dans 48 % des yeux ayant
subi une trabéculectomie comparativement à 25 %
des yeux traités avec des médicaments ± une trabécu-
loplastie au laser à argon (TLA) et 14 % des témoins,
avec une période moyenne de suivi de 5,8 ans dans le
groupe traité et de 4,0 ans dans le groupe témoin
21
.
Tableau 1 : L’effet de la phacoémulsification subséquente sur la PIO des yeux après la trabéculectomie (avec
une bulle de filtration)
Suivi
Étude Nombre d’yeux (mois) % de succès Définition du succès
Park
14
40 20,1 80 % à 3 ans PIO < 22 mm Hg ou réduction > 20 %
comparativement à avant la trabéculectomie. Pas
besoin de médicaments additionnels pour le glaucome
40 témoins 18,7 79 % à 3 ans
ou d’une autre chirurgie du glaucome.
(trabéculectomie
uniquement)
Chen
15
57 17,6 74 Pas besoin de médicaments additionnels pour le
glaucome, de suture de la bulle de filtration ou d’une
autre chirurgie du glaucome.
Manoj
16
21 15,1 100 PIO < 21 mm Hg et pas besoin de médicaments
supplémentaires pour le glaucome.
Crichton
17
69 22,2 77 Pas besoin de médicaments supplémentaires pour
le glaucome.
Casson
18
28 24 82 Pas besoin de médicaments supplémentaires pour
28 témoins 24 96 (p=0,089)
le glaucome.
(trabéculectomie
uniquement)
Rebolleda
20
49 19,5 67 Pas besoin de médicaments supplémentaires pour le
glaucome, de suture de la bulle de filtration ou d’une
autre chirurgie du glaucome.
Derbolav
19
48 23 67 PIO < 22 mm Hg et pas besoin d’une autre chirurgie
du glaucome.
come. Cependant, intuitivement, la chirurgie
combinée offre plusieurs avantages par rapport à
la chirurgie échelonnée. Ces avantages sont les
suivants :
• Réduction du risque lorsqu’une seule inter-
vention et une seule anesthésie sont effectuées.
• Réduction des coûts de soins de santé et des
coûts pour le patient.
• Réadaptation visuelle plus rapide.
• Possiblement, réduction du risque de pics
tensionnels post-opératoires associés à la
chirurgie de la cataracte.
Les techniques chirurgicales peuvent influer
sur les résultats, notamment la technique des
deux sites opératoires par rapport à un site, le
lambeau à base limbique par rapport au lambeau
à base au fornix et l’utilisation d’antimétabolites.
Plusieurs études randomisées et contrôlées com-
parant la technique d’un site opératoire par rap-
port à deux sites sont parvenues aux mêmes
conclusions. Toutes ces études ont constaté une
PIO plus basse après une chirurgie effectuée avec
deux sites opératoires, mais cette différence n’é-
tait pas statistiquement significative (tableau 3).
Un nombre significativement moins élevé de
médicaments pour le glaucome était nécessaire
dans le groupe où la technique d’un site opéra-
toire avait été utilisée dans une étude
24
et dans le
groupe dans lequel la technique de deux sites
opératoires avait été utilisée dans l’autre étude
25
.
Dans une troisième étude, on a constaté un nom-
bre significativement plus élevé de bulles de filtra-
tion cliniquement apparentes dans le groupe où la
technique de deux sites opératoires avait été utili-
sée
27
. Les auteurs d’une revue fondée sur des don-
nées scientifiques de la technique chirurgicale
d’un site opératoire par rapport à deux sites opéra-
toires ont conclu qu’il y avait peu de données
indiquant que la technique de deux sites opéra-
toires permettait d’obtenir une PIO de 1-2 mm Hg
plus faible que la technique d’un site opératoire
28
.
Dans cette même revue, les auteurs ont égale-
ment conclu que la chirurgie combinée cataracte
et glaucome avec l’addition de mitomycine-C et
non de 5-fluorouracil entraîne une réduction plus
prononcée de la PIO
28
. Les auteurs de trois publi-
cations comparant la réduction de la PIO du lam-
beau à base au fornix et limbique dans les
phacotrabéculectomies ont noté que le lambeau
conjonctival n’avait aucune influence sur la PIO
finale
29-31
.
Conclusion
Il n’existe pas une seule approche à adopter
chez le patient atteint de cataracte et de glaucome
coexistants. Chaque cas doit être individualisé et
l’on doit tenir compte du type et de la gravité du
glaucome, du taux de progression, de la réponse
Ophtalmologie
Conférences scientifiques
Tableau 3 : Phacotrabéculectomie avec un site opératoire vs 2 sites opératoires
PIO moyenne (mm Hg) PIO moyenne (mm Hg)
Nombre Suivi moyen Un site opératoire Deux sites opératoires
Étude d’yeux (mois) (% de réduction) (% de réduction)
Wyse
25
33 16,5 15,3±4,1 (23 %) 13,3±4,0 (31 %)
Borggrefe
26
50 19 16,8±5,1 (43 %) 15,0±3,1 (50 %)
El-Sayyad
27
74 12 19,1±3,1 (27 %) 17,6±3,3 (37 %)
Tableau 2 : Taux de formation de la cataracte après la trabéculectomie
Nombre Suivi moyen Nombre de
Étude Intervention d’yeux (années) cataractes (%)
CNTGS
21
* Témoin 79 4,0 11 (14)
Médicament ± TLA 28 5,8 7 (25)
Trabéculectomie 33 5,8 16 (48)
AGIS
22
** TLA comme 1re ou 2e intervention 461 10,0 3 (0,7)
Trabéculectomie comme 1re ou 513 9,8 21 (4,1)
2e intervention
Trabéculectomie comme 3e intervention 46 6,6 3 (7,0)
CIGTS
23
*** Médicament 300 3 52 (17,3)
Chirurgie 307 3 19 (6,2)
Légende : * CNTGS = Collaborative Normal Tension Glaucoma Study ; ** AGIS = Advanced Glaucoma Intervention Study ;
*** GIGTS = Collaborative Initial Glaucoma Treatment Study
au traitement du glaucome et du degré de la
cataracte. Enfin, il existe des nouvelles techniques
chirurgicales qui peuvent modifier l’approche
adoptée. Lorsque toutes ces questions sont prises
en compte, les approches suivantes pour les
patients atteints de cataracte et de glaucome
coexistants présentant des tableaux cliniques
différents sont appropriées :
Le patient dont le glaucome est contrôlé et
dont la cataracte entraîne une atteinte
significative de la vision
La phacoémulsification seule permet d’obtenir
une réduction transitoire de 2-4 mm Hg de la PIO
pendant 1 à 2 ans
7
, et doit donc être envisagée
chez les patients atteints de neuropathie optique
glaucomateuse légère à modérée contrôlée avec 1
ou 2 médicaments pour le glaucome. Dans le cas
de sous-groupes spécifiques de glaucome, tels que
le glaucome à angle fermé
8
, le glaucome par
pseudo-exfoliation capsulaire
9
, le glaucome
secondaire à un mauvais trajet de l’humeur aque-
use, le glaucome phacomorphique, le glaucome
phacolytique et le glaucome secondaire à la
microsphérophakie
10
, il est plus probable que la
phacoémulsification seule entraîne une améliora-
tion du contrôle de la PIO. Cependant, il est
impératif de surveiller étroitement la PIO pendant
la période post-opératoire, étant donné qu’il existe
des rapports indiquant que dans 28 % des patients
atteints de glaucome primitif à angle ouvert,
le contrôle est moins bon et 7 % nécessite une
chirurgie filtrante dans les deux ans suivant la
phacoémulsification
11
.
Patient dont le glaucome et la cataracte
ne sont pas contrôlés
Dans ce scénario, il est peu probable que la
phacoémulsification seule entraîne une améliora-
tion. Bien que la trabéculectomie seule puisse
fournir un contrôle de la PIO légèrement
supérieur à celui obtenu avec la phacotrabéculec-
tomie combinée
7
, l’effet de la chirurgie sub-
séquente de la cataracte sur la fonction de la bulle
de filtration doit être débattu
14-20
. De plus, les
questions liées à la qualité de vie, comprenant la
possibilité de réduire le risque avec une interven-
tion par rapport à deux, le coût accru des deux
interventions et la réadaptation visuelle plus
longue sont autant de facteurs qui appuient la
phacotrabéculectomie combinée en tant qu’inter-
vention de choix dans cette situation. Technique-
ment, la technique de deux sites opératoires avec
l’addition de mitomycine-C peut fournir une
réduction supplémentaire de la PIO
28
.
Patient souffrant de neuropathie optique
glaucomateuse au stade avancé et
de cataracte légère à modérée
Si la prévention des pics tensionnels post-
opératoires et la réduction à long terme de la PIO
ont une importance essentielle, la réalisation de la
trabéculectomie avec l’addition de mitomycine-C
initialement, suivie de la chirurgie de la cataracte
au moins 6 mois plus tard (si nécessaire), serait
l’approche la plus appropriée. Étant donné que la
trabéculectomie peut être réalisée actuellement
en chirurgie d’un jour, le taux de progression sub-
séquente de la cataracte peut être tel que de nom-
breux patients peuvent être satisfaits de leur
vision et ne jamais avoir besoin d’une chirurgie de
la cataracte.
References
1. Jampel HD, Friedman DS, Lubomski LH, et al. Methodologic
rigor of clinical trials on surgical management of eyes with
coexisting cataract and glaucoma. Ophthalmology 2002;109:
1892-1901.
2. Jacobi PC, Dietlein TS, Krieglstein GK. Bimanual trabecular
aspiration in pseudoexfoliation glaucoma: an alternative in
nonfiltering glaucoma surgery. Ophthalmology 1998;105:
886-94.
3. Gimbel HV, Anderson Penno EE, Ferensowicz M. Combined
cataract surgery, intraocular lens implantation, and visco-
canalostomy. J Cataract Refract Surg 1999;25:1370-5.
4. Gianoli F, Schnyder CC, Bovey E, Mermoud A. Combined
surgery for cataract and glaucoma: phacoemulsification and
deep sclerectomy compared with phacoemulsification and
trabeculectomy. J Cataract Refract Surg 1999;25:340-6.
5. Gayton JL, Van Der Karr M, Sanders V. Combined cataract
and glaucoma surgery: Trabeculectomy versus endoscopic
laser cycloablation. J Cataract Refract Surg 1999;25:1214-9.
6. Tanito M, Ohira A, Chihara E. Surgical outcome of combined
trabeculotomy and cataract surgery. J Glaucoma 2001;10:
302-8.
7. Friedman DS, Jampel HD, Lubomski LH, et al. Surgical strate-
gies for coexisting glaucoma and cataract: an evidence-based
update. Ophthalmology 2002;109:1902-13.
8. Hayashi K, Hayashi H, Nakao F, Hayashi F. Changes in ante-
rior chamber angle width and depth after intraocular lens
implantation in eyes with glaucoma. Ophthalmology
2000;107:698-703.
9. Shingleton BJ, Heltzer J, O’Donoghue MW. Outcomes of
phacoemulsification in patients with and without pseudoex-
foliation syndrome. J Cataract Refract Surg 2003;29:1080-6.
10. Willoughby CE, Wishart PK. Lensectomy in the management
of glaucoma in spherophakia. J Cataract Refract Surg
2002;28:1061-4.
11. Hayashi K, Hayashi H, Nakao F, Hayashi F. Effect of cataract
surgery on intraocular pressure control in glaucoma patients.
J Cataract Refract Surg 2001;27:1779-86.
12. Pohjalainen T, Vesti E, Uusitalo FJ, Laatikainen L. Phacoemul-
sification and intraocular lens implantation in eyes with
open-angle glaucoma. Acta Ophthalmol Scand 2001;79:313-6.
13. Meyer MA, Savitt ML, Kopitas E. The effect of phacoemulsifi-
cation on aqueous outflow facility. Ophthalmology 1997;104:
1221-7.
14. Park HJ, Kwon YH, Weitzman M, Caprioli J. Temporal corneal
phacoemulsification in patients with filtered glaucoma. Arch
Ophthalmol 1997;115:1375-80.
Ophtalmologie
Conférences scientifiques
Réunion scientifique à venir
16 au 19 juin 2004
Réunion annuelle de la Société
canadienne d’ophtalmologie
Vancouver, Colombie-Britannique
Renseignements : Courriel :
Site web : www.eyesite.ca
Evénements futurs dans le département
5 juin 2004
Journée de la recherche –
Auditorium Koffler de l’Université de Toronto
569 Spadina Avenue
Renseignements : Sertina Law (416) 603-5663
16 au 19 juin 2004
Réunion de la Société canadienne d’ophtalmologie,
Vancouver
23 au 27 octobre
Réunion de l’American Academy – Nouvelle-Orléans
3 au 4 décembre 2004
Walter Wright Day « Ocular Emergencies »
Coordinateur – Dr Dan DeAngelis
Note : Adresse du site du Programme pour les professeurs
invités (PPI) : Toronto Western Hospital, West Wing, Room
2-401, 399 Bathurst Street, Toronto
L’année prochaine, le PPI aura lieu à l’Hôpital St Michael,
30 Bond Street, Toronto – Paul Marshall Lecture Theatre,
B1-Queen, entrée Queen Street (près de Second Cup).
15. Chen PP, Weaver YK, Budenz DL, Feuer WJ. Trabeculectomy func-
tion after cataract extraction. Ophthalmology 1998;105:1928-35.
16. Manoj B, Chako D, Khan MY. Effect of extracapsular cataract
extraction and phacoemulsification performed after trabeculec-
tomy on intraocular pressure. J Cataract Refract Surg 2000;26: 75-8.
17.Crichton ACS, Kirker AW. Intraocular pressure and medication
control after clear corneal phacoemulsification and AcrySof poste-
rior chamber intraocular lens implantation in patients with filter-
ing blebs. J Glaucoma 2001;10:38-46.
18. Casson R, Rahman R, Salmon JF. Phacoemulsification with intraoc-
ular lens implantation after trabeculectomy. J Glaucoma 2002;11:
429-33.
19. Derbolav A, Vass C, Menapace R, Schmetterer K, Wedrich A. Long-
term effect of phacoemulsification on intraocular pressure after
trabeculectomy. J Cataract Refract Surg 2002;28:425-30.
20.Rebolleda G, Munoz-Negrete FJ. Phacoemulsification in eyes with
functioning filtering blebs: A prospective study. Ophthalmology
2002;109:2248-55.
21. The Collaborative Normal-Tension Glaucoma Study Group. The
effectiveness of intraocular pressure reduction in the treatment of
normal-tension glaucoma. Am J Ophthalmol 1998;126:498-505.
22. The AGIS Investigators. The advanced glaucoma intervention
study (AGIS): 11. Risk factors for failure of trabeculectomy and
argon laser trabeculoplasty. Am J Ophthalmol 2002;134:481-98.
23. Lichter PR, Musch DC, Gillespie BW, et al. Interim clinical out-
comes in the collaborative initial glaucoma treatment study com-
paring initial treatment randomized to medications or surgery.
Ophthalmology 2001;108:1945-53.
24. Rossetti L, Bucci L, Miglior S, Orzalesi N. Temporal corneal pha-
coemulsification combined with separate-incision superior tra-
beculectomy vs standard phacotrabeculectomy. A comparative
study. Acta Ophthalmol Scand Suppl 1997;224:39.
25. Wyse T, Meyer M, Ruderman JM, et al. Combined trabeculectomy
and phacoemulsification: a one-site vs a two-site approach. Am J
Ophthalmol 1998;125:334-9.
26. Borggrefe J, Lieb W, Grehn F. A prospective randomized compari-
son of two techniques of combined cataract-glaucoma surgery.
Graefes Arch Clin Exp Ophthalmol 1999;237:887-92.
27.El-Sayyad F, Helal M, El-Maghraby A, Khalil M, El-Hamzawey H.
One-site versus 2-site phacotrabeculectomy: a randomized study. J
Cataract Refract Surg 1999;25:77-82.
28. Jampel HD, Friedman DS, Lubomski LH, et al. Effect of technique
on intraocular pressure after combined cataract and glaucoma
surgery. An evidence-based review. Ophthalmology 2002;109:
2215-24.
29. Lemon LC, Shin DH, Kim C, Bendel RE, Hughes BA, Juzych MS.
Limbus-based vs fornix-based conjunctival flap in combined glau-
coma and cataract surgery with adjunctive mitomycin C. Am J
Ophthalmol 1998;125:340-5.
30. Shingleton BJ, Chaudhry IM, O’Donoghue MW, Baylus SL, King RJ,
Chaudry MB. Phacotrabeculectomy: limbus-based versus fornix-
based conjunctival flaps in fellow eyes. Ophthalmology 1999;106:
1152-5.
31. Kozobolis VP, Siganos CS, Christodoulakis EV, Lazarow NP,
Koutentaki MG, Pallikaris IG. Two-site phacotrabeculectomy with
intraoperative mitomycin-C: fornix- versus limbus-based conjunc-
tival opening in fellow eyes. J Cataract Refract Surg 2002;28:
1758-62.
© 2004 Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto, seul responsable du contenu de cette publication. Édition : SNELL Communication
Médicale Inc. avec la collaboration du Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto.
MD
Ophtalmologie – Conférences scientifiques est une marque
de commerce de SNELL Communication Médicale Inc.Tous droits réservés. L’administration d’un traitement thérapeutique décrit ou mentionné dans Ophtalmologie – Conférences scientifiques doit
toujours être conforme aux renseignements d’ordonnance approuvés au Canada. SNELL Communication Médicale se consacre à l’avancement de l’éducation médicale continue de niveau supérieur.
L’élaboration de cette publication a bénéficié d’une subvention à l’éducation de
Novartis Ophthalmics
130-008F
La version française a été révisée par le professeur Pierre Lachapelle,
Montréal.
Les avis de changement d’adresse et les demandes d’abonne-
ment pour Ophtalmologie – Conférences Scientifiques doivent
être envoyés par la poste à l’adresse C.P. 310, Succursale H,
Montréal (Québec) H3G 2K8 ou par fax au (514) 932-5114 ou
par courrier électronique à l’adresse
Veuillez vous référer au bulletin Ophtalmologie – Conférences
Scientifiques dans votre correspondence. Les envois non
distribuables doivent être envoyés à l’adresse ci-dessus.
Poste-publications #40032303
SNELL
Ophtalmologie
Conférences scientifiques
JUIN/JUILLET 2004
Volume 2, numéro 6
COMPTE RENDU DES CONFÉRENCES
SCIENTIFIQUES DU DÉPARTEMENT
D’OPHTALMOLOGIE ET
DES SCIENCES DE LA VISION,
FACULTÉ DE MÉDECINE,
UNIVERSITÉ DE TORONTO
Département d’ophtalmologie
et des sciences de la vision
Faculté de médecine
Université de Toronto
60 Murray St.
Bureau 1-003
Toronto (Ontario) M5G 1X5
Le contenu rédactionnel d’Ophtalmologie –
Conférences scientifiques est déterminé
exclusivement par le Département
d’ophtalmologie et des sciences de la vision,
Faculté de médicine, Université de Toronto.
Département d’ophtalmologie
et des sciences de la vision
Jeffrey Jay Hurwitz, M.D., Rédacteur
Professeur et président
Martin Steinbach, Ph.D.
Directeur de la recherche
The Hospital for Sick Children
Elise Heon, M.D.
Ophtalmologiste en chef
Mount Sinai Hospital
Jeffrey J. Hurwitz, M.D.
Ophtalmologiste en chef
Princess Margaret Hospital
(Clinique des tumeurs oculaires)
E. Rand Simpson, M.D.
Directeur, Service d’oncologie oculaire
St. Michael’s Hospital
Alan Berger, M.D.
Ophtalmologiste en chef
Sunnybrook and Women’s College
Health Sciences Centre
William S. Dixon, M.D.
Ophtalmologiste en chef
The Toronto Hospital
(Toronto Western Division and
Toronto General Division)
Robert G. Devenyi, M.D.
Ophtalmologiste en chef
Oncologie oculaire :
Le mélanome malin de la conjonctive
PAR HUGH D. MCGOWAN, M.D.
Le mélanome malin de la conjonctive/cornée est une tumeur maligne rare des
mélanocytes conjonctivaux, dont le traitement peut avoir un impact sur la survie. La dis-
tinction entre le mélanome malin de la conjonctive et d’autres tumeurs mélanocytaires
de la conjonctive est fondée sur certaines caractéristiques cliniques de la tumeur. La
prise en charge appropriée de cette tumeur nécessite de comprendre l’anatomie et l’his-
tologie normales de la cornée et de la conjonctive, ainsi que de connaître les principes de
l’oncothérapie des tumeurs. Le traitement est axé sur l’excision de la tumeur avec une
« manipulation minimale » accompagnée d’une cryothérapie adjuvante. Toutefois, on a
découvert récemment que la chimiothérapie topique et l’immunothérapie pouvaient
également jouer un rôle dans le traitement. On a de plus en plus recours à la biomicro-
scopie ultrasonique (UBM) pré-opératoire dans l’exploration des marges chirurgicales.
Le mélanome conjonctival est associé à un taux de morbidité et de mortalité élevé et
l’exploration des ganglions lymphatiques sentinelles joue un rôle de plus en plus impor-
tant dans la stadification de la tumeur.
Physiopathologie
Le mélanome malin de la conjonctive se développe aux dépens des mélanocytes issus du
neuroectoderme dans la couche basale de la conjonctive et peut manifester une variabilité
clinique importante. La majorité d’entre eux (60 à 75 %) se développent dans la mélanose
primitive acquise (PAM), 20 à 25 % dans des naevi conjonctivaux préexistants (naevi de jonc-
tion ou composés) et 10 à 25 % se développent de novo dans l’épithélium conjonctival
d’apparence normale
1-3
. La majorité d’entre eux (> 90 %) sont de nature mélanotique, mais
certains peuvent se présenter sous la forme de tumeurs amélanotiques.
Incidence
Les tumeurs conjonctivales surviennent plus fréquemment chez les sujets de type
Caucasien que chez les sujets issus de races à la peau pigmentée
4
, avec une médiane à
62 ans ou l’incidence homme/femme est égale
1
. Au Danemark, l’incidence annuelle est de
0,052 cas/100 000 comparée à 0,6 cas/100 000 pour le mélanome uvéal. Singh et al. ont fait
état d’une incidence annuelle ajustée en fonction de l’âge de 0,012 cas/100 000 des États-
Unis
6
. Le mélanome conjonctival représente seulement 2 % de l’ensemble des tumeurs
malignes oculaires. Comme pour le mélanome cutané, des données publiées par le pro-
gramme Surveillance, Epidemiology and End Results (SEER) du National Cancer Institute
(NCI) aux États-Unis indiquent que l’incidence du mélanome conjonctival a augmenté entre
1973 et 1999, en particulier chez les patients de sexe masculin, de race blanche et âgés de
plus de 60 ans
5
. Cela peut conduire à penser que l’exposition aux rayons ultraviolets joue un
rôle dans l’étiologie de ces tumeurs.
Mortalité et morbidité
Les estimations de la mortalité globale à 10 ans, liée à la tumeur, sont de 25 à 26 %
1
. Une
étude menée par Paridaens et al a mis en évidence un taux de survie à 5 ans de 83 à 84 % et
un taux de survie à 10 ans compris entre 69 et 80 %. Shields et al ont déterminé que le taux
de mortalité à 5 et 8 ans était respectivement de 7 % et 13 % (tableau 1)
2
. Les taux de
récidive étaient de 39 % à 5 ans dans l’étude de Moorfields
3
et de 26 % à 5 ans et de 51 % à
10 ans dans l’étude Philadelphie
2
. La morbidité à 5 ans, mesurée par le taux des métastases
et la fréquence des exentérations, était respectivement de 16 % et de 8 %. Les facteurs de
MC
Département
d’ophtalmologie et des
sciences de la vision
FACULTY OF MEDICINE
University of Toronto
Disponible sur Internet à :
www.ophtalmologieconferences.ca
risque de décès, faisant appel à une analyse multivariée,
comprenaient les symptômes (reflétant la taille de la
tumeur) (p = 0,004) et la pathologie du mélanome malin
qui se développe de novo (p = 0,05)
2
.
Évaluation clinique
Anamnèse
L’anamnèse du développement d’un mélanome con-
jonctival est essentielle et varie selon l’origine et la locali-
sation de la tumeur. Les mélanomes qui se développent
de novo dans le limbe cornéen présentent généralement
une courte phase de croissance horizontale suivie d’une
phase de croissance verticale plus rapide. Les méla-
nomes qui se développent à partir de naevi préexistants
présentent une croissance et une vascularité accrue de
la lésion d’origine (figure 1). L’épaississement nodulaire
suivi d’une vascularité accrue et de l’adhérence au tissu
scléral sous-jacent marquent le début de la dégénéres-
cence maligne en mélanose primitive acquise.
Diagnostic différentiel
Les tumeurs qui proviennent de mélanocytes de la
conjonctive comprennent le naevus, qui est le plus
fréquent (figure 2), la mélanose raciale, la mélanose
primitive acquise et le mélanome malin
1
.
Le diagnostic différentiel d’une pigmentation con-
jonctivale accrue comprend la mélanocytose oculaire, le
ptérygion pigmenté/la pinguécula ; le syndrome d’Axen-
feld-Rieger, les collyres contenant des sels d’argent, le
mascara, le pigment adénochrome, l’ochronose et
l’alcaptonurie
1
. Le tableau clinique du pseudomélanome
peut se présenter comme une extension extrasclérale du
mélanome du corps ciliaire (CC) (figure 3), un staphy-
lome antérieur de la sclérotique, un corps étranger sub-
conjonctival avec hémosidérose, des plaques de Cogan
à l’insertion des muscles droits et des kystes sub-
conjonctivaux hémorragiques suite à un traumatisme
ou à une chirurgie
1
.
Biomicroscopie avec une lampe à fente
L’évaluation clinique avec une lampe à fente doit
permettre de préciser la taille, la localisation, la mobilité
conjonctivale, la vascularité de la tumeur ainsi que son
association avec des naevi conjonctivaux ou une
mélanose primitive acquise (PAM). Une localisation
dans la conjonctive bulbaire est la plus fréquente, mais
la tumeur peut se développer également dans le fornix,
la conjonctive palpébrale et la conjonctive tarsienne
ainsi que dans la caroncule.
Biomicroscopie ultrasonique (UBM)
La biomicroscopie ultrasonique à haute fréquence
(50 MHz) du mélanome conjonctival permet de mesurer
précisément l’épaisseur de la tumeur, celle-ci pouvant
être considérée comme un prédicteur de la survie
6
.
L’imagerie préopératoire permet de préciser le degré
d’extension de la tumeur aux structures de la cornée
(membrane de Bowman intacte, envahissement du
stroma) et le degré d’extension à la sclérotique sous-
jacente (envahissement scléral, atteinte de la veine émis-
saire; figure 4). Les mélanomes nodulaires du limbe
types se présentent sous la forme d’une masse solide
avec une réflectivité interne de faible degré, alors que
les tumeurs plus diffuses s’étendent sur une plus grande
surface et les marges sont souvent difficiles à délimiter
avec précision
6
.
La biomicroscopie ultrasonique préopératoire peut
aider le chirurgien ophtalmologiste à prendre une
décision sur le type et l’étendue de la kératectomie
Tableau 1 : Risque de récidive de la tumeur locale,
d’exentération, de métastases et de décès chez
des patients atteints d’un mélanome conjonctival
2
Durée du suivi
Résultat ±5 ans ±10 ans ±15 ans
Récidive (%) 26 51 65
Exentération (%) 8 16 32
Métastases (%) 16 26 32
Décès (%) 7 13 ND
ND = non disponible
Figure 1: Mélanome conjonctival du limbe type
1a : Mélanome conjonctival du limbe présentant une lésion de la
cornée et une vascularité accrûe.
1b : Cliché de biomicroscopie ultrasonique (UBM) montrant la
composante cornéenne d’une tumeur (flèche plus épais) avec
une membrane de Bowman intacte (petite flèche).
1c : Cliché histopathologique montrant des îlots de cellules de
mélanome (grosse flèche) se substituant à toutes les couches
normales de l’épithélium conjonctival.
1a
1c1b
Figure 2: Naevus conjonctival type observé au
niveau du limbe chez une jeune femme de 14 ans.
2a : L’examen avec une lampe à fente du naevus peut laisser
apparaître des modifications kystiques caractéristiques.
2b : Cliché histopathologique montrant des cellules du naevus
dans le stroma (flèche plus épais) sous un épithélium
conjonctival (petite flèche).
2a
2b
l’épithélium ont tendance à se développer en îlots
irréguliers. La tumeur peut se propager au stroma sous-
jacent et remplacer toutes les couches de l’épithélium
conjonctival normal
7
. Les cellules du mélanome sont
plus grandes que celles du naevus. Elles ont un gros
noyau avec une agglutination de chromatine à la
périphérie de la membrane nucléaire et ont des
nucléoles éosinophiliques distincts. Ce peut être des
superficielle et/ou de la sclérectomie superficielle néces-
saire au moment de l’excision initiale de la tumeur.
Biopsie diagnostique et stadification
Les mélanomes du limbe classiques doivent faire
l’objet d’une excision chirurgicale complète (technique
« sans contact ») associée à une cryothérapie des marges
de résection sans tumeur. La technique du traitement
chirurgical initial constitue un important facteur de
réduction de la récidive (p = 0,07), des métastases
(p = 0,03) et de la mortalité (p = 0,006), mais une valeur
statistiquement significative n’a été conservée qu’en
analyse univariée
2
.
La stadification comprend une classification clini-
que et une classification pathologique décrites par
l’American Joint Committee on Cancer. Elle est applicable
au mélanome conjonctival caractérisé par une histoire
naturelle d’extension aux ganglions lymphatiques
régionaux et de maladie métastasique subséquente. Il
n’en va pas de même du mélanome uvéal pour lequel
l’état ganglionnaire n’est pas pertinent, étant donné l’ab-
sence de drainage lymphatique de l’orbite postérieure
au septum orbitaire.
Stadification
La classification clinique des mélanomes conjoncti-
vaux est présentée au tableau 2, alors que la classifica-
tion pathologique est présentée dans le tableau 3. Il
n’existe actuellement pas de groupe identifiant le stade.
La désignation du type histopathologique est le « méla-
nome malin de la conjonctive ».
Pour le stade histopathologique, qui représente la
tumeur primitive, les appellations suivantes sont
utilisées :
• GX – L’origine ne peut être évaluée
• G0 – Mélanose primitive acquise (PAM)
• G1 – Mélanome malin provenant d’un naevus
• G2 – Mélanome malin provenant d’une mélanose
primitive acquise
• G3 – Mélanome malin développé de novo.
Résultats histopathologiques
Dans le mélanome malin de la conjonctive, des
mélanocytes anormaux près de la couche basale de
Figure 3 : Extension extrasclérale d’un mélanome du
corps ciliaire (CC) simulant le mélanome conjonctival
3a : Image reflex rouge montrant un mélanome du corps ciliaire et
un nodule scléral pigmenté (flèche).
3b : Grossissement plus important du nodule scléral.
3c : Cliché de biomicroscopie ultrasonique montrant la connexion
d’une veine émissaire entre la tumeur intraoculaire et le nodule
scléral (flèche) (reproduit avec l’aimable autorisation du
Dr C. J. Pavlin)
3a 3b 3c
Tableau 3 : La classification pathologique des
mélanomes conjonctivaux
Tumeur primitive (pT)
pTX La tumeur primitive ne peut être explorée
pT0 Aucune preuve de tumeur primitive
pT1 Tumeur(s) de la conjonctive bulbaire,
≤ 1 quadrant, < 2 mm d’épaisseur
pT2 Tumeur(s) de la conjonctive bulbaire,
>1 quadrant, ≤ 2 mm d’épaisseur
pT3 Tumeur(s) du fornix conjonctival, de la
conjonctive palpébrale ou de la caroncule, > 2 mm
pT4 Tumeur envahissant la paupière, la cornée et l’orbite
Ganglions lymphatiques régionaux (pN)
pNX Les ganglions lymphatiques régionaux ne peuvent
être explorés
pN0 Aucune métastase des ganglions lymphatiques
régionaux
pN1 Métastases des ganglions lymphatiques régionaux
Métastases distantes (pM)
pMX Les métastases distantes ne peuvent être explorées
pM0 Aucune métastase distante
pM1 Métastases distantes
AJCC, Cancer Staging Manual, 5
e
édition;1998.
American Joint Committee on Cancer (AJCC), Cancer Staging Manual,
5
e
édition;1998.
Tableau 2 : La classification clinique (cTNM) des
mélanomes conjonctivaux
Tumeur primitive (T)
TX La tumeur primitive ne peut être explorée
T0 Aucune preuve de tumeur primitive
T1 Tumeur(s) de la conjonctive bulbaire, ≤ 1 quadrant
T2 Tumeur(s) de la conjonctive bulbaire, >1 quadrant
T3 Tumeur(s) du fornix conjonctival, de la conjonctive
palpébrale ou de la caroncule
T4 Tumeur envahissant la paupière, la cornée et l’orbite
Ganglions lymphatiques régionaux (N)
NX Les ganglions lymphatiques régionaux ne
peuvent être explorés
N0 Aucune métastase des ganglions lymphatiques
régionaux
N1 Métastases des ganglions lymphatiques régionaux
Métastases distantes (M)
MX Les métastases distantes ne peuvent être explorées
M0 Aucune métastase distante
M1 Métastases distantes