Les troubles de l’intégration visuelle - part 2 doc
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (658.18 KB, 19 trang )
aux commentaires sur leur air « fatigué » ou « épuisé », mais
il s’agit véritablement d’un problème fonctionnel chez les
patients qui doivent soulever à la main l’excès de peau pour
dégager leur axe visuel. Le patient peut également remar-
quer une perte de son acuité visuelle centrale ou une
diminution de son champ visuel central ou périphérique,
lesquelles sont attribuables à l’obstruction mécanique
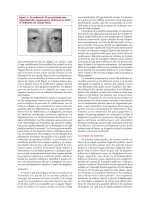
directe du champ visuel (Figure 1). Certaines femmes peu-
vent se plaindre d’avoir de la difficulté à appliquer du fard
et du mascara sur leurs paupières supérieures. Les plaintes
peuvent aussi porter sur la céphalée en casque ou la
migraine, causées par la sur-utilisation chronique des mus-
cles frontaux.
L’étiologie de l’hyperélasticité cutanée et un grand nom-
bre des changements observés dans la région périorbitaire
sont secondaires au processus de vieillissement. Avec le
temps, le collagène que contiennent les minces tissus des
paupières subit une dégénérescence due aux rayons ultravi-
olets (UV) et au vieillissement. Les collagénases, provenant
de l’épiderme endommagé, contribuent également à la
dégénérescence et à l’enchevêtrement des fibres de col-
lagène individuelles
3
. Les fibres élastiques sous-jacentes sont
aussi endommagées par l’exposition aux rayons UV solaires,
bien qu’une grande proportion de ces dommages se soit déjà
produite pendant la jeunesse
4
. Les forces gravitationnelles
jouent aussi un rôle important dans la redondance des tis-
sus. Le vieillissement chronologique est accompagné d’un
affaissement mécanique des sourcils et de la graisse rétro-
orbiculaire des paupières (GROP), ce qui contribue à la
redondance tissulaire de la paupière supérieure. La contrac-
tion répétée des muscles orbiculaires pendant de nom-
breuses années contribue à l’étirement septal orbitaire, à
l’atténuation et au prolapsus graisseux. Le prolapsus grais-
seux est plus communément observé dans la partie médiale
des paupières supérieures, et dans les parties centrale et
latérale des paupières inférieures. L’hérédité et d’autres fac-
teurs environnementaux, tels que le tabagisme et la nutri-
tion, peuvent également contribuer à l’aspect des paupières.
Évaluation
L’examen ophtalmologique permet au médecin de
déterminer si le patient est un candidat qualifié à la
chirurgie. L’évaluation de l’acuité visuelle et du champ
visuel, avec les paupières en leur état naturel et avec l’ex-
cès de tissu soulevé, est essentielle pour consigner l’impor-
tance des déficits de l’acuité visuelle et (ou) du champ
visuel attribuables à l’hyperélasticité cutanée. L’évaluation
de la ptôse peut être difficile en présence d’une importante
hyperélasticité cutanée, mais elle est essentielle, car la véri-
table ptôse n’est pas traitée au moyen des techniques stan-
dard de blépharoplastie.
L’évaluation de la motilité extraoculaire est importante
pour déceler des déficits fonctionnels dans la verticalité du
regard. L’utilité d’effectuer un test préopératoire de Schirmer
demeure controversée; il peut toutefois fournir d’impor-
tants renseignements sur l’état du film lacrymal
5
. Un exa-
men à la lampe à fente pour déceler une lagophtalmie, une
kératite ponctuée superficielle et une érosion récidivante de
la cornée est utile pour consigner l’état du film lacrymal. Un
examen des paupières inférieures peut révéler diverses
combinaisons d’herniation graisseuse orbitaire, de rhytides
ou d’excès de peau de la paupière inférieure. Il est essentiel
d’examiner les paupières inférieures afin d’y déceler tout
signe de laxité et de rétraction préexistante. Une importante
laxité de la paupière inférieure peut prédisposer les patients
à une rétraction de la paupière inférieure et à une manifes-
tation sclérale si elle n’est pas corrigée avant ou pendant la
blépharoplastie.
Un traitement préopératoire permet l’identification de
variables pouvant potentiellement mener à un résultat
chirurgical non optimal. Le médecin doit, d’abord et avant
tout, déterminer dans quelle mesure le patient a des objec-
tifs réalistes et des attentes raisonnables, et si la blépharo-
plastie seule constitue ou non l’intervention de choix pour
régler ces problèmes. Les patients sont avisés d’éviter
l’aspirine, l’ibuprofen et tout médicament similaire au
moins pendant les deux semaines précédant l’intervention,
car ces médicaments peuvent causer des saignements pen-
dant et après l’opération. Il est important d’interroger les
patients sur leur consommation de médicaments à base
d’herbes, car les constituants tels que le gingembre, le
gingko et le ginseng asiatique sont connus pour accroître le
saignement pendant les opérations chirurgicales
6
. Des
agents antiviraux prophylactiques sont administrés
lorsqu’un resurfaçage au laser à gaz carbonique (CO
2
) doit
être effectué. Les patients sont également avisés qu’ils
doivent cesser de fumer, car la cigarette réduit la circulation
cutanée et entrave la cicatrisation.
Les principes du traitement
De manière traditionnelle, une incision cutanée au
moyen d’un scalpel constituait l’approche préférée, mais il
existe de nouvelles options, dont des appareils à haute
fréquence et des lasers à gaz carbonique. L’approche chirur-
gicale visant à enlever l’excès de gras dans les paupières
inférieures a également connu un changement de para-
digme. L’approche sous-ciliaire de la blépharoplastie
inférieure constitue la norme supérieure pour corriger l’hy-
perélasticité cutanée de la paupière inférieure et elle peut
toujours constituer l’intervention la plus appropriée dans
certains cas. Cependant d’autres approches ont été adoptées
lorsqu’il a été reconnu que l’approche sous-ciliaire causait
une rétraction de la paupière inférieure et des manifesta-
tions sclérales chez certains patients
7
.La re-suspension
simultanée du canthus externe, en plus de la blépharoplas-
tie sous-ciliaire, a également été prônée pour réduire l’inci-
dence de rétraction de la paupière inférieure. De nombreux
chirurgiens ont opté pour la blépharoplastie inférieure
Figure 1 : Ce patient de 70 ans présente une
hyperélasticité cutanée grave obstruant sa vision
et réduisant son champ visuel.
La technique de blépharoplastie
inférieure transconjonctivale
L’approche chirurgicale transconjonctivale constitue
l’intervention de choix en présence de poches graisseuses
particulièrement importantes sans excès de peau ni
rhytides profondes. Les importantes poches graisseuses
devraient idéalement être marquées alors que le patient est
en position verticale, car leur importance s’amenuise une
fois le patient en position couchée. Après l’application de
gouttes topiques de proparacaïne dans le fornix conjoncti-
val, l’anesthésie locale est pratiquée de manière transcon-
jonctivale dans les poches graisseuses. Un écarteur de
Desmarres est utilisé pour écarter la paupière inférieure, et
une plaque palpébrale est insérée dans le fornix inférieur
afin de protéger le globe oculaire. Tous les instruments
utilisés lors d’une blépharoplastie avec laser à CO
2
doivent
être non-réfléchissants. Une incision à travers la conjonc-
tive et les écarteurs de la paupière inférieure est alors pra-
tiquée au moyen du laser à CO
2
, environ 5 mm sous la
bordure tarsienne inférieure. Les poches graisseuses médi-
ale, centrale et latérale sont identifiées par dissection addi-
tionnelle à travers les écarteurs de la paupière inférieure.
La visualisation du gras peut être optimisée en appliquant
une légère pression sur le globe oculaire. Les poches grais-
seuses orbitaires sont excisées en portant une attention
particulière à l’hémostase. Le modelage des poches grais-
seuses médiale et centrale doit être effectué avec un soin
particulier, car le muscle oblique inférieur s’étend entre
elles et un traumatisme à ce muscle peut mener à la
diplopie. La paupière inférieure est ensuite remise à sa
position d’origine, et son contour est réévalué. Au besoin,
une plus grande quantité de gras peut être excisée des
régions dominantes ou, inversement, des perles de gras
peuvent être réintroduites dans des régions plus affaissées
de la paupière inférieure.
Si un resurfaçage d’appoint au laser à CO
2
doit être
effectué, une nouvelle anesthésie infiltrante sous-cutanée
est pratiquée. Un protecteur scléral métallique non
réfléchissant est placé sur le globe oculaire, et le resurfaçage
est effectué au moyen d’un laser à CO
2
dont les paramètres
sont spécifiquement établis par le chirurgien. Les rhytides
sont traitées de manière confluante, perpendiculairement à
la marge de la paupière. Les débris sont ensuite doucement
enlevés à l’aide de gaze imbibée de solution saline. Au
besoin, d’autres passages peuvent être effectués pour
obtenir le degré de traitement et le resserrement cutané
voulus. Enfin, un onguent antibiotique et des pansements
de Cellophane sont appliqués sur les régions resurfacées
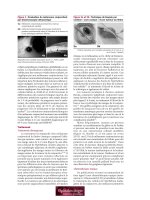
(Figure 3).
transconjonctivale afin de réduire l’incidence de telles com-
plications. La blépharoplastie transconjonctivale a l’avan-
tage de permettre l’excision et le retrait du gras avec un
risque nettement moindre de rétraction de la paupière
inférieure.
À l’occasion, le retrait du gras dans la paupière
inférieure peut entraîner la formation accrue de fines rides
et la redondance de la peau des paupières inférieures,
compte tenu de l’étirement chronique de la peau. Ces fines
rhytides sont difficiles à traiter au moyen des techniques
de blépharoplastie traditionnelles et, pour cette raison,
le resurfaçage superficiel au laser a été prôné comme
traitement d’appoint à la blépharoplastie. Carter et al ont
démontré que la combinaison de la blépharoplastie
transconjonctivale avec le resurfaçage d’appoint au laser à
CO
2
réduit l’incidence de rides postopératoires et améliore
l’aspect cosmétique ultime
8
.
La technique de blépharoplastie supérieure
Au moins 10 mm de paupière devraient être laissés
entre l’incision supérieure et les poils les plus bas du sour-
cil, car une résection cutanée excessive peut tirer le sourcil
vers le bas ou causer des problèmes d’occlusion de la
paupière. Une prémédication de 5 à 10 mg de midazolam
peut être administrée 15 minutes avant l’intervention. Une
anesthésie locale composée de 2 % de lidocaïne combinée à
de l’épinéphrine et à de l’hyaluronidase dosées à 1:100 000
est utilisée en infiltration sous-cutanée. Un scalpel ou le
laser à CO
2
est utilisé pour pratiquer les incisions cutanées,
lesquelles suivent avec précision les contours des marques
préopératoires. La peau et le muscle orbiculaire sont excisés
en une seule couche pour exposer la cloison orbitaire. Une
hémostase méticuleuse est essentielle. Une fois la cloison
orbitaire incisée, le gras pré-aponévrotique est visible,
recouvrant l’aponévrose du muscle releveur. Le gras est
doucement séparé de ses attaches à l’aponévrose du muscle
releveur sous-jacente, puis excisé au moyen de techniques
hémostatiques. L’excision hémostatique du gras peut être
effectuée au moyen d’un cautère portatif, d’appareils à
haute fréquence, d’un cautère bipolaire ou de lasers. Un
modelage plus approfondi de la graisse rétro-orbiculaire des
paupières (GROP) peut également être nécessaire dans cer-
tains cas. Une fois l’hémostase adéquate terminée, la suture
peut être effectuée au moyen de catgut 6-0 non absorbable
ou rapidement résorbable. L’utilisation de fixations sus-tar-
siennes lors de la suture finale permet la création d’un sillon
agréable sur le plan cosmétique alors que les tissus cica-
trisent (Figure 2).
Figure 3 : Aspect A. préopératoire et B. six mois
après l’intervention d’un patient ayant subi une
blépharoplastie transconjonctivale inférieure au
moyen d’un resurfaçage au laser à CO
2
.
Figure 2 : Photos A. avant l’opération et
B. quatre mois après l’intervention d’un
patient présentant une hyperélasticité cutanée
modérée de la paupière supérieure après
une blépharoplastie simple.
AB
AB
Soins postopératoires
Des compresses fraîches et un onguent antibio-
tique topique constituent le principal traitement au
cours de la période qui suit immédiatement l’interven-
tion. Des antibiotiques systémiques et des corti-
costéroïdes à dose rapidement dégressive peuvent
également être prescrits sur une base individuelle. Les
patients qui subissent régulièrement un resurfaçage au
laser reçoivent des antibiotiques systémiques, des
antiviraux et, souvent, de la prédnisone après l’inter-
vention. Ces patients doivent en outre s’assurer de
protéger toutes les régions traitées contre le soleil.
L’enlèvement des points de suture, le cas échéant, se
fait généralement cinq à sept jours après l’intervention.
Les patients sont avisés d’éviter toute activité physique
intense pendant la première semaine suivant l’opéra-
tion afin de réduire l’incidence d’hématomes et
d’œdème postopératoires.
Complications
La complication la plus dévastatrice après une
blépharoplastie est l’hémorragie orbitaire doublée de
cécité. On rapporte une incidence de 0,04 %, bien que
ce chiffre corresponde sans doute à une sous-estima-
tion compte tenu du manque de données rapportées.
L’étiologie peut être multifactorielle, mais elle inclut
probablement une traction excessive des poches grais-
seuses antérieures combinée à de mauvaises hémostase
et visualisation peropératoires. Ceci provoque une
compression du nerf optique et une ischémie se-
condaire du nerf optique. Le traitement comprend le
diagnostic précoce, une canthotomie et une cantho-
lyse latérales et l’administration d’agents systémiques
antihypertenseurs pour soulager l’ischémie. Bien que
cela soit rare, il arrive qu’une décompression orbitaire
soit nécessaire. Les complications localisées dans les
tissus mous sont plus souvent associées à un excès de
peau ou au retrait de gras plutôt qu’à une insuffisance
de peau et au retrait de gras. Des cas de lagophtalmie
légère peuvent se produire, lesquels sont généralement
résolus après une chirurgie de la paupière, mais une
lagophtalmie prononcée peut causer une irritation
oculaire, une kératite lagophtalmique et une kératite
infectieuse. Ceci peut être aggravé par des dommages
causés par inadvertance à la glande lacrymale, allant
jusqu’à l’excision, pendant la chirurgie. Un sillon
supérieur plus affiné peut être plus acceptable chez les
femmes que chez les hommes, mais un retrait excessif
de gras peut se traduire par un sillon supérieur creux
peu seyant. Des plis multiples ou asymétriques au
niveau de la paupière peuvent être le résultat d’un
mauvais marquage préopératoire ou d’une incision
pratiquée au mauvais endroit.
Lors du rajeunissement de la paupière inférieure,
le retrait de l’excès de peau en présence d’une laxité
horizontale de la paupière peut résulter en un « œil
rond » avec dystopie et ectropion du canthus latéral. La
résolution de ce problème peut nécessiter un relâche-
ment lamellaire moyen, la mise en place d’une pièce
d’espacement au niveau de la lamelle postérieure, une
re-suspension médiofaciale ou, à l’occasion, une greffe
cutanée au niveau de la lamelle antérieure. Enfin,
compte tenu de la proximité du muscle oblique
inférieur avec la poche graisseuse centrale de la
paupière inférieure, une diplopie passagère peut égale-
ment se produire après l’intervention.
Remodelage endoscopique du sourcil
Le rôle de la position des sourcil dans l’esthétique
médiofaciale a été largement ignoré et mésestimé.
Leurs mouvements clés influent profondément sur
l’animation et l’expression faciales. Dans la mesure où
ils occupent les limites supérieures de la région médio-
faciale, une position anormale peut causer une asymé-
trie et engendrer des problèmes esthétiques et
fonctionnels. Comme dans le cas de la chirurgie de la
paupière, l’objectif du rajeunissement des sourcils est
de donner à la région périorbitaire un nouvel aspect de
jeunesse. La correction de la ptôse du sourcil peut
également contribuer à améliorer les lignes et sillons
horizontaux, grâce au retrait des muscles et tissus qui
causent le froncement.
Pendant des décennies, le remodelage du sourcil
par ouverture coronale a constitué la norme par excel-
lence du rajeunissement du front. Les chirurgiens ont
favorisé cette méthode car elle permet de clairement
exposer l’ensemble des structures anatomiques impor-
tantes, en particulier pour ceux ne disposant pas des
instruments endoscopiques appropriés ou qui ne se
sentent pas à l’aise avec cette technologie ou avec la
courbe d’apprentissage sous-jacente. Bien que certains
chirurgiens favorisent toujours cette technique pour
le rajeunissement du front, il est clair que l’approche
endoscopique est de plus en plus favorisée. La tech-
nique endoscopique a évolué avec la mise en applica-
tion d’interventions de rajeunissement facial plus
complexes
9
. En fait, certains rapports donnent à
penser que les résultats de cette approche peuvent
équivaloir, voire surpasser, d’autres méthodes de
rajeunissement du front
10,11
. L’approche endoscopique
présente des avantages très nets, dont des incisions
plus petites, ce qui réduit la cicatrisation, l’engour-
dissement, le saignement, l’alopécie et donne lieu à
une période de récupération beaucoup plus courte
qu’avec l’approche coronale.
Évaluation
Il est encore une fois essentiel de déterminer quels
candidats se qualifient pour cette intervention. Les
patients qui affirment que hausser les sourcils
améliore leur vision peuvent effectivement nécessiter
une blépharoplastie et (ou) une réparation de la ptôse.
Un remodelage du sourcil en présence de ptôse ne
dégagera en aucun cas les paupières de l’axe visuel. De
même, le patient présentant une hyperélasticité
cutanée et une ptôse involutive du sourcil et optant
pour la blépharoplastie seule doit comprendre qu’un
nouvel affaissement du sourcil peut se produire après
l’intervention. Outre l’examen soigneux du contour et
Ophtalmologie
Conférences Scientifiques
de la position du sourcil, l’évaluation de la position de
la ligne de contour de la chevelure est également
essentielle, car les patients ayant une ligne de contour
très élevée pourraient tirer un meilleur parti d’une
approche endoscopique que d’une ouverture coronale.
Enfin, il faut tenir compte des différences entre les con-
tours des sourcils : les sourcils des hommes ont un
profil relativement plat et bas, alors que ceux des
femmes ont généralement le tiers latéral arqué.
Technique
Le remodelage endoscopique du sourcil peut être
effectué sous anesthésie générale ou sous sédation
consciente. Une sédation intraveineuse de midazolam
et de fentanyl et une analgésie locale combinant des
agents d’action brève et longue peuvent procurer une
anesthésie suffisante pour la durée de l’intervention.
Des anesthésies tronculaires locales et des injections
dans un garrot vasculaire permettent de maintenir
l’hémostase pendant l’intervention. Cinq incisions sont
généralement pratiquées dans le cuir chevelu : 1 inci-
sion centrale, 2 incisions paracentrales et 2 incisions
temporales. Les incisions sont pratiquées vers le bas,
au centre jusqu’au périoste et à travers la peau et le
tissu sous-cutané au niveau de la couche superfi-
cielle de l’aponévrose profonde temporale. Puisque
l’approche endoscopique repose beaucoup sur les
instruments permettant la visualisation, un plan de
dissection sous-périosté relativement sans saignement
est idéal et permet un accès facile à tous les repères
clés (Figure 4).
Bien que de nombreux facteurs importants soient
associés à la chirurgie endoscopique du sourcil, aucun
n’est plus critique que la compréhension du trajet du
nerf facial dans les diverses couches du tissu conjonctif.
Tout dommage porté à ce nerf le long des branches
frontales ou zygomatiques peut entraîner une paralysie
faciale permanente. Pour obtenir une mobilité complète
du cuir chevelu, la dissection temporale des cavités doit
être liée à la dissection centrale sous-périostée des
cavités. Un plan de dissection temporal à central assure
que le nerf facial demeure en superficie et qu’il ne
risque pas d’être endommagé par inadvertance.
La libération périostique est également un facteur
important de tout remodelage endoscopique du sour-
cil. Une libération périostique adéquate tout le long
des bords sus-orbitaires permet la mobilité complète
du lambeau musculo-cutané. Ceci nécessite la dissec-
tion jusqu’à l’occiput et d’une oreille à l’autre pour per-
mettre ensuite la mobilisation complète du cuir
chevelu. La libération périostique endoscopique peut
être effectuée au moyen du laser à CO
2
, d’un dis-
secteur périostique affilé ou de pinces à dissection
endoscopiques. Les muscles sourcilier et procerus
doivent en outre être complètement libérés afin
d’obtenir un contour frontal lisse et permettre ainsi le
remodelage médial des sourcils. Auparavant, cette
opération était traditionnellement pratiquée au moyen
de pinces à dissection endoscopiques, mais les expéri-
ences d’ablation à l’aide d’un laser endoscopique à CO
2
ont démontré que cette méthode était supérieure à la
résection manuelle
12
. Le laser permet à la fois une
hémostase contrôlée et le relâchement des dépresseurs
sourciliers coagulés. De plus, la résection accrue du
muscle glabellaire au moyen de toxine botulinique A
peropératoire peut procurer un relâchement durable
pendant l’adhérence périostique.
L’étape finale d’un remodelage endoscopique effi-
cace du sourcil est la fixation à la calotte crânienne,
dont les modes absorbable et permanent ont été
décrits. Des vis de fixation au titane chargées de
sutures de polyglyconate 2-0 peuvent facilement être
insérées dans les deux incisions paracentrales et fixées
au cortex extérieur de la calotte crânienne. Après avoir
enfilé les sutures dans une aiguille libre pour la dure-
mère, le cuir chevelu est placé en tension postérieure,
et l’aiguille est utilisée pour engager le périoste au bord
de l’incision antérieure. La stabilité latérale du sourcil
est assurée par la fixation du lambeau musculo-cutané
au moyen d’une suture d’acide polyglycolique 2-0 à
l’aponévrose temporale. Des agrafes sont utilisées pour
fermer les incisions cutanées supérieures.
Si la ptôse latérale est importante et source de
problème, une résection du cuir chevelu au niveau de
l’incision temporale permet d’obtenir des résultats plus
esthétiques. Cette intervention est parfois nécessaire,
Ophtalmologie
Conférences Scientifiques
Figure 4 : Un plan de dissection vasculaire
sous-périostée utilisé au cours du
remodelage endoscopique du sourcil.
L’endoscope est pointé vers le bord
sus-orbitaire inférieur. La petite flèche
représente l’os frontal, et la grande flèche
pointe vers le périoste réfléchi au-dessus
du faisceau neurovasculaire.
Figure 5 : Photos A. avant l’opération et
B. après l’intervention d’un patient avant et
six mois après un remodelage endoscopique
du sourcil. Remarquez l’aspect plus jeune et
plus détendue de la région périorbitaire.
AB
Références
1. Warwar RE, Bullock JD, Markert RJ, Marciniszyn SL, Bienenfeld DG. Social
implications of blepharoptosis and dermatochalasis. Ophthal Plast Reconstr
Surg 2001;17(4):234-40
2. American Society for Aesthetic Plastic Surgery, 2001 Statistics, Communica-
tions Office, www.surgery.org.
3. Kurban RS, Bhawan J. Histologic changes in skin associated with aging.
JDermatol Surg Oncol 1990;16(10) 908-14.
4. Leyden JJ. Clinical features of aging skin. Br J Dermatol 1990;122 Suppl
35:1-3.
5. Burke AJC, Wang T. Should formal ophthalmic evaluation be a preoperative
requirement prior to blepharoplasty. Arch Otol Head Neck Surg 2001;127:
719-722.
6. Pribitkin E, Boger G. Herbal Therapy: What every facial plastic surgeon
must know. Arch Facial Plast Surg 2001; 3(2):127-132.
7. P erkins SW, Dyer WKT, Simo F. Transconjunctival approach to lower eyelid
blepharoplasty. Experience, indications, and technique in 300 patients. Arch
Otolaryngol Head Neck Surg 1994;120(2):172-7.
8. Carter SR, Seiff SR, Choo PH, Vallabhanath P. Lower eyelid CO2 laser reju-
venation: A randomized prospective clinical study. Ophthalmology
2001;108:437-441.
9. Carter SR, Choo PH. New techniques in eyebrow surgery. Opthalmol Clin N
Am 2000;13:731-748.
10. Steinsapir KD, Shorr N, Hoenig J, et al. The endoscopic forehead lift.Oph-
thalm Plast Reconstr Surg 1998;14:107-118.
11. Ramirez O. Why I prefer the endoscopic forehead lift. Plast Reconstr Surg
1997;100:1033-1039.
12. Choo PH, Carter SR, Seiff SR. Carbon dioxide laser-assisted endoscopic
forehead lift. Plast Reconstr Surg 1999;103(1):294-298.
Réunions scientifiques à venir
24 au 27 janvier 2004
6
e
Congrès international d’oncologie oculaire
Hyderabad, Inde
Renseignements : Arun Singh, MD,
Santosh G. Honavar, MD
Tél. : 91-40-23-548-267
Fax : 91-40-23-548-271
Courriel :
4 au 5 avril 2004
Royal National Institute of the Blind (RNIB)
8
th
International Conference on issues concerning
low vision and sight – Vision 2005 London
Londres, Angleterre
Renseignements : www.rnib.org.uk/vision2005/register
Tél. : 44(0)20 7940 5362
car le tiers latéral des sourcils est soumis à la dépression
non compensée des muscles orbiculaires, et il n’y a pas
latéralement de muscle frontal pour faciliter l’élévation du
sourcil (Figure 5).
Soins postopératoires
Avant leur sortie, les patients se font administrer un
litre entier de Ringer-lactate par voie intraveineuse à l’unité
de soins post-anesthésiques afin de combattre la redistribu-
tion liquidienne qui se produit souvent. L’administration
systématique de corticostéroïdes par voie orale permet de
réduire l’enflure postopératoire, tandis que l’administration
d’antibiotiques prophylactiques par voie orale permet de
réduire l’incidence d’infection. Les agrafes sont retirées une
semaine plus tard.
Complications
Le remodelage endoscopique du sourcil comporte un
minimum de risques et des complications potentielles. Le
risque de paralysie faciale est faible et dépend de la familiar-
ité du chirurgien avec l’anatomie des divers plans tissu-
laires. Le plus souvent, la paralysie faciale est temporaire, et
une guérison est observée dans les trois à six mois. Les fol-
licules pileux sont connus pour être extrêmement sensibles
à la chaleur et à la cautérisation thermale. Une cautérisation
excessive des tissus sous-jacents peut causer des dom-
mages permanents aux follicules et entraîner l’alopécie. Le
chirurgien risque également d’induire l’alopécie s’il pratique
des incisions transversales à travers la base des follicules
pileux et s’il applique une pression excessive en refermant
les plaies opératoires. Quoique rares, une infection et un
saignement peuvent également se produire.
En résumé
Les approches chirurgicales du rajeunissement périor-
bitaire se sont développées avec l’introduction de nouvelles
technologies dans la pratique médicale. Cela suppose égale-
ment une plus grande responsabilité de la part du
chirurgien qui doit se sentir parfaitement à l’aise et avoir
une connaissance approfondie non seulement des instru-
ments, mais aussi de l’anatomie détaillée de ces régions
spécifiques. Avec une évaluation préopératoire appropriée,
une attention consciencieuse portée à la technique per-
opératoire et un traitement postopératoire adéquat, les
complications peuvent être évitées et un résultat optimal
peut être obtenu.
Dan D. DeAngelis, M.D., F.R.C.S.(C) est médecin au service
d’ophtalmologie et des sciences de la vision du Mount Sinai
Hospital, université de Toronto, Toronto (Ontario).
SNELL
© 2003 Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto, seul responsable du contenu de cette publication. Édition : SNELL Communication
Médicale Inc. avec la collaboration du Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto.
MD
Ophtalmologie – Conférences scientifiques est une marque
de commerce de SNELL Communication Médicale Inc.Tous droits réservés. L’administration d’un traitement thérapeutique décrit ou mentionné dans Ophtalmologie – Conférences scientifiques doit
toujours être conforme aux renseignements d’ordonnance approuvés au Canada. SNELL Communication Médicale se consacre à l’avancement de l’éducation médicale continue de niveau supérieur.
L’élaboration de cette publication a bénéficié d’une subvention à l’éducation de
Novartis Ophthalmics
130-003F
La version française a été revisée par le professeur Pierre Lachapelle,
Montréal.
Les avis de changement d’adresse et les demandes d’abonne-
ment pour Ophtalmologie – Conférences Scientifiques doivent
être envoyés par la poste à l’adresse C.P. 310, Succursale H,
Montréal (Québec) H3G 2K8 ou par fax au (514) 932-5114 ou
par courrier électronique à l’adresse
Veuillez vous référer au bulletin Ophtalmologie – Conférences
Scientifiques dans votre correspondence. Les envois non
distribuables doivent être envoyés à l’adresse ci-dessus.
Ophtalmologie
Conférences Scientifiques
JANVIER 2004
Volume 2, numéro 1
COMPTE RENDU DES CONFÉRENCES
SCIENTIFIQUES DU DÉPARTEMENT
D’OPHTALMOLOGIE ET
DES SCIENCES DE LA VISION,
FACULTÉ DE MÉDECINE,
UNIVERSITÉ DE TORONTO
Département d’ophtalmologie
et des sciences de la vision
Faculté de médecine
Université de Toronto
60 Murray St.
Bureau 1-003
Toronto (Ontario) M5G 1X5
Le contenu rédactionnel d’Ophtalmologie –
Conférences scientifiques est déterminé
exclusivement par le Département
d’ophtalmologie et des sciences de la vision,
Faculté de médicine, Université de Toronto.
Département d’ophtalmologie
et des sciences de la vision
Jeffrey Jay Hurwitz, M.D., Rédacteur
Professeur et président
Martin Steinbach, Ph.D.
Directeur de la recherche
The Hospital for Sick Children
Elise Heon, M.D.
Ophtalmologiste en chef
Mount Sinai Hospital
Jeffrey J. Hurwitz, M.D.
Ophtalmologiste en chef
Princess Margaret Hospital
(Clinique des tumeurs oculaires)
E. Rand Simpson, M.D.
Directeur, Service d’oncologie oculaire
St. Michael’s Hospital
Alan Berger, M.D.
Ophtalmologiste en chef
Sunnybrook and Women’s College
Health Sciences Centre
William S. Dixon, M.D.
Ophtalmologiste en chef
The Toronto Hospital
(Toronto Western Division and
Toronto General Division)
Robert G. Devenyi, M.D.
Ophtalmologiste en chef
La biomicroscopie ultrasonographique
PAR CHARLES
J. PAVLIN, M.D.
L’échographie est un outil indispensable dans l’imagerie médicale qui joue un rôle
important dans les diagnostics ophtalmologiques. L’échographie mode B conventionnelle
produit des vues transversales bidimensionnelles de l’œil et de l’orbite. Cette méthode d’im-
agerie est la technique d’examen la plus importante pour les lésions intraoculaires, en parti-
culier en présence d’opacités du segment antérieur. Cependant, l’échographie
conventionnelle a des limites, en particulier dans le domaine de la résolution. Afin de mieux
comprendre les mécanismes des maladies oculaires, on a sans cesse besoin d’une résolution
plus élevée. Tout comme la microscopie optique a amélioré notre compréhension des
processus de base, une meilleure résolution de l’image nous permet de voir et de compren-
dre des processus nouveaux. Les principes physiques et les techniques de base des ultrasons
à plus haute fréquence pour visualiser des structures vivantes ont été mis au point dans les
laboratoires de Stuart Foster à l’Université de Toronto. Nous avons ultérieurement appliqué
ces techniques à l’imagerie oculaire et appelé ce processus « la biomicroscopie ultrasono-
graphique
1-3
» (BMU), c’est-à-dire l’imagerie des structures vivantes à une résolution micro-
scopique. Dans ce numéro d’
Ophtalmologie – Conférences scientifiques
, nous examinons les
fondements de cette méthode d’imagerie et illustrons comment l’utilisation de la résolution
microscopique pour voir en-dessous de la surface de l’oeil a permis d’améliorer les diagnos-
tics et de clarifier les mécanismes des maladies oculaires qui n’avaient pas été complète-
ment élucidés antérieurement.
Considérations théoriques
Les ondes et les vibrations mécaniques se produisent dans une large gamme de fréquence
appelée le spectre acoustique. Ce spectre s’étend de la gamme audible (10 à 20 000 Hz) que nous
connaissons tous, à la gamme des photons (> 1012 Hz) qui comprend les états vibrationnels de
la matière.
Les ultrasons à haute fréquence offrent une résolution plus élevée de l’ordre de 20 à 40 µm,
mais l’inconvénient est la pénétration moindre des structures. Tous les tissus humains ont des
coefficients d’atténuation des ultrasons qui augmentent avec la fréquence. La pénétration maxi-
male que l’on peut obtenir pour un système de 10 MHz est d’environ 50 mm. Pour un système
de 60 MHz, la pénétration n’est que de 5 mm. La pénétration limitée des ultrasons à haute
fréquence empêche la visualisation du pôle postérieur, mais est suffisante pour obtenir des infor-
mations utiles sur les événements dans le segment antérieur.
Utilisation clinique de la biomicroscopie ultrasonographique
Dans notre laboratoire, nous utilisons des instruments qui ont des fréquences entre 40 et
100 MHz. L’instrument commercial le plus fréquemment utilisé est un transducteur de 50 MHz,
qui offre un bon compromis entre la résolution et la pénétration. Divers instruments sont
actuellement commercialisés avec des fréquences se situant entre 20 et 50 MHz.
Technique
La technique pour utiliser la BMU lorsqu’on examine l’œil est similaire à celle utilisée pour
l’examen du segment antérieur au moyen de l’échographie mode B conventionnelle. Une tech-
nique d’immersion dans du liquide stérile est nécessaire pour fournir une distance adéquate
avec les structures examinées. Cette technique permet d’éviter la déformation de l’image près du
transducteur et d’empêcher le contact entre le transducteur et l’œil. Nous avons conçu une série
de cupules oculaires qui maintiennent les paupières écartées et permettent la préparation plus
MC
Département
d’ophtalmologie et des
sciences de la vision
FACULTY OF MEDICINE
University of Toronto
Disponible sur Internet à :
www.ophthalmologieconferences.ca
rapide du patient. Ces cupules oculaires ressemblent à
celles utilisées dans la biométrie ultrasonique convention-
nelle et sont dotées d’une languette que l’on glisse sous la
paupière et qui maintient la cupule en place. Elles dif-
fèrent des cupules oculaires biométriques, car elles sont
moins profondes et ont la capacité distinctive de permettre
une bonne visualisation de la structure sur laquelle la tête
de balayage est placée. De la
méthylcellulose à 1 % est
utilisée comme milieu de couplage.
Contrairement à l’échographie mode B à 10 MHz, les
transducteurs à haute fréquence ne sont généralement
pas recouverts d’une membrane, étant donné qu’une
membrane entraînerait une atténuation excessive du son
et irait à l’encontre de l’objectif des examens à cette
fréquence. Étant donné que le transducteur se déplace,
tout contact avec l’œil et l’abrasion de la cornée en résul-
tant doivent être soigneusement évités.
On peut examiner toute partie de l’œil dont on peut
approcher directement la surface. Tous les méridiens de la
cornée et des structures du segment antérieur sont facile-
ment examinés. La conjonctive, la sclérotique sous-jacente
et la rétine périphérique peuvent être examinées lorsque
l’œil est positionné aussi loin que possible de la région
examinée. Toutes les structures annexielles dont la surface
peut être exposée peuvent être examinées.
Mesure des structures oculaires
La BMU accroît notre capacité à mesurer précisément
les structures oculaires. La précision des mesures est
améliorée par la biomicroscopie ultrasonographique qui a
une résolution axiale de 5 à 10 fois celle de l’échographie
de 10 MHz conventionnelle. La mesure précise d’une
structure au moyen des ultrasons nécessite de connaître la
vitesse du son dans la structure examinée. Nous avons
utilisé une vitesse du son de 1540 m/s pour effectuer la
majorité des mesures. La vitesse est utilisée dans l’écho-
graphie conventionnelle pour mesurer les distances dans
la plupart des tissus.
La BMU dans les maladies oculaires
Étant donné que la BMU est un outil d’imagerie non
spécifique, elle permet d’examiner une large gamme de
maladies pour lesquelles les limites de pénétration de
cette technique ne sont pas une entrave. Elle est parti-
culièrement utile dans les maladies où il existe des anoma-
lies structurelles, c’est-à-dire les maladies qui entraînent
un réarrangement de l’anatomie normale.
Glaucome
Plusieurs types de glaucome sont causés par des
anomalies structurelles du segment antérieur du globe.
Cela est particulièrement vrai du glaucome à angle fermé et
du glaucome infantile. Étant donné la capacité de la BMU
à produire des images des anomalies structurelles à une
échelle beaucoup plus petite que cela était possible aupara-
vant, elle est un nouvel outil quantitatif pour la recherche
et l’évaluation clinique des maladies glaucomateuses.
Bloc pupillaire
Dans le bloc pupillaire, l’iris adopte un profil convexe
en raison de la pression différentielle entre les chambres
postérieure et antérieure (figure 1). Après une iridotomie,
le profil de l’iris a une configuration beaucoup plus droite.
On notera que le contact entre l’iris et le cristallin est rela-
tivement limité dans le bloc pupillaire, étant donné que
l’iris est décollé du cristallin. Le bloc n’est donc pas lié à la
surface de contact. La surface de contact entre l’iris et le
cristallin devient encore plus limitée lorsque la pupille se
dilate. Dans le bloc pupillaire, il se produit rapidement dans
l’obscurité une fermeture anatomique de l’angle qui est
due à l’épaisseur accrue de l’iris et à son bombement vers
l’avant sur sa base
4
. Un test de provocation en chambre
noire peut être effectué au moyen de la BMU qui détecte
la fermeture de l’angle par apposition dans l’obscurité
5
.
On a très fréquemment recours à la BMU lorsque
l’angle ne s’ouvre pas complètement après une iridotomie.
Ce problème est causé habituellement par l’iridotomie
sans incision, des synéchies antérieures ou le syndrome de
l’iris plateau, qui peuvent être détectés par une BMU.
Synéchies antérieures
La fermeture de l’angle par les synéchies est illustrée
dans la figure 2. L’iris adopte une forme angulaire con-
trairement à sa courbure régulière dans le bloc pupillaire.
Figure 1 : Dans le bloc pupillaire, l’iris montre un
bombement antérieur rétrécissant l’angle (flèche)
et un contact limité entre l’iris et le cristallin
S = sclère, C = cornée, I = iris, PC = procès ciliaire, z = zonule, Cr = cristallin
Figure 2 : Les synéchies antérieures montrent
un iris au profil en angle et sa fixation au réseau
trabéculaire (flèche)
PC
C
Z
Cr
S
I
Dispersion pigmentaire
Le syndrome de dispersion pigmentaire est caractérisé
par une perte pigmentaire de la couche épithéliale pig-
mentaire de l’iris et un dépôt pigmentaire subséquent
dans le réseau trabéculaire entraînant un glaucome
12
. Le
concept de bloc pupillaire inverse implique une inversion
temporaire de la pression différentielle dans les chambres
antérieure et postérieure, produisant un bombement
postérieur de l’iris entraînant un contact entre l’iris et la
zonule avec une perte pigmentaire mécanique. La BMU a
montré que l’accommodation produit un bombement
postérieur de l’iris qui est inversé par l’iridotomie
13
(figure
5 a et b). La question de savoir si une iridotomie est
indiquée dans cette affection n’a pas été élucidée, mais
cette intervention n’est probablement pas indiquée chez
les patients âgés dont la capacité d’accommodation est
réduite.
Tumeurs du segment antérieur
Tumeurs de l’iris et du corps ciliaire
La BMU est un examen d’appoint très utile dans le
traitement des tumeurs du segment antérieur
14,15
, four-
nissant une image claire des lésions du segment antérieur
même les plus petites (figure 6). La capacité à mesurer ces
lésions avec précision ajoute la dimension de la pro-
fondeur aux critères que nous utilisons pour démontrer la
présence d’une tumeur. La capacité à déterminer la struc-
ture sous-jacente de la tumeur permet une meilleure clas-
sification de celle-ci et l’identification d’une atteinte du
corps ciliaire. Lorsque l’on choisit l’observation de
préférence à l’approche chirurgicale, on peut suivre les
lésions avec une plus grande précision. Lorsqu’une inter-
vention chirurgicale est indiquée, les informations
obtenues sont utiles pour planifier l’approche.
Il est difficile d’effectuer un diagnostic histologique
très spécifique au moyen de l’ultrasonographie, même
avec les informations supplémentaires fournies par la
BMU. Le degré de résolution ne permet pas de différencier
les cellules individuelles.
L’état de l’angle derrière la synéchie peut être défini par
biomicroscopie ultrasonographique.
Syndrome de l’iris plateau
On a utilisé la BMU pour déterminer l’étiologie du
syndrome de l’iris plateau
6
. Dans le syndrome de l’iris
plateau, les procès ciliaires sont situés anatomiquement
sur la face antérieure, fermant le sillon ciliaire et four-
nissant un soutien structurel derrière l’iris périphérique
(figure 3). Cela empêche cette partie de l’iris de se disjoin-
dre du réseau trabéculaire après une iridectomie. Dans des
études sur l’iris plateau dans l’obscurité et après l’admini-
stration de pilocarpine, nous avons démontré que la dis-
tance entre les procès ciliaires et le réseau trabéculaire
demeurait constante, l’unique variable contribuant au
rétrécissement de l’angle étant l’épaisseur de l’iris
7
. Nous
avons démontré récemment que la chambre antérieure
axiale est moins profonde dans l’iris plateau que dans le
bloc pupillaire
8
. La fausse perception d’une chambre plus
profonde est due probablement au fait que la chambre
périphérique est plus profonde lorsque la configuration de
l’iris devient plus plate après une iridotomie. Le bloc pupil-
laire et l’iris plateau coexistent fréquemment.
Épanchements supraciliaires et glaucome malin
Les épanchements supraciliaires que l’on ne peut pas
détecter avec l’échographie conventionnelle peuvent être
visualisés par la BMU. Ces épanchements surviennent
dans diverses affections, comprenant les affections inflam-
matoires, les occlusions veineuses et après une chirurgie
pour un décollement de rétine
9,10
. Les épanchements
supraciliaires produisent une rotation des procès ciliaires
et de l’iris autour de l’éperon scléral. Cela peut entraîner la
fermeture de l’angle, en particulier si l’angle est faible au
départ. Nous avons constaté dans la plupart des cas de
glaucome malin la présence d’épanchements supraciliaires
et des procès ciliaires ayant subi une rotation antérieure
11
(figure 4). Il est probable que les épanchements jouent un
rôle dans la manifestation clinique de cette affection.
Figure 3 : Dans l’iris plateau, les procès ciliaires
(PC) sont en avant, soutenant l’iris périphérique
et produisant un rétrécissement de l’angle
périphérique (flèche).
Figure 4 : Dans le glaucome malin, un épanchement
supraciliaire est présent (flèche) avec une rotation
antérieure des procès ciliaires (PC) et de l’iris.
PC
PC
Kystes
La BMU permet de visualiser clairement les
kystes
16,17
. La présentation clinique habituelle d’un
kyste irido-ciliaire est l’élévation de l’iris périphérique
sans atteinte de l’iris. L’apparence typique à la bio-
microscopie ultrasonographique d’un kyste à paroi
mince sans réflexion interne (figure 7) a une valeur
diagnostique et permet essentiellement d’éliminer
tout doute sur la question de savoir si la lésion est un
kyste ou une tumeur solide. De petits kystes sont
également occasionnellement identifiés, soit de façon
isolée lors d’un examen pour une autre indication
clinique soit en association avec des lésions solides de
l’iris ou du corps ciliaire.
La zonule
La BMU permet de visualiser clairement la zonule
antérieure. On nous demande fréquemment de déter-
miner l’état de la zonule dans diverses maladies et
affections traumatiques avant la chirurgie de la
cataracte. L’absence de zonule ou l’irrégularité de
celle-ci peut généralement être déterminée et les
méridiens atteints signalés.
Affection cornéenne et sclérale
La BMU peut être utile chez les patients dont la
cornée est opaque avant une transplantation
18
. On
peut obtenir des renseignements sur le segment
antérieur, tels que la profondeur de la chambre
antérieure, l’état de l’angle, la présence de synéchies
antérieures et le positionnement du cristallin
intraoculaire, avant une intervention. Les anomalies
intracornéennes peuvent également être visualisées.
L’œdème de la cornée peut être évalué et mesuré. Un
balayeur à arc a été mis au point récemment qui
utilise le chemin d’un transducteur pour suivre la
courbure de la cornée et permet la visualisation de
toute la cornée en un seul balayage. Cet instrument
permet l’élaboration de cartes de profondeur en trois
dimensions de l’épaisseur de la cornée, de l’épaisseur
épithéliale et de la profondeur des incisions intra-
cornéennes
19
en chirurgie réfractive. La BMU est
également utile dans la sclérite, permettant la
différenciation entre l’atteinte extra-sclérale et intra-
sclérale et l’évaluation du degré d’amincissement
scléral
20
.
Ophtalmologie
Conférences Scientifiques
Figure 5a : Dispersion pigmentaire – le profil
de l’iris est droit lors de la fixation à distance
Figure 5b : Dispersion pigmentaire –
Bombement postérieur de l’iris lors de la
fixation de près
Figure 6 : Tumeur de l’iris (flèche) dans la
section radiale. L’épaisseur de la tumeur peut
être mesurée et suivie
Figure 7 : Un kyste irido-ciliaire (flèche)
produit une élévation de l’iris périphérique
5a
5b
Complications lors de l’implantation d’une lentille
intraoculaire
La BMU permet d’évaluer facilement la position
des haptiques de la lentille intraoculaire (figure 8).
Cela est très utile pour évaluer un mauvais position-
nement de la lentille ou la source du saignement
intraoculaire et pour déterminer si les haptiques sont
accessibles en cas de nécessité de retrait ou de reposi-
tionnement de la lentille intraoculaire.
Hypotonie et traumatisme
La BMU permet de visualiser les fentes de cyclo-
dialyse, même lorsque la chambre antérieure est peu
profonde et que la fente de cyclodialyse n’est pas visi-
ble à la gonioscopie
22
. Il y a toujours 360
o
de liquide
supraciliaire dans ces cas. La région de la fente est
habituellement visible grâce au déplacement de la
racine iridienne de l’éperon scléral. D’autres causes
d’hypotonie dans laquelle la BMU peut fournir des
informations utiles comprennent les fuites de plaies
occultes et la présence de membranes sur le corps
ciliaire. Dans d’autres problèmes traumatiques, la
BMU permet de visualiser la chambre antérieure sous
des opacités traumatiques
23
et de détecter de petits
corps étrangers qui sont difficiles à visualiser avec des
techniques conventionnelles
24
.
Affections de la conjonctive et des annexes
On peut utiliser la BMU pour examiner toute
lésion que l’on peut approcher sur la surface, four-
nissant d’importantes informations pour le diagnostic
différentiel des tumeurs, nous aidant à évaluer la pro-
fondeur de lésions conjonctivales et limbiques et
nous permettant de visualiser des affections intra-
canaliculaires
25
. On peut également voir un mauvais
positionnement de clous intracanaliculaires et dans le
point lacrymal (figure 9)
26
.
Résumé et orientations futures
La BMU est une nouvelle méthode pour visu-
aliser le segment antérieur de l’œil à une haute réso-
lution. Son avantage est sa capacité à produire des
sections transversales de l’œil vivant à une résolution
microscopique sans altérer l’intégrité du globe. Bien
que les spécimens pathologiques puissent permettre
parfois une évaluation histologique de divers types
de maladie, celle-ci est possible habituellement à un
stade plus tardif de la maladie et est soumise aux dis-
torsions inévitables associées au processus de prépa-
rations. La BMU, bien que n’offrant pas la résolution
de la microscopie optique, produit des images des
yeux vivants sans affecter les relations internes des
structures visualisées. Cette méthode s’est avérée
utile dans la pratique clinique et la recherche en oph-
talmologie. De nouvelles méthodes consistant à
utiliser des ultrasons à haute fréquence sont en cours
de développement, comprenant l’imagerie en trois
dimensions, le Doppler et l’utilisation de substances
de contraste. Ces progrès devraient élargir l’utilisation
de cette technique à de nouveaux domaines.
Le D
r
Pavlin est professeur à l’Université de Toronto
et médecin au Mount Sinai Hospital, au Princess
Margaret Hospital et au St. Michael’s Hospital.
Remerciement: L’auteur désire remercier Michael Sherar,
Brian Starkoski et Kasia Harasiewicz pour leur contri-
bution au développement de ce système d’imagerie fondé
sur la biomicroscopie ultrasonographique.
Références
1. Pavlin CJ, Sherar MD, Foster FS. Subsurface ultrasound microscopic
imaging of the intact eye. Ophthalmology 1990;97:244-50.
2. Pavlin CJ, Harasiewicz K, Sherar MD, Foster FS. Clinical use of ultra-
sound biomicroscopy. Ophthalmology 1991;98:287-95.
3. Pavlin CJ, Foster FS. Ultrasound Biomicroscopy of the eye. New York:
Springer -Verlag,1994.
4. Woo EK, Pavlin CJ, Slomovic A, Taback N, Buys YM. Ultrasound bio-
microscopic quantitative analysis of light-dark changes associated
with pupillary block. Am J Ophthalmol 1999;127:43-7.
5. Pavlin CJ, Harasiewicz K, Foster FS. An ultrasound biomicroscopic
dark-room provocative test. Ophthalmic Surg 1995;26:253-5.
6. Pavlin CJ, Ritch R, Foster FS. Ultrasound biomicroscopy in plateau
iris syndrome. Am J Ophthalmol 1992;113:390-5.
7. P avlin CJ, Foster FS. Plateau iris syndrome: changes in angle opening
associated with dark, light, and pilocarpine administration. Am J
Ophthalmol 1999;128:288-91.
8. Mandell MA, Pavlin CJ, Weisbrod DJ, Simpson ER. Anterior chamber
depth in plateau iris syndrome and pupillary block as measured by
ultrasound biomicroscopy. Am J Ophthalmol 2003;136(5):900-3
9. Pavlin CJ, Rutnin SS, Devenyi R, Wand M, Foster FS. Supraciliary effu-
sions and ciliary body thickening after scleral buckling procedures.
Ophthalmology 1997;104:433-8.
Ophtalmologie
Conférences Scientifiques
Figure 8 : Haptique de la lentille intraoculaire
(flèche) sur la pars plana
Figure 9 : Un clou (flèche) dans le point
lacrymal est visualisé dans le canalicule
2 avril 2004
Jack Crawford Day Hospital for Sick Children
Renseignements : Karen Martin (416) 813-8942 ou
22 avril 2004
PPI – D
r
Donald Fletcher, Birmingham, Alabama
Advances in Low Vision Rehabilitation
29 avril 2004
PPI – D
r
Douglas, Coster, Australie
Cornea
6 mai 2004
PPI – D
r
Kathleen Digre, Salt Lake City, Utah
Neuro-ophthalmic changes in pregnancy
13 mai 2004
PPI – D
r
Shaun Singer, Toronto, Ontario
Quality Assurance Rounds
20 mai 2004
PPI – D
r
David Apple, Charleston, Caroline du Nord
U of T & TOS combined Rounds
Note : Programme à l’intention des professeurs invités (PPI)
2003/2004
Adresse du centre : Toronto Western Hospital,
Aile Ouest, Salle 401, 399 Bathurst Street, Toronto
Réunions scientifiques à venir
4 au 5 avril 2004
Royal National Institute of the Blind (RNIB)
8
th
International Conference on issues concerning
low vision and sight – Vision 2005 London
Londres, Angleterre
Renseignements : www.rnib.org.uk/vision2005/register
Tél. : 44(0)20 7940 5362
10. Yuki T, Kimura Y, Nanbu S, Kishi S, Shimizu K. Ciliary body and choroidal
detachment after laser photocoagulation for diabetic retinopathy. A high-
frequency ultrasound study. Ophthalmology 1997;104:1259-64.
11. Trope GE, Pavlin CJ, Bau A, Baumal CR, Foster FS. Malignant glaucoma.
Clinical and ultrasound biomicroscopic features. Ophthalmology
1994;101:1030-5.
12. Potash SD, Tello C, Liebmann J, Ritch R. Ultrasound biomicroscopy in pig-
ment dispersion syndrome. Ophthalmology 1994;101:332-9.
13. Pavlin CJ, Macken P, Trope GE, Harasiewicz K, Foster FS. Accommodation
and iridotomy in the pigment dispersion syndrome. Ophthalmic Surg Lasers
1996;27:113-20.
14. Pavlin CJ, McWhae JA, McGowan HD, Foster FS. Ultrasound biomicroscopy
of anterior segment tumors. Ophthalmology 1992;99:1220-8.
15. Maberly DA, Pavlin CJ, McGowan HD, Foster FS, Simpson ER. Ultrasound
biomicroscopic imaging of the anterior aspect of peripheral choroidal
melanomas. Am J Ophthalmol 1997;123:506-14.
16. Augsburger JJ, Affel LL, Benarosh DA. Ultrasound biomicroscopy of cystic
lesions of the iris and ciliary body. Trans Am Ophthalmol Soc 1996;94:259-
71.
17. Fine L, Pavlin CJ. Primary iridociliary cysts: a report on 210 cases. Can J
Ophthalmol 1999.
18. Milner MS, Liebmann JM, Tello C, Speaker MG, Ritch R. High-resolution
ultrasound biomicroscopy of the anterior segment in patients with dense
corneal scars. Ophthalmic Surg 1994;25:284-7.
19. Reinstein DZ, Silverman RH, Raevsky T, et al. Arc-scanning very high-
frequency digital ultrasound for 3D pachymetric mapping of the corneal
epithelium and stroma in laser in situ keratomileusis. J Refract Surg 2000;
16:414-30.
20.Pavlin CJ, Easterbrook M, Hurwitz JJ, Harasiewicz K, Eng P, Foster FS. Ultra-
sound biomicroscopy in the assessment of anterior scleral disease. Am J
Ophthalmol 1993;116:628-35.
21. Pavlin CJ, Rootman D, Arshinoff S, Harasiewicz K, Foster FS. Determination
of haptic position of transsclerally fixated posterior chamber intraocular
lenses by ultrasound biomicroscopy. J Cataract Refract Surg 1993;19:573-7.
22. Gentile RC, Pavlin CJ, Liebmann JM, et al. Diagnosis of traumatic cyclodial-
ysis by ultrasound biomicroscopy. Ophthalmic Surg Lasers 1996;27:97-105.
23. Berinstein DM, Gentile RC, Sidoti PA, et al. Ultrasound biomicroscopy in
anterior ocular trauma. Ophthalmic Surg Lasers 1997;28:201-7.
24. Deramo VA, Shah GK, Baumal CR, et al. Ultrasound biomicroscopy as a tool
for detecting and localizing occult foreign bodies after ocular trauma.
Ophthalmology 1999;106:301-5.
25. Hurwitz JJ, Pavlin CJ, Hassan A. Proximal canalicular imaging utilizing
ultrasound biomicroscopy A: normal canaliculi.Orbit 1998;17:27-30.
26. Hurwitz JS, Pavlin CJ, Rhemtulla EK. The location of retained punctal plugs
using ultrasound biomicroscopy. Can J Ophthalmol Sous Presse.
Prochains événements au sein du service
12 février 2004
PPI – D
r
Rosa Braga-Mele and D
r
Joseph Mikhael, Toronto, ON
“Say what?” Effective communication to patients and
house staff
26 février 2004
PPI – D
r
Alan Crandal, Salt Lake City, Utah
20 Years of Cataract/Glaucoma
28 février 2004
Toronto Cataract Course, Sutton Place Hotel
955 Bay Street
Renseignements : Bureau de la formation médicale continue
(416) 978-2719
4 mars 2004
D
r
Frank Buffam, Vancouver, Colombie-Britannique
Management of Ophthalmic Complication of VII Palsy
SNELL
© 2004 Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto, seul responsable du contenu de cette publication. Édition : SNELL Communication
Médicale Inc. avec la collaboration du Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto.
MD
Ophtalmologie – Conférences scientifiques est une marque
de commerce de SNELL Communication Médicale Inc.Tous droits réservés. L’administration d’un traitement thérapeutique décrit ou mentionné dans Ophtalmologie – Conférences scientifiques doit
toujours être conforme aux renseignements d’ordonnance approuvés au Canada. SNELL Communication Médicale se consacre à l’avancement de l’éducation médicale continue de niveau supérieur.
L’élaboration de cette publication a bénéficié d’une subvention à l’éducation de
Novartis Ophthalmics
130-004F
La version française a été revisée par le professeur Pierre Lachapelle,
Montréal.
Les avis de changement d’adresse et les demandes d’abonne-
ment pour Ophtalmologie – Conférences Scientifiques doivent
être envoyés par la poste à l’adresse C.P. 310, Succursale H,
Montréal (Québec) H3G 2K8 ou par fax au (514) 932-5114 ou
par courrier électronique à l’adresse
Veuillez vous référer au bulletin Ophtalmologie – Conférences
Scientifiques dans votre correspondence. Les envois non
distribuables doivent être envoyés à l’adresse ci-dessus.
Ophtalmologie
Conférences Scientifiques
FÉVRIER 2004
Volume 2, numéro 2
COMPTE RENDU DES CONFÉRENCES
SCIENTIFIQUES DU DÉPARTEMENT
D’OPHTALMOLOGIE ET
DES SCIENCES DE LA VISION,
FACULTÉ DE MÉDECINE,
UNIVERSITÉ DE TORONTO
Département d’ophtalmologie
et des sciences de la vision
Faculté de médecine
Université de Toronto
60 Murray St.
Bureau 1-003
Toronto (Ontario) M5G 1X5
Le contenu rédactionnel d’Ophtalmologie –
Conférences scientifiques est déterminé
exclusivement par le Département
d’ophtalmologie et des sciences de la vision,
Faculté de médicine, Université de Toronto.
Département d’ophtalmologie
et des sciences de la vision
Jeffrey Jay Hurwitz, M.D., Rédacteur
Professeur et président
Martin Steinbach, Ph.D.
Directeur de la recherche
The Hospital for Sick Children
Elise Heon, M.D.
Ophtalmologiste en chef
Mount Sinai Hospital
Jeffrey J. Hurwitz, M.D.
Ophtalmologiste en chef
Princess Margaret Hospital
(Clinique des tumeurs oculaires)
E. Rand Simpson, M.D.
Directeur, Service d’oncologie oculaire
St. Michael’s Hospital
Alan Berger, M.D.
Ophtalmologiste en chef
Sunnybrook and Women’s College
Health Sciences Centre
William S. Dixon, M.D.
Ophtalmologiste en chef
The Toronto Hospital
(Toronto Western Division and
Toronto General Division)
Robert G. Devenyi, M.D.
Ophtalmologiste en chef
La dégénérescence maculaire liée à l’âge
PAR
MICHAEL H. BRENT
, M.D.
La dégénérescence maculaire liée à l’âge (DMLA) est la première cause de perte sévère et
irréversible de la vision en Amérique du Nord et dans tous les pays industrialisés
1
. Les personnes
atteintes de DMLA, âgées de 55 ans et plus, présentent souvent divers symptômes visuels à la
consultation. Une approche diagnostique ciblée peut aider à déterminer et à établir le stade du
processus morbide. Les résultats des études cliniques récentes et la technologie émergente ont
modifié le traitement de la DMLA.
Classification
La DMLA est la première cause de cécité dans la population âgée de 55 ans et plus. Le risque de
développer une forme de DMLA augmente avec l’âge, et à l’âge de 75 ans, le risque est de près de
40 %. La DMLA est classée en deux entités cliniques : atrophique (sèche) et exsudative (humide).
La DMLA atrophique
La DMLA atrophique touche environ 85 % de tous les patients souffrant de DMLA et est respon-
sable de 10 à 20 % des cas de cécité causée par cette maladie (figure 1). La perte de la vision est
généralement progressive et le degré de perte de vision est déterminé par le nombre, la taille, la mor-
phologie et la localisation des drusens dans la macula ainsi que par le degré et la localisation de l’at-
rophie de l’épithélium pigmentaire rétinien (ÉPR). La taille des drusens peut être petite (< 63 µm),
moyenne (63 µm-124 µm) ou grande (≥125 µm)
2
. Les drusens durs et de petite taille sont associés à
un faible risque d’évolution vers la DMLA de stade avancé, en particulier lorsque qu’ils sont en petit
nombre (p. ex. < 5). Les drusens de taille moyenne et de grande taille et les drusens confluents sont
des signes de DMLA de stade plus avancé qui pourrait évoluer vers une DMLA exsudative. La
présence d’un amas de pigments est souvent associée aux drusens. L’atrophie géographique non cen-
trale de l’ÉPR est un indicateur d’une DMLA atrophique de stade plus avancé. Les maculas compor-
tant au moins un drusen de grande taille et/ou de plusieurs drusens de taille moyenne sont plus
probablement associées au développement d’une atrophie de l’ÉPR. Chez les patients présentant une
DMLA atrophique de stade avancé, jusqu’à 43 % évoluent vers une DMLA exsudative sur une
période de 5 ans.
La DMLA exsudative
La DMLA exsudative touche environ 15 % de tous les patients souffrant de DMLA, et est pourtant
responsable de 80 à 90 % des cas de cécité causée par cette maladie (figure 2). La perte de la vision est
généralement rapide, en quelques jours ou mois, et est déterminée par la quantité de sang, de lipide et
de liquide dans l’espace sous-rétinien et intrarétinien et du tissu cicatriciel sous la rétine maculaire en
résultant. La physiopathologie acceptée conventionnellement comprend la prolifération de néovais-
seaux sanguins anormaux dans la choroïde qui entraîne le développement d’une membrane néovas-
culaire choroïdienne (MNVC). Ces néovaisseaux traversent la membrane de Bruch dans l’espace sous
l’ÉPR et sous-rétinien. Les exsudats, les hémorragies et les cicatrices fibrovasculaires endommagent et
détruisent les photorécepteurs paramaculaires, entraînant une baisse d’acuité visuelle sévère.
Récemment, Yannuzzi et coll. ont décrit un autre processus physiopathologique appelé la pro-
lifération angiomateuse rétinienne (PAR) qui peut également entraîner une perte sévère de la vision
centrale et est incluse dans la catégorie de la DMLA exsudative
3
. Dans la PAR, la prolifération capil-
laire débute dans la région paramaculaire au niveau du plexus capillaire profond de la rétine. La pro-
lifération néovasculaire se produit antérieurement et postérieurement. La prolifération postérieure
envahit finalement l’espace sous-rétinien et une membrane néovasculaire sous-rétinienne se forme et
produit alors un soulèvement de l’ÉPR séreux. L’aggravation de la prolifération entraîne l’envahisse-
ment de la choroïde par les vaisseaux, formant la MNVC. La prolifération antérieure des vaisseaux
forme une anastomose avec la circulation rétinienne. Il se produit donc une anastomose chorioréti-
nienne. Les tableaux clinique et angiographique sont similaires à ceux de la DMLA et souvent indis-
cernables de celle-ci où la néovascularisation débute dans la choroïde plutôt que dans la rétine. Les
deux entités peuvent répondre différemment aux modalités thérapeutiques existantes, à différents
stades de leur évolution.
MC
Département
d’ophtalmologie et des
sciences de la vision
FACULTY OF MEDICINE
University of Toronto
Disponible sur Internet à :
www.ophtalmologieconferences.ca
Présentation clinique
Chez les patients âgés de 55 ans et plus présentant une
vision trouble ou déformée, on devrait soupçonner une
DMLA. D’autres symptômes peuvent comprendre la difficulté
à lire ou des difficultés visuelles lorsque l’éclairage est insuff-
isant. On peut noter de longues périodes de stabilité de la
vision entrecoupées de périodes plus courtes de détériora-
tion. Lorsque l’on évalue des patients chez qui l’on soupçonne
une DMLA, l’anamnèse doit comprendre l’âge d’apparition, la
durée des symptômes, la localisation des distorsions/des sco-
tomes paracentraux et le degré de perte de la sensibilité au
contraste. Les facteurs de risque de DMLA doivent être exa-
minés, comprenant l’âge, la race, le sexe, la couleur claire
de l’iris, les antécédents familiaux, la présence de coro-
naropathie, d’hypertension, le tabagisme, une mauvaise ali-
mentation et l’exposition prolongée aux rayons ultraviolets.
Les personnes dont la peau est claire présentent un risque
plus élevé de développer une DMLA. Les femmes présentent
un risque deux fois plus élevé que les hommes et les fumeurs,
un risque 6 fois plus élevé. On doit interroger les patients sur
les médicaments qu’ils prennent qui pourraient avoir un effet
néfaste sur la fonction maculaire (p. ex. les dérivés de la
chloroquine, les phénothiazines et les médicaments antitu-
berculeux).
L’examen oculaire
L’examen oculaire doit établir la présence d’une baisse de
la vision et exclure une erreur de réfraction comme la cause
sous-jacente, soit par réfraction soit par la vérification de
l’acuité visuelle à l’aide d’un trou sténopéique.
• On doit utiliser la grille d’Amsler pour toutes les évalua-
tions de la DMLA, étant donné que c’est un test facile à
effectuer et s’il est positif, il peut aider à orienter l’investiga-
tion vers une zone spécifique durant l’examen biomicro-
scopique.
• En présence d’une opacité lenticulaire importante, le
test de la fonction maculaire au moyen de l’interférométrie
laser ou éventuellement d’un grillage d’acuité visuelle peut
permettre de déterminer dans quelle mesure la baisse de
l’acuité visuelle est due à la cataracte ou à une pathologie
maculaire.
• Une évaluation du champ visuel est recommandée pour
exclure la perte concomitante du champ visuel périphérique
ou des causes neurologiques de la perte de la vision centrale.
• Si disponible, le test de sensibilité binoculaire au con-
traste de Pelli Robson est rapide et fiable pour évaluer et
suivre la fonction visuelle dans la DMLA.
• L’examen de la macula doit être effectué au moyen de la
biomicroscopie avec une lentille biconvexe indirecte (60-90 D)
ou une lentille de Hruby. Malgré l’inversion de l’image, on
obtient une bonne stéréopsie. Durant la biomicroscopie macu-
laire, la taille, la localisation et la morphologie des drusens
doivent être notées. On doit noter les amas de pigments et les
zones d’atrophie de l’ÉPR, étant donné qu’ils peuvent être des
indicateurs d’une DMLA atrophique de stade avancé. La
présence de sang, de lipide ou de liquide sous la rétine est un
signe devant faire soupçonner la présence d’une MNVC.
• L’ophtalmoscopie directe ne fournit pas une stéréopsie
et ne permet pas d’évaluer correctement la macula dans la
DMLA.
• On peut obtenir une vue optique optimale de la macula
avec une lentille de contact maculaire. Cependant, cette tech-
nique nécessite une anesthésie topique et l’utilisation d’un
liquide visqueux pour éliminer l’interface air-cornée. Le
liquide visqueux peut altérer la qualité des clichés photo-
graphiques et angiographiques s’ils sont réalisés peu de
temps après l’examen.
Une perte sévère de vision, la déformation de la grille
d’Amsler et la présence cliniquement manifeste de sang, de
lipide ou de liquide nécessitent d’orienter le patient en
urgence vers un spécialiste de la rétine ayant la capacité de
réaliser une angiographie à la fluorescéine. L’algorithme en
vue de déterminer la meilleure ligne de conduite pour
réduire la perte de vision chez un patient affichant une
MNVC est fondé sur l’interprétation de l’angiographie à la
fluorescéine. Il permet de déterminer si le laser thermique, la
photothérapie dynamique avec Visudyne
®
ou simplement un
suivi pendant une période d’observation seront bénéfiques
pour le patient.
Histoire naturelle
Dans l’histoire naturelle de la DMLA, plusieurs facteurs
sont associés à la progression de la DMLA atrophique vers la
forme exsudative (tableau 1). En présence de drusens de
grande taille et/ou de plusieurs drusens de taille moyenne ou
d’une atrophie géographique non centrale, la formation d’une
MNVC est probable. Si un œil a déjà développé une MNVC
sous-fovéale, il existe des facteurs pronostiques importants de
perte de vision dans l’autre œil, secondaire au développement
d’une MNVC. Ces facteurs sont fondés sur le type de DMLA
tardive documentée dans le premier œil et incluent
>5drusens, un drusen mou de grande taille, un amas de
pigments et une hypertension systémique. Lorsque le nombre
de facteurs de risque augmente, le risque de développer une
DMLA exsudative dans l’autre œil est de près de 90 %
(figure 3)
4
.
I
Figure 1 : DMLA atrophique Figure 2 : DMLA exsudative
DMLA = dégénérescence maculaire liée à l’âge
tous les quadrillages, le résultat du test est considéré comme
normal et l’autre œil doit être testé. Si le patient remarque une
distorsion, un flou ou des scotomes paracentraux, il faut les
inscrire sur la grille et inclure celle-ci dans son dossier médi-
cal. Ces informations peuvent être utiles pour une compa-
raison future et pour documenter l’évolution ou la régression
de la maladie.
Angiographie à la fluorescéine
L’angiographie à la fluorescéine est actuellement l’exa-
men de référence pour évaluer la circulation rétinienne et
choroïdienne dans la DMLA. Après avoir réalisé des clichés
photographiques en couleur du fond de l’œil, on injecte par
voie intraveineuse un colorant, la fluorescéine sodique. Ce
colorant est activé par la lumière du flash de l’appareil photo
qui passe à travers un filtre activateur bleu. La longueur
d’onde de 490 nm de la lumière bleue est absorbée par les
molécules de fluorescéine dans la circulation choroïdienne,
puis dans la circulation rétinienne. Le colorant est activé pour
émettre une lumière jaune-verte (530 nm) qui repasse dans
l’appareil photo par un filtre écran jaune-vert, bloquant la
lumière bleue réfléchie, ce qui permet à la fluorescence d’être
photographiée. Les clichés photographiques sont pris lorsque
le colorant passe à travers la circulation choroïdienne et
rétinienne. Les drusens peuvent être rendus fluorescents,
l’atrophie de l’épithélium pigmentaire rétinien apparaît
comme des défauts, et les néovaisseaux choroïdiens laissent
fuir le colorant et sont hyperfluorescents. La néovascularisa-
tion choroïdienne est interprétée et classifiée selon le type de
fuite
8
. La néovascularisation choroïdienne classique apparaît
comme une zone d’hyperfluorescence vive et bien démar-
quée durant la phase initiale de l’angiogramme, avec une
fuite progressive du colorant dans l’espace sous-rétinien sus-
jacent durant la dernière phase de l’angiogramme (figure 4).
Les lésions occultes peuvent présenter deux schémas
angiographiques :
• Le décollement de l’épithélium pigmentaire rétinien
démontre une hyperfluorescence tachetée qui n’est pas aussi
vive ou discrète que dans la néovascularisation choroïdienne
classique, 1 à 2 minutes après l’injection de la fluorescéine,
avec une coloration ou une fuite persistante de la fluo-
rescéine 10 minutes après l’injection.
• Le deuxième schéma est celui d’une fuite tardive de
source indéterminée. Cela ne se produit que durant la
dernière phase de l’angiogramme, sans signes de néovascula-
risation choroïdienne classique ou de décollement de l’épi-
thélium pigmentaire rétinien fibrovasculaire durant les
phases initiale et intermédiaire de l’angiogramme pour expli-
quer la fuite (figure 5).
Jusqu’à récemment, la plupart des clichés photo-
graphiques et des clichés angiographiques à la fluorescéine
du fond de l’œil étaient enregistrés sur film. Avec les progrès
Étude des maladies oculaires liées à l’âge
L’étude AREDS (Age Related Eye Disease) a examiné le rôle
de la supplémentation en micronutriments dans la modifica-
tion de l’histoire naturelle de la DMLA atrophique
5
. Elle a
démontré l’efficacité de fortes doses d’anti-oxydants et de
minéraux pour réduire le risque de progression de la DMLA
de stade intermédiaire vers une DMLA unilatérale de stade
avancé de 25 % et de perte modérée de vision (≥ 3 lignes) de
19 % à 5 ans. Les patients ne souffrant pas de DMLA ou ne
présentant qu’une DMLA de stade précoce n’ont obtenu
aucun avantage. La préparation étudiée consistait en 500 mg
de vitamine C, 400 UI de vitamine E, 25 000 UI de bêta-
carotène, 80 mg d’oxyde de zinc et 2 mg d’oxyde cuivrique.
Les auteurs de l’étude AREDS Update II ont examiné les
facteurs de risque de DMLA et le rôle des lipides alimentaires
dans la pathogenèse de la DMLA
6
. Ils ont rapporté qu’un
apport plus élevé de lipides alimentaires, tels que les acides
gras polyinsaturés à longue chaîne oméga-3/le poisson et la
lutéine/la zéaxanthine, était associé à un risque réduit
de développer une DMLA néovasculaire. Seddon et coll. ont
constaté qu’un apport total plus élevé de graisses augmentait
le risque de progression vers des formes avancées de DMLA
7
.
Un apport plus élevé de graisses végétales et, dans une moin-
dre mesure, de graisses animales, augmentait le taux de pro-
gression. On a constaté en particulier que les produits
transformés cuits au four entraînaient un taux plus élevé de
progression, alors que les noix avaient un effet protecteur.
Par conséquent, la modification de l’apport de graisses pour-
rait potentiellement modifier l’évolution de la maladie chez
les patients présentant les formes précoce et intermédiaire
de DMLA.
Évaluation diagnostique
Les tests suivants sont utiles pour déterminer la présence
d’une DMLA et évaluer son stade.
Grille d’Amsler
La grille d’Amsler est un excellent test de la fonction mac-
ulaire monoculaire pour déterminer la présence d’une
pathologie maculaire. Chaque carré de 5 mm sur la grille
forme un angle visuel de 1
o
lorsque l’on tient la grille à une
distance de 30 cm. Par conséquent, la grille entière teste 10
o
de chaque côté du point de fixation, sur les lignes horizon-
tales et verticales. Le test de la grille d’Amsler doit être effec-
tué avant la dilatation de la pupille et la tonométrie par
aplanation. Avec leurs lunettes de lecture, les patients se
cachent un œil et fixent le point central sur la grille. Si le
patient voit toutes les lignes sans distorsions et s’ils voient
PC
Tableau 1 : Évolution de la DMLA atrophique vers
la DMLA exsudative
La composition et le nombre de drusens dans la DMLA
sèche sont des facteurs associés à un risque plus élevé
d’évolution vers la DMLA humide :
• Yeux porteurs de drusens bilatéraux
• Drusens mous, avec une bordure mal définie non discrète
• Nombreux drusens mous (> 20) associés à un
changement pigmentaire de l’ÉPR
• Au moins cinq drusens de grande taille (> 63 µm)
• Hyperpigmentation locale de l’ÉPR
• Anomalies pigmentaires comprenant des amas
de pigments
• Patients présentant une atrophie géographique
(stade tardif de la DMLA)
Figure 3 : Évolution vers la DMLA exsudative dans
le deuxième œil
4
100 %
90 %
80 %
70 %
60 %
50 %
40 %
30 %
20 %
10 %
0 %
0 1 2 3 4
7 %
25 %
44 %
53 %
87 %
Risque à cinq ans de développer une DMLA humide dans l’œil controlatéral
Nombre de facteurs de ris
q
ue
de la technologie, la capture numộrique et le stockage
dimages
sont devenus couramment utilisộs. Des rộsul-
tats instantanộs sont obtenus et la taille des lộsions peut
ờtre mesurộe de faỗon plus prộcise. Les composantes des
lộsions causộes par la nộovascularisation choroùdienne
peuvent ờtre ộvaluộes quantativement, afin que lon
dộtermine si un traitement est appropriộ
9
. Les images
numộriques sont facilement stockộes un coỷt peu
ộlevộ et le procộdộ numộrique permet dộtablir des bases
de donnộes pour aider la recherche.
Angiographie au vert dindocyanine
Langiographie au vert dindocyanime (AVI) est un
autre outil diagnostique important dans lộvaluation de
la MNVC dans la DMLA. Le vert dindocyanime est un
colorant base de tricarbocyanine qui absorbe la
lumiốre 790-805 nm et qui a un pic dộmission
835 nm, qui se situe dans le spectre infrarouge. Il est
injectộ par voie intraveineuse et la vidộoangiographie
infrarouge numộrique est utilisộe pour photographier
les vaisseaux de la rộtine et de la choroùde. Le vert din-
docyanine est liộ 95 % au plasma et reste donc en
grande partie dans les vaisseaux, facilitant la visualisa-
tion des vaisseaux choroùdiens. Le vert dindocyanine
peut ờtre visualisộ travers une mince couche de sang,
le liquide sộreux et les pigments. Langiographie au vert
dindocyanine, utilisộe conjointement langiographie
la uorescộine, permet de mieux dộterminer lộtendue
dune lộsion chez les patients prộsentant une MNVC
occulte ou minimalement classique. Cela se traduit par
un meilleur traitement et un taux rộduit de rộpộtition du
traitement. Le vert dindocyanine est sỷr pour un usage
gộnộral et il est moins toxique que la fluorộscộine
sodique. Il contient environ 5 % diode par poids et est
ộliminộ par le foie. Le vert dindocyanine est donc contre-
indiquộ pour les patients allergiques liode ou aux crus-
tacộs ou souffrant dune maladie hộpatique importante.
Tomographie cohộrence optique
La tomographie cohộrence optique (TCO) est une
technologie similaire lộchographie, mais qui utilise les
ondes lumineuses plutụt que les ondes acoustiques pour
produire des images transversales haute rộsolution du
pụle postộrieur. Cette technologie non invasive permet
la visualisation lộchelle du micron des microstructures
tissulaires in situ, en temps rộel. Le Stratus OCT3 de
Zeiss Humphrey est un modốle de 3
e
gộnộration ayant
une rộsolution axiale de 7-8 àm. De fausses couleurs
sont ajoutộes aux tissus avec diffộrentes propriộtộs
optiques de diffusion, amộliorant la qualitộ de limage.
La TCO trốs haute rộsolution a ộtộ dộveloppộe, mais
elle nest pas encore commercialisộe. Elle fournit une
rộsolution axiale aussi haute que 1-2 àm. La TCO est un
outil utile pour diagnostiquer une pathologie maculaire
et pour surveiller le succốs du traitement. Elle permet de
mesurer lộpaisseur de la rộtine et de visualiser le liquide
intrarộtinien et le liquide sous-rộtinien (sang, liquide
sộreux, MNVC). Cest ộgalement une excellente tech-
nologie pour dộmontrer la traction de la macula (mem-
branes ộpirộtiniennes), la traction vitrộo-maculaire et la
formation dun trou maculaire. Lorsque le traitement est
amorcộ, la TCO est extrờmement utile pour surveiller et
quantier la rộponse post-opộratoire et faciliter la dộci-
sion de retraiter le patient. Elle devient rapidement un
outil diagnostique important dans lộvaluation et le
traitement de la DMLA.
Traitement clinique
La DMLA atrophique
Aprốs un examen clinique, chez les patients que lon
considốre ờtre atteints de DMLA atrophique et dont le
test de la grille dAmsler est normal, il nest gộnộralement
pas nộcessaire deffectuer une angiographie. Il faut don-
ner au patient une grille dAmsler pour quil effectue
quotidiennement le test la maison des fins de
dộpistage. Il faut lui rappeler de porter ses lunettes de
lecture et deffectuer le test dans les mờmes conditions
dộclairage. Il devra appeler le cabinet du mộdecin sil
remarque un changement important dans la grille
durant 3 jours ou plus. Une rộộvaluation urgente devra
ờtre effectuộe et si lon soupỗonne une DMLA exsuda-
tive, il est recommandộ dadresser le patient un spộcia-
liste de la rộtine. Il faut conseiller aux patients dadopter
un rộgime alimentaire riche en lộgumes et daugmenter
leur apport de poisson 1 2 portions par semaine. Il
peut ờtre utile ộgalement de rộduire lapport de graisses
alimentaires.
Chez les patients ne fumant pas et prộsentant des
drusens extensifs de taille moyenne (63-124 àm), au
moins un drusen de grande taille ( 125 àm), une atro-
phie gộographique non centrale dans lun ou les deux
yeux, ou souffrant dune DMLA de stade avancộ ou
dune perte de lacuitộ visuelle due une DMLA dans un
il, une supplộmentation en micronutriments peut ờtre
bộnộque, tel quindiquộ dans lộtude AREDS. Actuelle-
ment, il existe deux prộparations commercialisộes au
Ophtalmologie
Confộrences Scientifiques
Figure 4 : MNVC sous-fovộale essentiellement
classique dans la DMLA
Figure 5 : MNVC occulte dans la DMLA
MNVC = membrane nộovasculaire choroùdienne
Canada qui correspondent au dosage prộconisộ dans
lộtude AREDS. Avec Vitalux
đ
AREDS par Novartis
Ophthalmics, 2 comprimộs par jour correspondent au
dosage prộconisộ dans lộtude. Cette prộparation con-
tient de la lutộine et de la zộaxathộine. Avec la prộpara-
tion Ocuvite Preser Vision
đ
par Bausch & Lomb, qui ne
contient pas de lutộine et de zộaxanthộine, 4 comprimộs
par jour correspondent au dosage de lộtude. Les
fumeurs prộsentent un risque plus ộlevộ de dộvelopper
un cancer du poumon sils prennent de la bờta-carotốne.
On doit les en informer et ils devraient sarrờter de
fumer, si possible. Il ny a pas de consensus sur la durộe
pendant laquelle un fumeur doit sarrờter de fumer
avant de prendre sans danger de la bờta-carotốne
10
.
Certains fumeurs atteints de DMLA dộsireront peut-ờtre
prendre la prộparation AREDS sans bờta-carotốne. Cette
prộparation est commercialisộe sous le nom de Vitalux-
S
đ
, par Novartis Ophthalmics, 2 comprimộs par jour. Les
patients souffrant de DMLA doivent se protộger contre
les rayons ultraviolets en portant des lunettes de soleil
ayant une forme enveloppante lorsquils sortent dehors
la lumiốre du jour.
La DMLA exsudative
Les patients chez qui lon soupỗonne une DMLA
exsudative doivent faire lobjet dune investigation plus
approfondie. Langiographie la fluorescộine est
actuellement le test diagnostique de choix pour ộvaluer
la DMLA exsudative, ộtant donnộ quelle fournit des
informations sur la localisation, la composition et lộten-
due des lộsions. En prộsence de MNVC qui sont bien
dộlimitộes et extra-fovộales ou juxta-fovộales, le laser
thermique offre un avantage par opposition ladminis-
tration daucun traitement
11
. Pour les lộsions qui sont
mal dộlimitộes, il nest gộnộralement pas recommandộ
dutiliser le laser thermique. Pour les MNVC sous-
fovộales, il peut ờtre avantageux dutiliser la photo-
thộrapie dynamique (PTD) avec Visudyne
đ
, selon lacuitộ
visuelle initiale et la composition et la taille des lộsions.
Lộtude TAP (Treatment of Age-Related Macular
Degeneration with Photodynamic Therapy) a dộmontrộ
que la PTD avec Visudyne avait un effet bộnộfique
statistiquement signicatif par rapport au placebo pour
les lộsions sous-fovộales qui ộtaient essentiellement clas-
siques, avec une acuitộ visuelle initiale de 20/40
20/200
12
.Lộtude VIP (Verteprofin in Photodynamic
Therapy) a dộmontrộ que la PTD avec Visudyne avait un
effet thộrapeutique cliniquement signicatif sur la fonc-
tion visuelle chez les patients qui souffraient de DMLA
occulte, ne comprenant pas de lộsions sous-fovộales
classiques et dont la maladie avait rộcemment ộvoluộ
13
.
Chez les patients qui avaient une acuitộ visuelle initiale
20/50 et dont la taille des lộsions ộtait 4 tờtes du nerf
optique, on a obtenu des rộsultats optimaux. La PTD
avec Visudyne na offert aucun avantage statistiquement
significatif pour les yeux affichant une MNVC sous-
fovộale minimalement classique. Pour les lộsions princi-
palement classiques, ou occultes sans lộsions classiques
qui sont juxtafovộales, la thộrapie photodynamique avec
Visudyne doit ờtre envisagộe lorsque la lộsion est si prốs
du centre fovộal que la photocoagulation au laser ther-
mique conventionnelle sộtendrait probablement sous le
centre de la zone fovộale avasculaire.
Rộcemment, une analyse rộgression linộaire multi-
ple des donnộes des ộtudes TAP et VIP a indiquộ que
comparộ la composition des lộsions ou lacuitộ
visuelle initiale, la taille des lộsions ộtait le facteur ayant
limpact le plus signicatif sur les rộsultats thộrapeu-
tiques
15
. On a constatộ que chez les patients prộsentant
des lộsions de plus petite taille ( 4 tờtes du nerf
optique), la perte de lacuitộ visuelle ộtait moindre et le
traitement avait un bienfait similaire, que la lộsion soit
essentiellement classique, minimalement classique ou
occulte et ne contenant pas de lộsions classiques.
15
Actuellement, les rộgimes de santộ provinciaux
prennent en charge le coỷt du traitement des patients
affichant une MNVC essentiellement classique se-
condaire une DMLA, lexception de lẻle-du-Prince-
ẫdouard et de Terre-Neuve. Les rộgimes de santộ de
Colombie-Britannique et du Quộbec prennent en charge
les coỷts du traitement de tous les types de MNVC, la
discrộtion de lophtalmologiste traitant. Dans toutes les
autres provinces, les patients afchant des lộsions mini-
malement classiques ou occultes sans MNVC sous-
fovộale dues une DMLA, qui dộsirent recevoir un
traitement, doivent payer pour lusage en dộrogation de
directives de la PTD par Visadyne. Le traitement est coỷ-
teux et nộcessite en moyenne 4 6 sộances pour une
occlusion de la MNVC. Les patients doivent ờtre infor-
mộs que lobjectif du traitement est la stabilisation de la
vision, bien que certains patients remarquent une lộgốre
amộlioration de la vision la n du traitement. Lorsque
la PTD est rộpộtộe, les lộsions qui sont initialement mini-
malement classiques ou qui sont occultes et ne com-
prennent pas de lộsions classiques peuvent devenir
essentiellement classiques. Malheureusement, la dộci-
sion des rộgimes de santộ provinciaux de prendre en
charge le coỷt de la PTD est fondộe sur le tableau
clinique initial, tel quindiquộ par langiographie la u-
orescộine.
Traitements expộrimentaux
Il existe plusieurs nouvelles options thộrapeutiques
pour la DMLA qui sont divers stades dộtudes cli-
niques. La rhộophorốse pour la DMLA atrophique fait
actuellement lobjet dộtudes cliniques de phase III. Ce
procộdộ ltre les macromolộcules (p. ex. macroglobu-
line, brinogốne, complexes cholestộrol-LDL et IgA) qui,
pense-t-on, ont des effets dộlộtốres sur la circulation
microvasculaire, entraợnant le processus dộgộnộratif
atrophique. Lộtude TTT4CNV (Transpupillary Thermal
Therapy for occult CNVM in AMD) est terminộe, mais les
rộsultats nont pas encore ộtộ publiộs. La thermothộrapie
transpupillaire ou TTT utilise un laser diodes (810 nm)
de type infra-rouge pour traiter la MNVC sous-fovộale.
Le protocole du traitement recommande une faible illu-
mination, une longue durộe dexposition et une grande
surface dexposition pour crộer une hyperthermie gradu-
elle des vaisseaux sanguins de la choroùde. Lobjectif est
de crộer une obturation de la MNVC sans causer de
lộsions thermiques de la rộtine sus-jacente
16
. Le facteur
de croissance de la vascularisation endothộliale (VEGF)
est une protộine qui stimule la permộabilitộ et langio-
genốse vasculaires. On a constatộ des taux ộlevộs de
VEGF dans des maladies telles que la DMLA, oự la for-
mation active de vaisseaux sanguins est ộvidente. Linhi-
bition du VEGF est une approche utilisộe pour traiter ces
maladies. Le traitement anti-VEGF pour la MNVC sous-
fovộale, nộcessitant une sộrie dinjections intravitrộales,
est un domaine de recherche trốs passionnant et lon
devrait obtenir les rộsultats des ộtudes au cours des
prochaines annộes. Lacộtate danộcortave fait actuelle-
Ophtalmologie
Confộrences Scientifiques
9. Brent MH. Fluorescein angiography interpretation and quantitative assess-
ment of lesion area. A presentation at the PDT Users Meeting, Mt. Trem-
blant, Quebec; May 26, 2001.
10. The alpha-tocopherol, beta-carotene cancer prevention study group. The
effect of vitamin E and beta-carotene on the incidence of lung cancer and
other concerns in male smokers. N Engl J Med 1994;330:1029-1035.
11. Macular Photocoagulation Study Group. Argon laser photocoagulation for
neovascular maculopathy: five year results from randomized clinical trials.
Arch Ophthalmol 1991;109:1109-1114.
12. Treatment of Age-Related Macular Degeneration with Photodynamic
Therapy (TAP) Study Group. Photodynamic therapy of subfoveal choroidal
neovascularization in age-related macular degeneration with verteporfin:
two-year results of 2 randomized clinical trials: TAP Report no. 2. Arch Oph-
thalmol 2001;119:198-207.
13. Verteporfin in Photodynamic Therapy (VIP) Study Group. Verteporfin ther-
apy of subfoveal choroidal neovascularization in age-related macular
degeneration: two year results from a randomized clinical trial including
lesions with occult with no classic choroidal neovascularization:
Verteporfin in Photodynamic Therapy Report no. 2. Am J Ophthalmol
2001;131:541-560.
14. Verteporfin Roundtable 2000 and 2001 participants, Treatment of Age-
related macular degeneration with Photodynamic therapy (TAP) Study
Group Principal Investigators, and Verteporfin In Photodynamic therapy
(VIP) Study Group Principal Investigators. Guidelines for using verteporfin
(Visudyne
®
) in photodynamic therapy to treat choroidal neovascularization
due to age-related macular degeneration and other causes. Retina
2002;22:6-18.
15. Treatment of Age-Related Macular Degeneration with Photodynamic Ther-
apy and Verteporfin in Photodynamic Therapy Study Groups. Effect of lesion
size, visual acuity, and lesion composition on visual acuity change with and
without verteporfin therapy for choroidal neovascularization secondary to
age-related macular degeneration: TAP and VIP Report no. 1. Am J Ophthal-
mol 2003;136:407-418.
16. Mainster M A, Reichel E. Transpupillary thermotherapy for age-related
macular degeneration: Principles and techniques. Semin Ophthalmology
2001;16(2): 055-059.
Réunion scientifique à venir
4 au 5 juin 2004
Age-related Macular Degeneration Update 2004
Baltimore, Maryland
Renseignements : Tél. : 410-955-5880
Courriel :
ment l’objet d’études cliniques. Une injection juxtasclérale
postérieure est administrée sur la surface sclérale postérieure.
L’action du médicament est d’inhiber la croissance des vais-
seaux sanguins en inhibant les protéases nécessaires pour la
migration des cellules endothéliales vasculaires. Les études
SST (Submacular Surgery Trials) évaluent les avantages de
l’exérèse chirurgicale de la MNVC sous-fovéale dans la
DMLA. La fin du recrutement a eu lieu en 2001. Le suivi a été
terminé en septembre 2003 et les résultats devraient être
bientôt publiés. La translocation maculaire est une autre
approche chirurgicale pour traiter les patients affichant une
MNVC sous-fovéale dans la DMLA. Cette intervention con-
siste à détacher la rétine et à lui faire subir une rotation, afin
de déplacer la macula malade et de la replacer sur un
endothélium pigmentaire rétinien sain. La MNVC qui n’est
plus en position sous-fovéale, est donc accessible à la photo-
coagulation au laser thermique. Enfin, des études sont en
cours sur l’utilisation de prothèses visuelles à des fins de
réadaptation visuelle, comprenant le télescope miniaturisé
implantable et la vision artificielle à l’aide de microcircuits
intégrés épirétiniens et sous-rétiniens.
En conclusion, les nouvelles approches pour traiter la
DMLA et la technologie qui évolue rapidement modifient
les modes d’évaluation et de traitement de la DMLA. De
nouvelles modalités thérapeutiques intéressantes nous
permettront de relever les défis que pose cette maladie
dévastatrice et d’améliorer la qualité de vie de nos patients
atteints de DMLA.
Michael H. Brent, MD, FRCSC,
est professeur adjoint
d’Ophtalmologie et des Sciences de la vision, Université de
Toronto, et ophtalmologiste au Mount Sinai Hospital, Toronto
et au William Osler Health Centre, Campus de Brampton.
Références
1. National Advisory Eye Council. Vision Research- A National Plan: 1999-
2003, Vol 1. A report of the National Advisory Eye Council. Bethesda, Md:
National Institute of Health; 1999. NIH publication 98-4120.
2. The Age-Related Eye Disease Study Research Group. The Age-Related Eye
Disease Study (AREDS): Design Implications. AREDS Report No. 1. Control
Clin Trials 1999; 20:573-600.
3. Yannuzzi LA, Negrao S, Iida T, et al. Retinal angiomatous proliferation in
age-related macular degeneration. Retina 2001;21:416-434.
4. Klein R, Klein BEK, Linton KLP. Prevalence of age-related maculopathy.
Ophthalmology 1992;99:933-943.
5. The Age-Related Eye Disease Study Research Group. A randomized,
placebo-controlled, clinical trial of high-dose supplementation with vita-
mins C and E, beta-carotene, and zinc for age-related macular degeneration
and vision loss. AREDS Report No. 8. Arch Ophthalmol 2001;119:1417-1436.
6. Chew E. The Retina Debates 2003. New Technology and Controversies
from the Posterior Segment. A presentation at the American Academy of
Ophthalmology, Anaheim, California; November 14-15, 2003.
7. Seddon JM, Cote J, Rosner B. Progression of age–related macular degenera-
tion. Association with dietary fat, transunsaturated fat, nuts, and fish
intake. Arch Ophthalmol 2003;121:1728-1737.
8. Treatment of Age-Related Macular Degeneration with Photodynamic Ther-
apy (TAP) Study Group. Photodynamic therapy of subfoveal choroidal neo-
vascularization in age-related macular degeneration with verteporfin.
One-year results of 2 randomized clinical trials – TAP Report no.1. Arch
Ophthalmol 1999;117:1329-1345.
SNELL
© 2004 Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto, seul responsable du contenu de cette publication. Édition : SNELL Communication
Médicale Inc. avec la collaboration du Département d’ophtalmologie et des sciences de la vision, Faculté de médecine, Université de Toronto.
MD
Ophtalmologie – Conférences scientifiques est une marque
de commerce de SNELL Communication Médicale Inc.Tous droits réservés. L’administration d’un traitement thérapeutique décrit ou mentionné dans Ophtalmologie – Conférences scientifiques doit
toujours être conforme aux renseignements d’ordonnance approuvés au Canada. SNELL Communication Médicale se consacre à l’avancement de l’éducation médicale continue de niveau supérieur.
L’élaboration de cette publication a bénéficié d’une subvention à l’éducation de
Novartis Ophthalmics
130-005F
La version française a été revisée par le professeur Pierre Lachapelle,
Montréal.
Les avis de changement d’adresse et les demandes d’abonne-
ment pour Ophtalmologie – Conférences Scientifiques doivent
être envoyés par la poste à l’adresse C.P. 310, Succursale H,
Montréal (Québec) H3G 2K8 ou par fax au (514) 932-5114 ou
par courrier électronique à l’adresse
Veuillez vous référer au bulletin Ophtalmologie – Conférences
Scientifiques dans votre correspondence. Les envois non
distribuables doivent être envoyés à l’adresse ci-dessus.
Poste-publications #40032303
Ophtalmologie
Conférences Scientifiques
MARS 2004
Volume 2, numéro 3
COMPTE RENDU DES CONFÉRENCES
SCIENTIFIQUES DU DÉPARTEMENT
D’OPHTALMOLOGIE ET
DES SCIENCES DE LA VISION,
FACULTÉ DE MÉDECINE,
UNIVERSITÉ DE TORONTO
Département d’ophtalmologie
et des sciences de la vision
Faculté de médecine
Université de Toronto
60 Murray St.
Bureau 1-003
Toronto (Ontario) M5G 1X5
Le contenu rédactionnel d’Ophtalmologie –
Conférences scientifiques est déterminé
exclusivement par le Département
d’ophtalmologie et des sciences de la vision,
Faculté de médicine, Université de Toronto.
Département d’ophtalmologie
et des sciences de la vision
Jeffrey Jay Hurwitz, M.D., Rédacteur
Professeur et président
Martin Steinbach, Ph.D.
Directeur de la recherche
The Hospital for Sick Children
Elise Heon, M.D.
Ophtalmologiste en chef
Mount Sinai Hospital
Jeffrey J. Hurwitz, M.D.
Ophtalmologiste en chef
Princess Margaret Hospital
(Clinique des tumeurs oculaires)
E. Rand Simpson, M.D.
Directeur, Service d’oncologie oculaire
St. Michael’s Hospital
Alan Berger, M.D.
Ophtalmologiste en chef
Sunnybrook and Women’s College
Health Sciences Centre
William S. Dixon, M.D.
Ophtalmologiste en chef
The Toronto Hospital
(Toronto Western Division and
Toronto General Division)
Robert G. Devenyi, M.D.
Ophtalmologiste en chef
Pathologie oculaire : les lésions
conjonctivales pigmentaires
PAR
YENI H. YÜCEL
, M.D., PH.D., FRCPC
La richesse et la diversité qui caractérisent le domaine de la pathologie oculaire
ont servi d’assise à la pratique de l’ophtalmologie clinique. L’application de la patholo-
gie en ophtalmologie a eu un impact phénoménal sur notre compréhension de l’his-
toire naturelle des maladies oculaires et de la réponse des tissus aux différentes
modalités thérapeutiques. De plus, en tentant de déterminer comment et pourquoi des
cellules oculaires en viennent à abandonner leurs relations physiologiques et leurs
rôles normaux, la pathologie oculaire constitue une interface entre l’ophtalmologie
expérimentale et l’ophtalmologie clinique. Le présent numéro d’
Ophtalmologie —
Conférences scientifiques
met en lumière ce rôle d’interface en examinant trois cas de
lésions mélanocytaires conjonctivales.
Comme l’œil peut être examiné et imagé directement, l’ophtalmologie a pu
exploiter considérablement la corrélation entre les manifestations cliniques et les don-
nées pathologiques de la maladie. Qu’il soit effectué à la suite d’une cytoponction,
d’une biopsie, d’une éviscération, d’une énucléation ou d’une exentération, l’examen
pathologique d’un échantillon de tissu oculaire joue un rôle important dans l’arbre
décisionnel conduisant au diagnostic et au traitement des patients. Le fait de procurer
des renseignements cliniques pertinents au pathologiste peut donner une valeur
ajoutée aux études pathologiques. Les corrélations clinico-pathologiques continuent
d’avoir une importance fondamentale pour la pratique clinique de l’ophtalmologie et
sont hautement pertinentes dans l’étude des nouvelles maladies et des nouveaux
traitements en émergence.
Le rôle de la pathologie oculaire n’est nulle part plus évident que dans la prise en
charge d’un patient présentant une tumeur primaire ou secondaire soupçonnée ou
avérée. L’examen pathologique est essentiel pour établir une distinction entre des lésions
bénignes, précancéreuses et cancéreuses. Cette information est nécessaire pour permettre
le traitement adéquat des tumeurs malignes, tout en évitant un traitement trop agressif
des lésions bénignes et précancéreuses. Le traitement des lésions épibulbaires est un
exemple classique d’une situation dans laquelle la collaboration entre le chirurgien et le
pathologiste permet la meilleure issue possible pour les patients.
Les lésions conjonctivales épibulbaires
Dans le cas des lésions conjonctivales épibulbaires non pigmentaires, le diagnostic est
habituellement basé sur les caractéristiques cliniques des lésions. Le diagnostic différen-
tiel comprend la pinguécolite, l’épisclérite, le kyste conjonctival, la conjonctivite
MC
Département
d’ophtalmologie et des
sciences de la vision
FACULTY OF MEDICINE
University of Toronto
Disponible sur Internet à :
www.ophtalmologieconferences.ca
allergique, le granulome à corps étranger, le lymphan-
giome, et la néoplasie de l’épithélium pavimenteux
1
.
Dans le cas des lésions conjonctivales épibulbaires
pigmentaires, les renseignements qui aident à dis-
tinguer les lésions pigmentaires bénignes des lésions
malignes et des lésions qui ont un potentiel de mali-
gnité comprennent l’âge et la pigmentation cutanée du
patient, de même que la localisation, la couleur, la taille
et la hauteur de la lésion. Le diagnostic différentiel
comprend un certain nombre de manifestations, telles
que la mélanose conjonctivale d’origine ethnique, la
mélanose primaire acquise, la mélanose secondaire, le
nævus, le mélanome, la mélanocytose oculaire, et
l’extension extraoculaire d’un mélanome uvéal
1
. Il peut
ne pas être possible de baser un diagnostic uniquement
sur les caractéristiques cliniques d’une lésion; la biopsie
aux fins d’examen histopathologique peut alors aider
à formuler un diagnostic et à établir le pronostic du
patient. Pour illustrer nos propos, nous vous présentons
trois cas de lésions conjonctivales mélanocytaires.
Figure 1 : Lésion kystique pigmentaire dans la
conjonctive bulbaire temporale
Figure 2 : Coupe histologique colorée à
l’hématoxyline-éosine montrant l’épithélium
conjonctival (flèche) et la substantia propria
Un homme blanc âgé de 45 ans présente une
lésion kystique pigmentaire dont le volume aug-
mente progressivement dans la conjonctive bul-
baire temporale de l’œil droit (figure 1). La lésion
de couleur brune mesure 3,5 x 3 mm. Après une
excision chirurgicale, le spécimen est soumis à un
examen pathologique.
La figure 2, avec coloration à l’hématoxyline-
éosine, montre l’épithélium conjonctival (flèche)
et la substantia propria. On note la présence de
cellules de nævus pigmentaire dans l’épithélium
et d’autres nids de cellules næviques dans la sub-
stantia propria. De nombreux kystes épithéliaux
sont également présents (C). Les marges de résec-
tion (non montrées) ne présentent pas de cellules
næviques. Selon le diagnostic pathologique, il
s’agit d’un nævus conjonctival pigmentaire com-
plètement réséqué.
Commentaire : Dans ce cas de nævus conjonc-
tival pigmentaire, le changement de la taille
apparente de la lésion résulte probablement
d’une augmentation du volume des kystes intrin-
sèques. L’implication des kystes épithéliaux dans
l’augmentation de la taille de ces lésions a été
décrite à plusieurs reprises
2-4
. D’autres causes pos-
sibles d’une telle augmentation peuvent être une
inflammation au cœur du nævus, une augmenta-
tion de la pigmentation de régions du nævus qui
ne contenaient auparavant pas de mélanine, ou
encore une croissance néoplasique. C’est l’exa-
men histopathologique qui est le plus à même
d’évaluer ces différentes causes.
Cas n° 1 — Un nævus conjonctival pigmentaire
C
c = kyste
La calibration indique 250 µm.