Sinh bệnh học các biến chứng mạn bệnh đái tháo đường
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (698.29 KB, 10 trang )
7
SINH BỆNH HỌC CÁC BIẾN CHỨNG MẠN BỆNH ĐÁI THÁO ĐƯỜNG
Nguyễn Thị Thu Thảo*
ĐẶT VẤN ĐỀ
Trong nhiều năm gần đây, mức độ quan
trọng của biến chứng do đái tháo đường
(ĐTĐ) đã có nhiều thay đổi. Thật vậy, các biến
chứng cấp do ĐTĐ ngày càng ít gặp, trong khi
các biến chứng mạn ngày càng gia tăng do các
lý do sau
(12)
:
Tỉ lệ bệnh ĐTĐ ngày càng gia tăng trên
toàn thế giới nhưng do có sự cải thiện về
phòng bệnh và điều trị tích cực bệnh ĐTĐ đã
giúp ngăn ngừa các biến chứng cấp và làm
chậm sự xuất hiện của các biến chứng mạn.
Bên cạnh đó dân số ngày càng già hơn, không
chỉ ở các nước phương Tây mà còn cả ở các
nước đang phát triển cũng góp phần làm gia
tăng bệnh ĐTĐ trên toàn cầu. Trong đó bệnh
ĐTĐ típ 2 chiếm tỉ lệ lớn, chủ yếu xảy ra sau
tuổi 40, là một bệnh diễn tiến chậm khó xác
định được thời điểm bị bệnh, nên ngay ở thời
điểm bệnh được chẩn đoán đã có thể xuất hiện
ít nhiều các biến chứng mạn. Nếu không được
chẩn đoán sớm và điều trị kịp thời, các biến
chứng sẽ gia tăng góp phần làm gia tăng tỉ lệ
biến chứng mạn của ĐTĐ.
Các biến chứng mạn làm gia tăng độ tàn
phế và tử vong trên bệnh nhân ĐTĐ. Vì thế,
gánh nặng biến chứng mạn do ĐTĐ sẽ gia
tăng nhanh trong những năm tới, trong đó bao
gồm các biến chứng mạch máu lớn và mạch
máu nhỏ.
ĐỊNH NGHĨA
Bệnh đái tháo đường là một nhóm bệnh
chuyển hoá được đặc trưng bởi tình trạng tăng
đường huyết do hậu quả của sự thiếu insulin
tương đối hoặc tuyệt đối. Tình trạng tăng
đường huyết lâu dài sẽ gây ra nhiều rối loạn
chức năng ở các cơ quan, đặc biệt là các mạch
máu lớn và mạch máu nhỏ
(4)
. Cơ chế bệnh sinh
của bệnh ĐTĐ típ 2 bao gồm nhiều yếu tố
phức tạp, diễn tiến trong nhiều năm, đó là:
- Đề kháng insulin làm giảm sự thu nạp
glucose ở mô ngoại vi, đây là hiện tượng quan
trọng khởi đầu trong bệnh ĐTĐ típ 2.
- Cơ chế thứ hai là tình trạng tăng sản xuất
glucose từ gan, bình thường khi glucose máu
tăng, insulin sẽ gắn vào thụ thể đặc hiệu để ức
chế sự sản xuất glucose từ gan; nếu không có
sự ức chế này, glucose máu sẽ tăng cao và
glycogen bị lắng đọng.
- Cơ chế thứ ba là có rối loạn tiết insulin
của tế bào β tụy, mặc dù đề kháng insulin là
hiện tượng khởi đầu trong bệnh ĐTĐ típ 2,
nhưng nếu chỉ riêng đề kháng insulin thì
không đủ để gây bệnh; chính đáp ứng của tế
bào β với tình trạng đề kháng insulin mới là
yếu tố quyết định diễn tiến đến rối loạn dung
nạp glucose và ĐTĐ típ 2, và chính điều này
giúp cho sự quyết định chọn lựa cách điều trị.
Tuy nhiên, dù cơ chế bệnh sinh khác nhau,
nhưng các biến chứng mạn đều xảy ra ở cả 2
típ ĐTĐ bao gồm các biến chứng mạch máu
lớn, mạch máu nhỏ và các biến chứng không
phải mạch máu
(12).
CÁC BIẾN CHỨNG MẠN CỦA ĐTĐ
Tất cả các biến chứng mạn tính của bệnh
ĐTĐ đều có thể gặp trong ĐTĐ típ 1 cũng như
ĐTĐ típ 2. Tuy nhiên, có những biến chứng hay
gặp trong ĐTĐ típ này nhiều hơn trong típ kia
(3)
.
Bệnh nhân ĐTĐ típ 2 tử vong nhiều nhất do các
biến chứng tim mạch, còn bệnh nhân ĐTĐ típ 1
tử vong nhiều nhất do biến chứng thận
(9)
.
Các biến chứng mạn gia tăng theo tình
trạng tăng đường huyết kéo dài, thường xuất
hiện sau thập kỷ thứ hai của bệnh, bởi vì ĐTĐ
típ 2 có một thời gian dài không triệu chứng và
nhiều bệnh nhân ĐTĐ típ 2 đã có các biến
*
Khoa Nội Tiết - Thận
, Bệnh Viện Nhân Dân Gia Định
8
chứng ngay tại thời điểm mới chẩn đoán
(12)
.
Việc điều trị, dù được tuân thủ và theo dõi
nghiêm ngặt cũng khó lòng đạt được mục đích
kiểm soát đường huyết tối ưu lâu dài. Vì lẽ đó,
sự xuất hiện của một hoặc nhiều biến chứng
mạn trong quá trình diễn tiến bệnh là điều khó
tránh khỏi. Các biến chứng mạn của ĐTĐ
được phân chia thành hai loại là biến chứng
mạch máu và không phải mạch máu
(12)
.
.
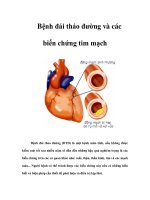
Hình 1: Các biểu hiện lâm sàng của bệnh ĐTĐ
(11)
- Các biến chứng mạch máu bao gồm biến
chứng mạch máu nhỏ (mắt, thận, thần kinh) và
biến chứng mạch máu lớn (bệnh mạch vành, bệnh
mạch máu ngoại biên và bệnh mạch máu não).
- Các biến chứng không phải mạch máu
bao gồm rối loạn tiêu hoá, rối loạn tình dục,
nhiễm trùng (hình 1) và những thay đổi ở da.
SINH LÝ BỆNH CÁC BIẾN CHỨNG MẠN CỦA
BỆNH ĐTĐ
(12)
Tác dụng trực tiếp của tăng đường huyết
lên sự xuất hiện các biến chứng ĐTĐ đã được
bàn cải từ lâu. Độ trầm trọng của các biến
chứng mạch máu nhỏ có liên hệ mật thiết với
thời gian mắc bệnh và mức tăng đường huyết
(Sơ đồ 1).
Nghiên cứu DCCT thực hiện trên 1441 trên
bệnh nhân ĐTĐ típ 1 công bố năm 1993 và
nghiên cứu UKPDS thực hiện trên 5102 bệnh
nhân ĐTĐ típ 2 công bố năm 1998 cho thấy
nếu kiểm soát đường huyết (ĐH) chặt chẽ sẽ
làm giảm rõ rệt nguy cơ phát triển và diễn tiến
của các biến chứng mạch máu nhỏ.
Bệnh lý võng
mạc
Đục thủy tinh thể
Bệnh lý
thận (suy
thận)
Bất lực
Rối loạn thần kinh tự
ñộng (dạ dày giảm co
bóp, tiêu chảy)
Bệnh mạch vành (ñau
ngực, NMCT, …)
Bệnh mạch máu não
Bệnh lý thần kinh ngoại
biên (ñau, mất cảm
giác)
Bệnh mạch máu ngoại
biên (cắt cụt chi)
9
Sơ ñồ 1: Cơ chế bệnh sinh của tăng ñường huyết mạn tính
(15)
Thuyết chuyển hoá
(5)
Glycat hoá protein không enzyme
Glucose + Protein Shiff base (Aldimine) Ketoamin
Là sự gắn kết của một phân tử glucose với
một protein mà không cần enzym. Lysine và
Valine là 2 vị trí acid amin đầu tiên mà glucose
gắn kết. Khi glucose kết hợp với protein sẽ làm
thay đổi cấu trúc và chức năng của các protein.
Đường huyết càng tăng và sự tiếp xúc giữa
đường và protein càng lâu thì quá trình này càng
lan rộng. Quá trình glycat hoá sản sinh ra các gốc
tự do và các sản phẩm gọi chung là AGE
(Advanced Glycosylation End products)
(15)
. AGE
có vai trò rất quan trọng trong cơ chế bệnh sinh
các biến chứng mạn của ĐTĐ.
Khi AGE gắn vào các thụ thể của nó, chủ
yếu ở các đại thực bào và các tế bào nội mạc
mạch máu, các nguyên bào sợi, tế bào trung
mô sẽ gây phóng thích các yếu tố gây hoại tử
mô (TNF), interleukin I, yếu tố tăng trưởng
giống insulin (IGF 1), và các yếu tố tăng
trưởng tiểu cầu (PDGF), các yếu tố của mô,
gây tăng tính thấm thành mạch và ảnh hưởng
đến quá trình đông máu. Ngoài ra, PDGF còn
làm tăng sản xuất chất nền ở tế bào trung mô
gây ra những biến đổi tại cầu thận. AGEs trên
bề mặt hồng cầu của người bị ĐTĐ sẽ gắn kết
với các tế bào nội mạc, gây ra các stress oxy
hóa là yếu tố quan trọng trong sự phát triển
các biến chứng mạch máu.
May thay trên thực nghiệm ở động vật,
người ta nhận thấy aminoguanidine ức chế sự
thành lập AGEs, là chất có vai trò dự phòng
Tăng ñường
huyết
• Tăng hoạt tính men
Aldose Reductase
• Tích tụ Sorbitol
• Giảm myoinositol
• Thay ñổi hoạt ñộng
bơm Na - KATPase
• Tăng hoạt tính DAG và
β2 PKC
• Thay ñổi tính co thắt và ñáp
ứng hormone của cơ trơn
mạch máu.
• Thay ñổi tính thấm của TB
nội mô
• Tăng quá trình Glycat hoá
không enzym
• Hoạt hoá các thụ thể AGE
ñại thực bào và TB nội mô
• Thay ñổi lipoprotein, chất
nền và cấu trúc protein của
màng cơ bản
Các biến chứng ñái tháo ñường
10
một số biến chứng của ĐTĐ ở động vật làm
ngăn ngừa sự hoạt hoá đại thực bào, sự kích
thích các cytokin, bài tiết các yếu tố tăng
trưởng, tăng tính thấm của tế bào nội mạc. Do
đó, việc điều trị bằng aminoguanidine cho các
bệnh nhân ĐTĐ sẽ làm chậm các biến chứng
thần kinh, võng mạc và bệnh lý thận do ĐTĐ
(15)
.
Quá trình glycat hóa có thể xảy ra với
hemoglobin, albumin, protein của thủy tinh
thể, fibrin, collagen, lipoprotein và hệ thống
glycoprotein trong tế bào nội bì của gan,
antithrombin gây ra những thay đổi về cấu
trúc và chức năng của các thành phần kể
trên. Vì thế, AGEs có vai trò rất quan trọng
trong cơ chế bệnh sinh của các biến chứng
mạn của ĐTĐ.
Glycat hoá hemoglobin
Là một trong những quá trình glycat hóa
được nhấn mạnh trên bệnh nhân bị ĐTĐ.
Hemoglobin bị glycat hóa có ái lực cao với oxy
nên khó phóng thích oxy hơn so với
hemoglobin bình thường
(15)
, gây ra tình trạng
thiếu oxy đồng thời làm giảm khả năng biến
dạng của hồng cầu, ảnh hưởng đến đặc tính
huyết lưu. Ở trạng thái bình thường, sự giảm
chuyển nhượng oxy cho mô không đủ gây
khuyết dưỡng nhưng sẽ trở nên quan trọng
khi nhu cầu oxy của mô gia tăng
(1)
.
HbA Pre A1c HbA1c.
Glycat hóa albumin
Khi glucose kết hợp với albumin sẽ làm
albumin bị biến dạng, cấu trúc và chức năng bị
thay đổi. Albumin bị glycat hóa sẽ không được
thu nhận ở gan bởi các glycoprotein và được
đưa vào thành các mạch máu nhỏ nhanh hơn
các albumin bình thường, làm xơ hoá cầu thận
ở người bị ĐTĐ
(15)
.
Glycat hóa fibrin
Fibrin bị glycat hóa sẽ không được tiêu hủy
bởi plasmin, do đó tích tụ lại ở các mô của
người bị ĐTĐ và làm ảnh hưởng đến quá trình
đông máu.
Glycat hóa protein của thủy tinh thể
Thúc đẩy sự hình thành đục thuỷ tinh thể
do sự gia tăng các cầu nối disulfide giữa các
phân tử protein làm tăng sản xuất NO làm dãn
các mạch máu ở võng mạc. Tuy nhiên, cơ chế
gây đục thuỷ tinh thể còn chưa được biết rõ hết.
Glycat hóa collagen
(12)
Các collagen bị glycat hóa sẽ kém hòa tan
và khó bị thoái giáng hơn so với collagen bình
thường. Người ta nghi ngờ có lẽ đây là chất có
vai trò quan trọng trong sự làm dầy màng đáy
cơ bản cầu thận ở người bị ĐTĐ dẫn đến tăng
tính thấm của màng cơ bản. Ngoài ra, quá trình
glycat hóa còn gây rối loạn cấu trúc lớp
collagen của da, làm hạn chế cử động khớp
được xem như là các yếu tố nguy cơ làm gia
tăng các biến chứng muộn của ĐTĐ.
Glycat hóa màng hồng cầu
Đóng vai trò quan trọng trong việc làm
giảm thời gian sống sót của tế bào hồng cầu,
làm mất khả năng biến dạng của hồng cầu
bình thường nơi người bị ĐTĐ không được
kiểm soát tốt, làm giảm tốc độ máu lưu thông,
gây thiếu máu cục bộ ở cầu thận và võng mạc.
Ngoài ra, AGE trên bề mặt hồng cầu của
người bị đái tháo đường sẽ gắn kết với các tế
bào nội mạc, gây ra các stress oxy hoá là yếu tố
quan trọng trong sự phát triển các biến chứng
mạch máu.
Glycat hóa myelin protein làm giảm tốc độ
dẫn truyền thần kinh gây nên bệnh lý thần
kinh ngoại vi do ĐTĐ.
Glycat hóa màng tế bào bạch cầu máu làm
giảm sự điều hòa thẩm thấu, tình trạng xuyên
mạch, giảm hoạt động của các thực bào và của
các vi khuẩn, đáp ứng miễn dịch qua trung
gian tế bào đưa đến tình trạng dễ nhiễm trùng
trên bệnh nhân ĐTĐ.
Glycat hóa yếu tố Von Willebrand’s
Glycat hóa quá mức các yếu tố Von
Willebrand’s góp phần làm gia tăng kết dính
11
Aldose reductase
Sorbitol dehydrogenase
↓
Myoinsitol
↓
Na
+
K
+
ATPase
NAD
+
NADH
tiểu cầu ở người ĐTĐ kiểm soát kém gây ra
các biến chứng mạch máu lớn của bệnh ĐTĐ.
Glycat hóa lipoprotein
AGEs tác động trực tiếp với các lipoprotein
torng huyết tương ngăn không cho các mô
nhận biết được thụ thể LDL. Các LDL
cholesterol bị glycat hóa sẽ không được thu
nhận tại các thụ thể LDL trên bề mặt tế bào
gan do đó làm tăng LDL trong huyết tương.
Trong khi đó, ngược lại, HDL bị glycat hóa sẽ
chuyển hoá nhanh hơn nên làm giảm HDL
trong huyết tương đưa đến hậu quả rối loạn
chuyển hoá lipid, góp phần gây xơ vữa mạch
máu nơi người bị ĐTĐ.
Chuyển hoá Glucose theo con đường
polyol
(15)
Chuyển hoá glucose theo con đường
polyol góp phần gây ra glycat hoá protein
không enzym.
Giai đoạn 1 của con đường polyol là tạo ra
sorbitol (Sơ đồ 2).
Ở người bình thường, Glucose vào tế bào
được phosphoryl hoá bởi men hexokinase để
tạo ra G6 – phosphat và tiếp tục đi theo con
đường ly giải vào chu trình Krebs để tạo năng
lượng. Và như vậy ở người bình thường con
đường polyol là con đường chuyển hoá phụ.
Ở người ĐTĐ, khi đường huyết tăng,
Glucose vào tế bào do sự chênh lệch áp suất
thẩm thấu, do đó Glucose trong tế bào tăng và
men hexokinase bị bão hoà, lúc này men
aldose reductase được hoạt hoá và Glucose
trong tế bào được chuyển hoá theo con đường
polyol để tạo sorbitol dưới tác dụng của men
aldose reductase vốn có nhiều ở võng mạc, cầu
thận, thủy tinh thể, tế bào schwann và động
mạch chủ.
Do sorbitol không qua màng tế bào nên bị
tích tụ lại trong tế bào, gây ra những thay đổi
về áp suất thủy tĩnh, làm phá hủy tế bào. Sự
tích tụ sorbitol bao gồm ở mô thần kinh và các
mô khác như cầu thận, võng mạc .v.v… Sự tích
tụ này làm giảm myoinositol trong tế bào, vốn
rất cần cho hoạt động của hệ Na
+
- K
+
ATPase,
do đó làm giảm hoạt động của hệ này là hệ
duy trì điện thế của màng tế bào. Khi hệ thống
này hoạt động kém sẽ làm rối loạn hoạt động
khử cực của tế bào, tức làm thay đổi điện thế
màng và vận tốc dẫn truyền thần kinh, làm
chết các chu bào. Các biến đổi sinh hoá này
làm giảm nồng độ glutathion, sinh tố E và sinh
tố C vốn có vai trò thải trừ các gốc tự do gây
độc tế bào. Vì thế, việc điều trị với các chất
chống oxy hoá như sinh tố E, C, … sẽ cải thiện
chức năng mạch máu nhỏ và tim mạch ở bệnh
nhân ĐTĐ.
Glucose Sorbitol Fructose
Sơ đồ 2: Cơ chế tác động của con đường Polyol lên chức năng tế bào
(2)
Người ta đã chứng minh rằng các bệnh lý
thần kinh ngoại vi, bệnh lý võng mạc, đục
thủy tinh thể, bệnh lý thận do ĐTĐ ở động vật
có thể phòng ngừa bằng cách ức chế con
đường polyol. Tuy nhiên, nhiều thử nghiệm
trên người khi ức chế men aldose reductase đã
không chứng minh được hiệu quả có lợi trên
lâm sàng ở các biến chứng mạch máu nhỏ.
Giai đoạn 2 của con đường polyol là sự tạo
ra fructose (Sơ đồ 2)
Là đường có áp lực thẩm thấu cao hơn rất
nhiều so với Glucose. Fructose có vai trò quan
NADP NADPH
Rối loạn chức năng tế bào
12
trọng trong việc gây ra các biến chứng mạn
ĐTĐ hơn là giai đoạn chuyển hoáthành
sorbitol vì quá trình glycat hóa xảy ra với
fructose nhanh hơn Glucose gấp 7 – 8 lần.
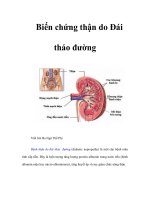
Hình 2: Sự hoạt hoá PKC và tích tụ AGE
(13)
Hoạt hóa Protein Kinase C (PKC)
(12)
Khi đường huyết tăng sẽ kích hoạt tổng
hợp diacylglycerol và làm hoạt hóa men PKC.
PKC bị hoạt hóa, làm thay đổi sự sao chép gen
cho fibronectin, collagen loại IV, các protein co
cơ, các protein nền trong tế bào nội bì và các
neurons. Các yếu tố tăng trưởng xuất hiện
đóng vai trò quan trọng trong biến chứng mạn
của ĐTĐ, như yếu tố tăng trưởng nội mạc
mạch máu (VEGF) và yếu tố tăng trưởng giống
insulin (IGF-β). Yếu tố tăng trưởng nội mạc
mạch máu gia tăng trong bệnh võng mạc tăng
sinh do ĐTĐ, còn yếu tố tăng trưởng giống
insulin gia tăng trong bệnh thận ĐTĐ, kích
thích các tế bào trung mô tăng sản xuất
collagen và fibronectin, làm dầy màng đáy cơ
bản ở cầu thận (Sơ đồ 3).
13
Sơ đồ 3: Cơ chế phân tử và tế bào trong biến chứng mạch máu của bệnh ĐTĐ
(11)
Tăng đường huyết
↑
Aldose Reductase
↑
Sorbitol
↓
Myoinositol
↓
Na
+
/K
+
ATPase
↑
vasodilatory
prostaglandins
↑ NADH
NAD
+
Tỉ lệ
Thay đổi tình trạng
redox tế bào
↑ Diacyl glycerol
Hoạt hoá PKC
↑
acid arachidonic
↑ AGEs
Thay đổi:
Chức năng Protein
Dẫn truyền tín hiệu
Biểu lộ gen
↓
Na
+
/K
+
ATPase
Rối loạn chức năng mạch máu
14
Ngoài ra, các yếu tố tăng trưởng khác như yếu tố tăng trưởng tiểu cầu, yếu tố tăng
trưởng nội bì, các yếu tố tăng trưởng giống insulin, hormôn tăng trưởng (GH), các
nguyên bào sợi, thậm chí cả insulin cũng gợi ý là có vai trò quan trọng trong các biến
chứng của ĐTĐ.
Tăng ĐH, mặc dù được xem là yếu tố khởi động ban đầu trong biến chứng ĐTĐ, tuy
nhiên vẫn còn chưa xác định rõ liệu có cùng tiến trình sinh bệnh lý ở tất cả các biến
chứng hay tiến trình này chỉ xảy ra ở một vài cơ quan mà thôi. Cuối cùng, stress oxy hóa
và sự hình thành các gốc tự do là hậu quả của tăng đường huyết, cũng có thể thúc đẩy
sự phát triển các biến chứng mạn ĐTĐ. Như vậy, các sản phẩm oxy hóa có thể xuất phát
từ quá trình glycat hóa hoặc do tăng hoạt tính oxy hóa khi kích hoạt protein kinase. Do
đó việc điều trị với những chất chống oxy hóa sẽ cải thiện được các biến chứng mạn ở
bệnh nhân ĐTĐ vì ngăn sự hoạt hóa protein kinase.
Rối loạn huyết động học
(12,15)
Các rối loạn huyết động học do bất thường về nội tiết dẫn đến tăng độ lọc cầu
thận, tăng lượng máu đến thận và tăng áp suất thủy tĩnh mao mạch cầu thận làm
tăng áp lực cầu thận. Từ đó, gây nên các tổn thương cầu thận do ĐTĐ.
Ở người bình thường, tại thận các tiểu động mạch đến và đi khỏi cầu thận có thể co
dãn độc lập để điều chỉnh áp lực lưu lượng máu ở cầu thận. Nếu huyết áp hệ thống
giảm, động mạch tới cầu thận sẽ dãn nở để duy trì độ lọc cầu thận. Khi huyết áp hệ
thống tăng, động mạch tới cầu thận sẽ co lại để làm giảm áp lực ở cầu thận.
Trên bệnh nhân ĐTĐ, thận sẽ mất cơ chế tự điều chỉnh này, hậu quả là làm tăng áp
lực mao mạch và tăng áp lực cầu thận, từ đó gây nên các tổn thương cầu thận do ĐTĐ
(5)
.
Giai đoạn đầu huyết áp còn bình thường, nhưng sức đề kháng ở tiểu động mạch cầu
thận đã bắt đầu giảm. Khi áp suất thủy tĩnh tại các giường mạch máu gia tăng sẽ làm
tăng sự lọc protein và các đại phân tử khác bao gồm các phức hợp miễn dịch qua thành
mạch máu và trung mô, làm tổn thương trung mô và màng đáy cơ bản. Những thay đổi
về lưu lượng máu có thể đảo ngược khi:
- Kiểm soát đường huyết tốt.
- Dùng thuốc ức chế men aldose reductase.
- Dùng thuốc ức chế men chuyển.
Tuy nhiên, giả thuyết về huyết động học ít thuyết phục hơn các giả thuyết trên,
nhưng cho thấy có mối liên hệ rõ rệt trong bệnh thận ĐTĐ.
THUYẾT DI TRUYỀN
Đa số các tác giả đều cho rằng, tăng đường huyết mạn tính và các bất thường về
chuyển hoá gây ra các biến chứng mạn của ĐTĐ. Tuy nhiên, bên cạnh các yếu tố trên
cũng còn nhiều yếu tố chưa xác định rõ cũng có liên quan đến sự phát triển các biến
chứng mạn do ĐTĐ. Sự tiến triển của bệnh lý thận không liên quan rõ ràng với thời gian
mắc bệnh ĐTĐ hay sự kiểm soát ĐH, và ở người sự tăng ĐH đơn độc không đủ để giải
thích những tổn thương thận trên gần nữa số bệnh nhân ĐTĐ
(10)
.
Tần suất bệnh thận đái tháo đường thay đổi theo chủng tộc. Nhiều nghiên cứu cho
thấy các chủng tộc gốc Phi hoặc châu Á có nguy cư mắc bệnh thận ĐTĐ nhiều hưn
15
người da trắng gấp 6 đến 13,6 lần, và hầu hết những bệnh nhân có trực hệ gần với
người bệnh thận đái tháo đường thì dễ bị bệnh thận ĐTĐ
(8)
.
Người ta ghi nhận một số bệnh nhân ĐTĐ típ 2 có đường huyết tăng cao kéo dài lại
không bao giờ có biến chứng thận hoặc biến chứng mắt. Ngược lại, một số bệnh nhân
ĐTĐ típ 2 được kiểm soát đường huyết tốt thì lại bị biến chứng mạch máu nhỏ. Vì lẽ đó,
người ta cho rằng có lẽ yếu tố di truyền cũng có vai trò đặc biệt trong sự phát triển các
biến chứng mạn
(12)
. Tuy nhiên, vấn đề này cũng còn đang tranh cãi.
Nhiều nghiên cứu dịch tễ gợi ý có tác động qua lại giữa các yếu tố chuyển hóa như
đường huyết cao và yếu tố di truyền trong sự tiến triển bệnh lý thận do ĐTĐ. Hiện
tượng hàng loạt bệnh lý thận cùng xảy ra trên anh chị em cho thấy yếu tố gia đình góp
phần trong bệnh lý thận do đái tháo đường. Ngoài ra các đối tượng có tầm vóc thấp,
nhẹ cân lúc sinh cũng có nguy cơ cho sự phát triển bệnh thận ĐTĐ được giải thích có
lẽ do giảm số lượng nephron
(10)
.
Các nghiên cứu cũng chứng minh tính đa dạng của men chuyển angiotensin I là
yếu tố nguy cơ làm gia tăng bệnh mạch máu lớn do đái tháo đường
(7)
. Một nghiên cứu
ở Pháp
(15)
với 316 bệnh nhân đái tháo đường tip 2 cho thấy có sự giảm đáng kể gen tạo
men chuyển angiotensin, là yếu tố nguy cơ độc lập và mạnh mẽ cho việc khởi phát
bệnh mạch vành ở giai đoạn sớm, độc lập với tăng huyết áp và mức lipid máu. Tuy
nhiên, bằng chứng này lại không được khẳng định ở một số dân tộc khác
(14,15)
.
Ngoài ra một bằng chứng củng cố cho tính di truyền trong sự phát triển biến
chứng mạch máu lớn là mức lipoprotein(a). là yếu tố nguy cơ cho bệnh vữa xơ mạch
máu. Trong một nghiên cứu ở ÚC trên bệnh nhân đái tháo đường típ 2 có tiểu đạm,
người ta nhận thấy mức lipoprotein(a) tăng rất cao trong máu. Điều này cũng tương tự
như một nghiên cứu ở người Mỹ La tinh bị ĐTĐ típ 2. Tuy nhiên bằng chứng này lại
không được khẳng định trong một nghiên cứu ở Đan mạch cũng thực hiện trên bệnh
nhân đái tháo đường típ 2 có tiểu đạm cho thấy mức lipoprotein(a) không tăng
(15).
Người ta cho rằng có một hệ di truyền nhạy cảm cho sự xuất hiện các biến chứng
mạch máu nhỏ trên bệnh nhân đái tháo đường, đặc biệt là đối với bệnh lý thận và bệnh
lý thần kinh
.
KẾT LUẬN
Cơ chế sinh bệnh học của các biến chứng mạn do ĐTĐ mặc dù đã được nghiên cứu
rất nhiều qua các thử nghiệm nhưng cho đến nay vẫn còn nhiều bàn cãi và vẫn cần phải
tiếp tục nghiên cứu. Việc điều trị bằng các chất ức chế sự thành lập AGE hay ức chế men
aldose reductase (Sorbinil) hoặc sử dụng các tác nhân chống oxy hoá cho đến nay vẫn chưa
có hiệu quả rõ ràng.
Các nghiên cứu DCCT và UKPDS cũng như nhiều nghiên cứu lâm sàng ngẫu nhiên
cho cả 2 típ ĐTĐ đều đã chứng minh được rằng việc kiểm soát ĐH chặt chẽ sẽ làm giảm
rõ rệt các biến chứng mạch máu nhỏ. Và các nghiên cứu gần đây cũng cho thấy có mối
liên hệ giữa tăng ĐH mạn và bệnh mạch máu lớn. Do đó tình trạng tăng ĐH mạn có lẽ
là vấn đề cốt lõi trong cơ chế bệnh sinh của các biến chứng mạn ĐTĐ. Vì thế trong điều
trị bệnh ĐTĐ, mục tiêu quan trọng hàng đầu là việc kiểm soát ĐH chặt chẽ chũng như
16
HbA1c, đồng thời loại bỏ các yếu tố nguy cơ, tăng cường thể lực đều đặn, duy trì nếp
sống lành mạnh nhằm giảm thiểu tối đa các biến chứng.
TÀI LIỆU THAM KHẢO
1. American Diabetes Association (2003), Report of the expert committee on the diagnosis and classification of
diabetes mellitus”. Diabetes Care, Vol. 26, suppl. 1, pp. S5 – S13
2. Atkinson AM. et al (2000). Type 1 Diabetes. In: Kahn CR. Atlas of Diabetes. Science Press Limited: 45 – 58
3. Brownlee M. et al (2000). Mechanism of Hyperglycemic Damage in Diabetes. In: Kahn CR. Atlas of Diabetes. Science
Press Limited: 121 – 123
4. Cooper M.E (1998). “Pathogenesis, prevention, and treatment of diabetic nephropathy”, The Lancet, Vol. 352, Issue
9123, pp. 213 – 219.
5. Effective Health Care (2000), “Complication of diabetes. Renal disease and promotion of self management”, The
Royal Society of Medecine Press Limited, Vol 6(1), pp. 2 – 5.
6. Mai Thế Trạch (1999). Biến chứng mãn tính của bệnh Đái Tháo Đường. Nội Tiết Học Đại Cương Mai Thế Trạch –
Nguyễn Thy Khuê. NXB TPHCM: trang 507
7. Masharani U. et al (2001). Pancreatic Hormones and Diabetes Mellitus. In: Grenspan FS. Basic and Clinical
Endocrinology. 6th Ed, McGraw – Hill: 634 – 688 – 694.
8. Mogyorosi A. (2001). Diabetic Nephropathy. In: Massry SG Textbook of Nephrology4th Ed, Lippincott Williams
and Wilkins: 874 – 886.
9. Mudaliar SR. et al (2000). Management and Prevention of Diabetic Complications.In: Kahn CR. Atlas of Diabetes.
Science Press Limited: 84 – 87.
10. Nguyễn Thị Thanh Thủy (2000). Khảo Sát Sự Tương Quan Giữa Microalbumin Niệu và Bệnh Lý Võng Mạc Trên
Bệnh Nhân Đái Tháo Đường. Luận án Thạc Sĩ Y Học.
11. Powers AC et al (2001). Diabetes Mellitus. In: Braunwald E. Principles Of Internal Medecine. Harrison’s 15th ed.
McGraw - Hill: 2109 – 2135.
12. Reusch Jane E.B. (2003). “Diabetes, microvascular complications, and cardiovascular complications: what is it about
glucose?” J. Clin. Invest. Vol. 112:7, pp. 986 – 988.
13. Santon R.C (2000), “Diabetes and Kiney” In: Kahn C R. Atlas of diabetes. Science Press Limited, pp. 152 – 160.
14. Trần Thị Tố Quyyên (2000). Tổng Kết Các Biến Chứng Mạn Của Bệnh Đái Tháo Đường Nhập Viện Tại Khoa Nội
Tiết Bệnh Viện Chợ Rẫy Năm 1998. Luận văn Thạc Sĩ Y Học.
15. Unger RH. (1998). Diabetes Mellitus In: Wilson JD. Williams Textbook of Endocrinology.9th Ed, W.B. Sauders
company: 979 – 1023.