Bai 9: Axit nitric
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (235.25 KB, 22 trang )
TẬP THỂ LỚP 11A
7
KÍNH CHÀO QUÍ THẦY
CÔ ĐẾN DỰ GIỜ TIẾT
THAO GIẢNG
TRƯỜNG THPT DƯỠNG ĐIỀM
TRƯỜNG THPT DƯỠNG ĐIỀM
Thao giảng tháng 9
Thao giảng tháng 9
Bài 9: (tiết 13)
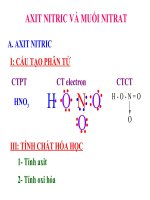
AXIT NITRIC
VÀ MUỐI NITRAT
GV: Nguyễn Minh Trí
Kiểm tra bài cũ
Kiểm tra bài cũ
Hoàn thành sơ đồ phản ứng sau:
Hoàn thành sơ đồ phản ứng sau:
(NH
4
)
2
SO
4
NH
3
NH
4
Cl
N
2
NO
(1)
(2)
(3)
(4)
(5)
Trả lời
Trả lời
(1) (NH
(1) (NH
4
4
)
)
2
2
SO
SO
4
4
+ BaCl
+ BaCl
2
2
2NH
4
Cl + BaSO
4
(2) NH
4
Cl + NaOH
NaCl + NH
3
+ H
2
O
(3) NH
3
+ HCl
NH
4
Cl
(4) 4NH
3
+ 3O
2
2N
2
+ 6H
2
O
(5) N
2
+ O
2
2NO
t
0
t
0
3000
0
C
Bài 9: (tiết 13)
AXIT NITRIC
VÀ MUỐI NITRAT
GV: Nguyễn Minh Trí
Nội dung
Nội dung
A. AXIT NITRIC:
A. AXIT NITRIC:
I. Cấu tạo phân tử.
I. Cấu tạo phân tử.
II. Tính chất vật lí.
II. Tính chất vật lí.
III. Tính chất hoá học.
III. Tính chất hoá học.
IV. Ứng dụng.
IV. Ứng dụng.
V. Điều chế.
V. Điều chế.
B. MUỐI NITRAT:
B. MUỐI NITRAT:
I. Tính chất của muối nitrat.
I. Tính chất của muối nitrat.
II. Ứng dụng.
II. Ứng dụng.
C.
C.
Chu trình của nitơ trong tự nhiên.
Chu trình của nitơ trong tự nhiên.
A. AXIT NITRIC:
A. AXIT NITRIC:
O
O
H O N
H O N
O
O
I. Cấu tạo phân tử:
+5
(HNO
(HNO
3
3
= 63)
= 63)
II. Tính chất vật lí:
II. Tính chất vật lí:
Là chất lỏng, không màu, bốc khói mạnh
Là chất lỏng, không màu, bốc khói mạnh
trong không khí ẩm.
trong không khí ẩm.
Kém bền. Ở nhiệt độ thường:
Kém bền. Ở nhiệt độ thường:
Tan trong nước theo bất kì tỉ lệ nào.
Tan trong nước theo bất kì tỉ lệ nào.
4HNO
3
4NO
2
+ O
2
+ 2H
2
O
Nâu đỏ