Xây dựng quy trình định lượng các acid amin không thay thế trong nước mắm bằng phương pháp sắc ký lỏng ghép khối phổ hai lần (lc
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (6.28 MB, 136 trang )
TR
I H C QU C GIA TP. HCM
NG
I H C BÁCH KHOA
--------------------
TR N
I NGH A
XÂY D NG QUY TRÌNH NH L
NG
CÁC ACID AMIN KHÔNG THAY TH
TRONG N
CM M
B NG PH
NG PHÁP S C KÝ L NG
GHÉP KH I PH HAI L N (LC/MS/MS)
Chuyên ngành : Công ngh th c ph m và
Mã ngành
: 605402
LU N V N TH C S
TP. H CHÍ MINH, tháng 08 n m 2011
u ng
CƠNG TRÌNH
C HỒN THÀNH T I
TR
NG
I H C BÁCH KHOA – HQG -HCM
Cán b h
ng d n khoa h c: PGS.TS. Võ Th B ch Hu
Ch ký: ....................................................................
Cán b ch m nh n xét 1: PGS.TS. Ngô M nh Th ng
Ch ký: ....................................................................
Cán b ch m nh n xét 2: TS. Phan Ng c Hòa
Ch ký: ....................................................................
Lu n v n th c s
c b o v t i Tr
ng
i h c Bách Khoa, HQG Tp.
HCM ngày 09 tháng 08 n m 2011
Thành ph n H i
1. PGS.TS.
ng ánh giá lu n v n th c s g m:
ng Th Anh ào (Ch t ch h i
ng)
2. PGS.TS. Ngô M nh Th ng ( y viên)
3. TS. Phan Ng c Hòa ( y Viên)
4. PGS.TS. Võ Th B ch Hu ( y viên)
5. TS. Ngô Thanh An (Th ký)
Xác nh n c a Ch t ch H i
ng ánh giá LV và Tr
chuyên ngành sau khi lu n v n ã
CH T CH H I
NG
ng Khoa qu n lý
c s a ch a (n u có)
TR
NG KHOA…………
C NG HÒA XÃ H I CH NGH A VI T
NAM c l p - T do - H nh phúc
I H C QU C GIA TP.HCM
NG
I H C BÁCH KHOA
TR
NHI M V LU N V N TH C S
H tên h c viên: TR N
I NGH A
MSHV: 10110189
Ngày, tháng, n m sinh: 30/11/1985
N i sinh: Tp. H Chí Minh
Chuyên ngành: Công ngh th c ph m và
u ng
Mã s :
TÀI: Xây d ng quy trình nh l ng các acid amin không thay th
TÊN
trong n c m m b ng ph ng pháp s c ký l ng ghép kh i ph! hai l"n
(LC/MS/MS)
I. NHI M V VÀ N I DUNG:
-
Kh o sát các quy trình tách chi t các acid amin không thay th trong n
m m
-
Kh o sát các i u ki n phân tách b ng s c ký l ng
-
Kh o sát các thông s trên
-
Xây d ng quy trình
ng d ng quy trình
nh l
c
u dị kh i ph hai l n
ng t các thơng s kh o sát.
c xây d ng trên m u n
c m m Nam Ng
II. NGÀY GIAO NHI M V : 02/ 2011
III. NGÀY HOÀN THÀNH NHI M V : 07/2011
CÁN B
H #NG D$N : PGS.TS. Võ Th B ch Hu
Tp. HCM, ngày . . . . tháng .. . . n m 20....
CÁN B H #NG D$N
(H tên và ch ký)
CH NHI M B MÔN ÀO T O
(H tên và ch ký)
TR %NG KHOA….………
(H tên và ch ký)
L I CAM OAN
Tôi xin cam oan lu n v n là k t qu nghiên c u c a riêng tôi, không
sao chép c a ai. N i dung lu n v n có tham kh o và s d ng các tài li u, thông
tin
c
ng t i trên các tác ph m, t p chí và các trang web theo danh m c
tài li u c a lu n v n.
Tác gi lu n v n
Tr n
i Ngh a
L IC M
N
Em xin chân thành c m n cô Võ Th B ch Hu
truy n
ã t n tình h
ng d n và
t nh ng ki n th c và kinh nghi m quý báu cho em trong su t th i gian em
th c hi n lu n v n này.
Em xin bày t lòng bi t n
n các v lãnh
o và các anh ch
tai Vi n V Sinh Y T Cơng C ng Tp. H Chí Minh ã giúp
ng nghi p
và t o m i i u
ki n thu n l i cho em trong quá trình th c hi n lu n v n.
Cu i cùng, em c ng xin chân thành cám n các th y cô, b n bè trong b môn
Công ngh th c ph m và khoa Cơng ngh hóa h c c a tr
Tp.H Chí Minh ã giúp
h c t p t i tr
ng.
,
ng
i h c Bách Khoa
ng vi n, t o i u ki n cho tôi trong su t th i gian
TÓM T T LU N V N
Hi n nay, vi c
nh l
ng các acid amin b ng ph
kh i ph hai l n (LC/MS/MS) ang
u i m là
nh y cao,
ng pháp s c ký l ng ghép
c nghiên c u và ng d ng nhi u vì có các
l p l i t t, phân tích
c nhi u n n m u, các acid amin
không c n ph i t o d n xu t nên th i gian phân tích c ng
c rút ng n.
Nghiên c u này kh o sát các quy trình làm s ch, tách chi t 9 acid amin
không thay th trong n n m u n
c m m k t h p v i kh o sát các i u ki n s c ký
tách các acid amin này trên c t phân tách và cu i cùng kh o sát các thông s c a
máy kh i ph
nh l
ng. Các thơng s thích h p
cm m
phân tích nh sau:
-
M un
c làm s ch b ng methanol, b t C18, và than ho t tính.
-
Vi c phân tách các acid amin trên c t s c ký Primesep 100
theo 2 c ch : lo i tr ion và trao
T Acetonitrile – n
Acetonitrile – n
i ion v i ch
c th c hi n
ng trình gradient n ng
c c t (30:70) b sung TFA 0,05% (pha
c c t (30:70) b sung TFA 0,3% (pha
:
ng A)
n
ng B) trong th i
gian 30 phút.
-
Vi c
nh l
ng các acid amin
c th c hi n b ng
(MS/MS) AB Sciex Triple Quad 5500
ch
u dò kh i ph 2 l n
Multiple reaction monitoring
(MRM) – Electrospray ionization (ESI) positive (+).
Khi ti n hành th m
nh quy trình
nh l
ng các acid amin, k t qu thu
c nh sau:
Kho ng tuy n tính: 0,5 cho
n 250 µmol/L
Gi i h n phát hi n t 0,0167 - 0,03 µmol/g, gi i h n
nh l
ng t 0,05
n
0,1 µmol/g.
! chính xác và
Hi u su t thu h i
! khơng
úng d
i 20%.
u trên 85% ngo i tr Lysine là 80%
m b o o t 8 – 13 % ngo i tr Lysine là 20%
Lu"n v#n này ã xây d ng th m
các acid amin không thay th trong n
kh i ph hai l n.
nh và
ngh
c m m b ng ph
c m t quy trình
nh l
ng
ng pháp s c ký l ng ghép
ABSTRACT OF THESIS
Nowadays, amino acids quantification performed by liquid chromatography
– tandem mass spectrometry (LC/MS/MS) has widely been used because of many
advantages: low limit of detection, good repeatability, analysing many kinds of
matrices, reducing analysis time when performing without amino acids
derivatization.
This research focused on the purification and extraction of 9 essential amino
acids from fish sauce, the separation on chromatography column and the
quantification on tandem mass spectrometry. The suitable technological parameters
of the amino acids quantification were as follows:
The amino acids from fish sauce were extracted and purified by methanol,
C18 powder and activated carbon.
Separation was achieved on Primesep 100 column using 2 mechanisms: ion –
exclusion and ion – exchange with the concentration gradients program:
From trifluoroacetic acid 0,05% in acetonitrile – water (30:70) (mobile phase
A) to trifluoroacetic acid 0,3% in acetonitrile – water (30:70) (mobile phase
B) in 30 minutes.
Quantification was acquired by tandem mass spectrometry (MS/MS) AB
Sciex Triple Quad 5500 using electrospray ionization (ESI) in the MRM scan
type, positive mode.
After performed method validation, the results were presented as follows:
Calibration curves were linear over the range 0,5 – 250 µmol/L.
Limit of detections of each amino acids were 0,0167 - 0,03 µmol/g, limit of
quantifications of each amino acid were 0,05 - 0,1 µmol/g
Relative standard deviations of repeatability and accuracy were below 20%.
Recoveries of almost amino acids were above 85% (except 80% for Lysine)
Uncertainties of almost amino acids were 8 – 13% (except 20% for Lysine)
The thesis accomplished a method validation and proposed a quantification
method for essential amino acids from fish sauce performed by liquid
chromatography - tandem mass spectrometry.
Các thu t ng và ch vi t t t
-
A (Accuracy):
úng
-
CE (Collision Energy): N ng l
-
CV (Coefficient of Variation): H s bi n
-
DP (Declusion potential): Th t o ion
-
ESI (Electrospray ionization): S ion hóa b ng
-
ILOD ( Instrument limit of detection): Gi i h n phát hi n c a thi t b
-
ILOQ ( Instrument limit of quantification): Gi i h n
-
LC/MS/MS (Liquid chromatography with tandem mass spectrometry): ph
ng phân m nh ion
ng
u phun electron
nh l
ng c a thi t b
ng
pháp s c ký l ng ghép kh i ph 2 l n
-
MLOD (Method limit of detection): Gi i h n phát hi n c a ph
-
MLOQ (Method limit of quantification): Gi i h n
-
MRM (multiple reaction monitoring): M t ch
nh l
ng pháp
ng c a ph
ch y
nh l
ng pháp
ng c a máy
kh i ph 2 l n
-
r (Repeatability):
l pl i
-
Rw (within – laboratory Reproducibility):
-
R (Reproducibility):
-
RSD (Relative Standard deviation):
-
SCX (Strong cation exchange): k thu t trao
-
SD (Standard deviation):
-
SPE (Solid phase extraction): k thu t tách chi t pha r n
-
TFA: Trifluoroacetic acid
-
U (Uncertainty):
-
Ubias ( Bias Uncertainty):
-
URw (Within – laboratory Uncertainty):
tái l p n i b phịng thí nghi m
tái l p
khơng
l ch chu n t
ng
i ion d
i
ng m nh
l ch chu n
mb o o
không
m b o o theo
không
l ch (hi u su t thu h i)
m b o o theo
n i b phịng thí nghi m
-
WCX (Weak cation exchange): k thu t trao
i ion d
ng y u
tái l p
1
LU N V N TH C S
M cl c
1. Ph n m
u ..................................................................................................... 6
2. T ng quan.......................................................................................................... 7
2.1. T ng quan v n c m m...............................................................................7
2.1.1. Gi i thi u v n c m m .........................................................................7
2.1.2. Thành ph n c a n c m m .....................................................................7
2.1.3. Các h enzym trong s n xu t n c m m.................................................8
2.1.4. Quy trình s n xu t n c m m .................................................................8
2.1.5. Các y u t nh h ng n quá trình ch bi n n c m m ........................9
2.1.5.1. nh h ng c a nhi t ...................................................................9
2.1.5.2. nh h ng c a mu i........................................................................9
2.1.5.3. nh h ng c a nguyên li u............................................................10
2.1.5.4. nh h ng c a di n tích ti p xúc ...................................................10
2.1.5.5. nh h ng c a ph ng pháp p mu i .........................................11
2.1.6. Tiêu chu n ánh giá ch t l ng n c m m...........................................11
2.2. T ng quan v acid amin .............................................................................12
2.2.1. Gi i thi u chung v acid amin ..............................................................12
2.2.2. Phân lo i các acid amin ........................................................................12
2.2.3. Các tính ch t chung c a các acid amin..................................................16
2.2.3.1. Tính tan..........................................................................................16
2.2.3.2. Tính phân c c ................................................................................16
2.2.3.3. Tính quang ho t .............................................................................17
2.2.3.3. Vai trò c a các acid amin ...............................................................17
2.3. T ng quan v các ph ng pháp phân tích acid amin....................................17
2.3.1. Ph ng pháp s c ký gi y .....................................................................17
2.3.2. Ph ng pháp s c ký b n m ng .............................................................18
2.3.3. Ph ng pháp s c ký khí (GC) ..............................................................18
2.3.4. Ph ng pháp s c ký l ng hi u n ng cao (HPLC) ..................................18
3. M c tiêu nghiên c u ........................................................................................ 20
4. Nguyên li u và ph ng pháp nghiên c u ......................................................... 21
4.1. Nguyên li u.................................................................................................21
4.1.1. Ch t chu n............................................................................................21
4.1.2. i t ng nghiên c u ...........................................................................21
4.2. D ng c , trang thi t b , hóa ch t..................................................................22
4.2.1. D ng c ................................................................................................22
4.2.2. Trang thi t b ........................................................................................23
4.2.3. Hóa ch t ...............................................................................................24
4.3. N i dung nghiên c u ...................................................................................25
4.3.1. Kh o sát các thông s kh i ph .............................................................27
4.3.1.1. Các thông s c
nh ......................................................................27
4.3.1.2. Các thông s kh o sát.....................................................................28
4.3.1.3. Cách th c th c hi n........................................................................28
Ng
i th c hi n: TR N
I NGH A
2
LU N V N TH C S
4.3.2. Kh o sát các thông s s c ký ................................................................29
4.3.2.1. Các thông s c
nh ......................................................................29
4.3.2.2. Các thông s kh o sát.....................................................................29
4.3.3. Kh o sát các quy trình chi t acid amin trong n c m m .......................32
4.3.4. Th m nh quy trình nh l ng b ng các ph ng pháp th ng kê ........37
4.3.4.1. Kho ng tuy n tính (Linear range)...................................................37
4.3.4.2. Gi i h n phát hi n và gi i h n c a ph ng pháp (MLOD, MLOQ) 37
4.3.4.3.
chính xác (Precision) ................................................................37
4.3.4.4.
úng (Accuracy) .......................................................................39
4.3.4.5.
không m b o o U (Uncertainty)...........................................40
5. K t qu và bàn lu n.......................................................................................... 42
5.1. Kh o sát các thông s kh i ph ...................................................................42
5.2. Kh o sát c a các thông s s c ký.................................................................43
5.3. Kh o sát các quy trình chi t acid amin trong n c m m..............................46
5.3.1. Kh o sát quy trình 1..............................................................................46
5.3.2. Kh o sát quy trình 2..............................................................................47
5.3.3. Kh o sát quy trình 3..............................................................................48
5.3.4. Kh o sát quy trình 4..............................................................................49
5.4. Th m nh quy trình nh l ng..................................................................50
5.4.1. Kho ng tuy n tính ................................................................................50
5.4.2. Xác nh gi i h n phát hi n và gi i h n nh l ng c a ph ng pháp ..53
5.4.3. Xác nh
chính xác ..........................................................................57
5.4.3.1. Xác nh
l p l i .........................................................................57
5.4.3.2. Xác nh
tái l p n i b phịng thí nghi m ..................................59
5.4.3. Xác nh
úng..................................................................................62
5.4.4. Xác nh
khơng m b o o.............................................................71
5.5. Xây d ng quy trình nh l ng ...................................................................72
5.5.1. Quy trình x lý m u n c m m ............................................................72
5.5.2. Quy trình ch y máy LC/MS/MS ...........................................................72
5.5.2.1. Các thông s s c ký........................................................................72
5.5.2.2. Các thông s kh i ph ....................................................................73
5.6. Áp d ng quy trình nh l ng các acid amin trong n c m m ....................75
6. K t lu n ........................................................................................................... 76
7. Ki n ngh ......................................................................................................... 78
8. Tài li u tham kh o ........................................................................................... 79
Ng
i th c hi n: TR N
I NGH A
3
Danh m c hình
LU N V N TH C S
Hình 4.1: M u n c m m Nam Ng ..................................................................22
Hình 4.2: B cơ quay chân khơng Buchi R- 210.................................................23
Hình 4.3: B chi t SPE Vacumn Manifold c a Supelco ....................................23
Hình 4.4: H th ng máy s c ký l ng hi u n ng cao Shimadzu..........................24
Hình 4.5: u dị kh i ph 2 l n AB Sciex Triple Quad 5500 ...........................24
Hình 4.6: Các giai o n ti n hành kh o sát vi c phân tích các acid amin trong
n c m m ............................................................................................................26
Hình 4.7 : Quy trình [1] tách các acid amin trong n c m m .........................33
Hình 4.8 : Quy trình [2] tách các acid amin trong n c m m .........................34
Hình 4.9 : Quy trình [3] tách các acid amin trong n c m m .........................35
Hình 4.10 : Quy trình [4] tách các acid amin trong n c m m........................36
Hình 5.1: C t Primesep 100 khi pH >1.00......................................................45
Hình 5.2: C t Primesep 100 khi pH <1.00......................................................46
Hình 5.3:
th bi u di n
ng chu n c a Threonine n ng
t 0,5 - 250
µmol/L ..................................................................................................................50
Hình 5.4:
th bi u di n
ng chu n c a Valine n ng
t 0,5 - 250
µmol/L ..................................................................................................................50
Hình 5.5:
th bi u di n
ng chu n c a Methionine n ng
t 0,5 - 250
µmol/L ..................................................................................................................51
Hình 5.6:
th bi u di n
ng chu n c a Leucine n ng
t 0,5 - 250
µmol/L ..................................................................................................................51
Hình 5.7:
th bi u di n
ng chu n c a Isoleucine n ng
t 0,5 - 250
µmol/L .................................................................................................................51
Hình 5.8:
th bi u di n
ng chu n c a Phenylalanine n ng
t 0,5 250 µmol/L ...........................................................................................................52
Hình 5.9:
th bi u di n
ng chu n c a Histidine n ng
t 0,5 - 250
µmol/L ..................................................................................................................52
Hình 5.10:
th bi u di n
ng chu n c a Lysine n ng
t 0,5 - 250
µmol/L ..................................................................................................................52
Hình 5.11:
th bi u di n
ng chu n c a Arginine n ng
t 0,5 - 250
µmol/L ..................................................................................................................53
Ng
i th c hi n: TR N
I NGH A
4
LU N V N TH C S
Danh m c b ng
B ng 1.1: !nh h ng c a các ph "ng pháp p mu i n t c
p mu i theo th i
gian ...................................................................................................................................... 11
B ng 1.2: Các Acid amin monoamino_monocacboxylic ................................................ 12
B ng 1.3: Các acid amin monoamino_dicacboxylic ....................................................... 13
B ng 1.4: Các acid amin diamino_monocacboxylic ....................................................... 13
B ng 1.5: Các acid amin ch#a Sulfur ............................................................................. 14
B ng 1.6: Các acid amin vòng th"m ................................................................................ 14
B ng 1.7: Các acid amin d vòng ...................................................................................... 15
B ng 1.8: Các amit c a acid amin .................................................................................... 15
B ng 1.9: Tính tan S(g/L) c a các acid amin trong n c 25oC ................................. 16
B ng 4.1: H$n h%p chu n g c c a các acid amin và n ng
t ng acid amin trong h$n
h%p....................................................................................................................................... 21
B ng 4.2: Các dung mơi, hóa ch&t s' d ng trong bài nghiên c#u................................. 24
B ng 4.3: Các thông s v( ph kh i l %ng ...................................................................... 27
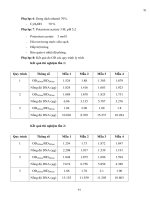
B ng 4.4: Ch "ng trình gradient n ng
th# 1............................................................. 29
B ng 4.5: Ch "ng trình gradient n ng
th# 2............................................................. 30
B ng 4.6: Ch "ng trình gradient n ng
th# 3............................................................. 31
B ng 5.1: Th t o ion chính (DP) và các n ng l %ng phân m nh ion (CE) c a các acid
amin..................................................................................................................................... 42
B ng 5.2: N ng
và di n tích peak t "ng #ng c a Threonine ................................... 50
B ng 5.3: N ng
và di n tích peak t "ng #ng c a Valine .......................................... 50
B ng 5.4: N ng
và di n tích peak t "ng #ng c a Methionine ................................. 51
B ng 5.5: N ng
và di n tích peak t "ng #ng c a Leucine ....................................... 51
B ng 5.6: N ng
và di n tích peak t "ng #ng c a Isoleucine.................................... 51
B ng 5.9: N ng
và di n tích peak t "ng #ng c a Phenylalanine............................. 52
B ng 5.10: N ng
và di n tích peak t "ng #ng c a Histidine.................................... 52
B ng 5.11: N ng
và di n tích peak t "ng #ng c a Lysine........................................ 52
B ng 5.12: N ng
và di n tích peak t "ng #ng c a Arginine .................................... 53
B ng 5.13: tín hi u (S/N) c a Threonine c a 8 m u tr ng thêm chu n (1 µmol/L) .... 54
B ng 5.14: tín hi u (S/N) c a Valine c a 8 m u tr ng thêm chu n .............................. 54
(1 µmol/L) ........................................................................................................................... 54
B ng 5.15: tín hi u (S/N) c a Methionine c a 8 m u tr ng thêm chu n (1 µmol/L)... 54
B ng 5.16: tín hi u (S/N) c a Leucine c a 8 m u tr ng thêm chu n (0,5 µmol/L)...... 55
B ng 5.17: tín hi u (S/N) c a Isoleucine c a 8 m u tr ng thêm chu n (0,5 µmol/L) .. 55
B ng 5.18: tín hi u (S/N) c a Phenylalanine c a 8 m u tr ng thêm chu n (0,5
µmol/L)................................................................................................................................ 55
B ng 5.19: tín hi u (S/N) c a Histidine c a 8 m u tr ng thêm chu n (1 µmol/L)....... 56
B ng 5.20: tín hi u (S/N) c a Lysine c a 8 m u tr ng thêm chu n .............................. 56
(1 µmol/L) ........................................................................................................................... 56
B ng 5.21: tín hi u (S/N) c a Arginine c a 8 m u tr ng thêm chu n (1 µmol/L) ....... 56
B ng 5.22: Kh o sát
l)p l i c a 3 m u n c m m không thêm chu n trong cùng
ngày phân tích .................................................................................................................... 57
B ng 5.23: Kh o sát
l)p l i c a 6 m u n c m m thêm chu n n ng
thêm vào
5 µmol/g trong cùng ngày phân tích................................................................................. 58
Ng
i th c hi n: TR N
I NGH A
5
LU N V N TH C S
B ng 5.24: Kh o sát
l)p l i c a 3 m u n c m m khơng thêm chu n trong ngày
phân tích khác .................................................................................................................... 59
B ng 5.25: Kh o sát
tái l)p n i b phịng thí nghi m c a 6 m u n c m m không
thêm chu n trong 2 ngày phân tích khác nhau............................................................... 60
B ng 5.26 : Kh o sát
l)p l i c a 6 m u n c m m thêm chu n n ng
thêm vào
5 µmol/g trong ngày phân tích khác................................................................................. 60
B ng 5.27: Kh o sát
tái l)p n i b phịng thí nghi m c a 12 m u n c m m thêm
chu n n ng
thêm vào 5 µmol/g trong 2 ngày phân tích khác nhau ...................... 61
B ng 5.28: Kh o sát
úng c a Threonine .................................................................. 62
B ng 5.29: Kh o sát
úng c a Valine ......................................................................... 63
B ng 5.30: Kh o sát
úng c a Methionine................................................................ 64
B ng 5.31: Kh o sát
úng c a Leucine....................................................................... 65
B ng 5.32: Kh o sát
úng c a Isoleucine ................................................................... 66
B ng 5.33: Kh o sát
úng c a Phenylalanine........................................................... 67
B ng 5.34: Kh o sát
úng c a Histidine..................................................................... 68
B ng 5.35: Kh o sát
úng c a Lysine......................................................................... 69
B ng 5.36: Kh o sát
úng c a Arginine ..................................................................... 70
B ng 5.37:
khơng m b o o theo
tái l)p phịng thí nghi m,
không m
b o o theo
l ch bias,
không m b o o toàn ph n ........................................... 71
B ng 5.38: Ch "ng trình gradient n ng
.................................................................... 73
B ng 5.39: DP và CE c a các acid amin .......................................................................... 74
B ng 5.40: Giá tr các acid amin trong m u n c m m Nam Ng ............................... 75
s
ng ký 6007 570517 .................................................................................................... 75
Ng
i th c hi n: TR N
I NGH A
6
1. Ph n m
N
LU N V N TH C S
u
c m m là m t lo i gia v và n
rãi trong m th c c a các n
c
c ch m quen thu c,
c s d ng r ng
Châu Á. ! Vi t Nam, n
c m m th "ng có
trong b#a n hàng ngày c a h u h t m$i gia ình.
Tu% theo t&ng vùng khác nhau, n
h
ng v
c m m s'
c ch bi n và mang nh#ng
c tr ng riêng cho t&ng vùng mi n. Nh
c ch bi n t& cá c m, t i Phan Thi t thì n
n c ho c t i (ng b ng sơng C u Long thì n
n
c m m cịn
m m n i ti ng
Trong n
cm m
c làm t& con cà cu ng. M t s
cm m
c ch bi n t& cá
c m m t& cá linh,
m t s thì
a danh s n xu t n
c
Vi t Nam nh : Phú Qu c, Phan Thi t, Nha Trang…
c m m thành ph n ch y u và quy t
dinh d )ng
Phú Qu c, n
ó chính là các acid amin nh
nh
n ch t l
ng. giá tr
Lysine, Valine, Glutamic,
Arginine, Methionine, Tyrosine, PhenylAlanine, Threonine, Leucine,
IsoLeucine…
Hi n nay * ánh giá ch t l
ng và giá thành c a n
ki*m nghi m v n ang d a vào tiêu chu n xác
m m b ng ph
nh
ng pháp Kjeldahl r(i quy ra hàm l
pháp này có khuy t i*m là không th* phân bi t
ch a
m dinh d )ng và các h p ch t ch a
c m m, các trung tâm
ng
m t ng c a n
c
m amin. Ph
ng
c các lo i h p ch t có
m khơng dinh d )ng. M t s
c s s n xu t ã l i d ng vào tiêu chu n trên, làm t ng
thêm urê vào n
nh#ng nh h
Tr
c m m * làm gi m giá thành s n xu t, i u ó gây ra
ng nghiêm tr$ng
n s c kh e ng "i tiêu dùng.
c th c tr ng trên, chúng tôi th c hi n
Xây d ng
m b ng cách
c ph
ng pháp xác
tài này nh m:
nh acid amin trong n
th* là nhóm acid amin khơng thay th - b ng ph
cm m-c
ng pháp s c ký l ng
ghép kh i ph 2 l n (LC/MS/MS)
Làm c s
* xác
nh ch t l
amin.
Ng
i th c hi n: TR N
I NGH A
ng n
c m m b ng các ch+ tiêu v acid
7
LU N V N TH C S
2. T ng quan
2.1. T ng quan v( n
c m m [1], [8], [9], [10], [16], [21]
2.1.1. Gi i thi u v( n
N
cm m
c m m là h,n h p mu i các acid amin
c th y phân t& protein trong th t
cá v i tác nhân là h enzyme có s-n trong n i t ng cá cùng v i m t s vi khu n
k. khí.
T i Vi t Nam, các vùng mi n bi*n nh Phú Qu c, Phan Thi t, Nha Trang
làm n
c m m. Tu% theo
m m thành các c p
h ng (350
m trong n
:n
m), h ng 1(300
m), h ng 2 (250
2.1.2. Thành ph n c a n
- Các ch t
c m m mà ng "i ta phân lo i n
c bi t (kho ng 400
cm m
u có
m), n
c m m th
i 200
m), h ng 3 (d
c
ng
m).
cm m
m: chi m ch y u và là thành ph n quy t
nh giá tr c a n
c
m t ng: Là t ng s Nit có trong n
c m m (g/L), dùng * phân h ng n
c
m amin: Là t ng l
i d ng acid amin (g/L), quy t
m m.
Các ch t
+
m
c phân thành 3 lo i:
m m
+
tr n
+
ng
mn md
cm m
m amoni: L
càng kém ch t l
Ngồi các ch t
ng
m này có trong n
c m m càng nhi u thì n
cm m
ng.
m trên, trong n
dipeptide, tripeptide, peptone..
n
nh giá
c m m d/ b h h ng do ho t
c m m cịn có các lo i
m khác nh
ây là nh#ng thành ph n trung gian làm cho
ng c a vi sinh v t.
Các h p ch t bay h i: g(m nhi u nhóm và quy t
nh
nh
ng v n
m m
Hàm l
ng m t s ch t bay h i có trong n
c m m (mg/100g n
c m m):
+ Các h p ch t carbonyl bay h i: 407 – 512 (Ví d : Formaldehyde)
+ Các acid bay h i: 404 – 533 ( acid propionic)
Ng
i th c hi n: TR N
I NGH A
c
8
LU N V N TH C S
+ Các amin bay h i: 9,5 - 11,3 (isopropylamine)
Các ch t vô c : NaCl chi m nhi u nh t (250 – 280 g/L) và m t s ch t
khoáng khác nh
Ca; Mg; S; P; I.
Các vitamin: B1; B2; B12; PP
2.1.3. Các h enzym trong s n xu&t n
cm m
G(m 3 h l n:
H Metalo-protease ( hay còn g$i là Aminodipeptidase):
H enzyme này có trong n i t ng cá, ch u
m nh trong th"i gian
u lên men n
c n(ng
c m m, gi m d n
mu i cao, ho t
ng
tháng th 3 v sau. H
enzyme có ho t tính m nh, có kh n ng th y phân r ng rãi
i v i các nhóm
peptide khác nhau. Nhóm enzyme này là nhóm enzyme trung tính, pHopt = 5-7,
pI = 4-5, n
nh v i ion Ca2+ và Mg2+ và m t ho t tính khi có các ion Zn2+,
Pb2+, Hg2+.
H enzyme serine – protease:
i*n hình là enzyme trypsine, có nhi u trong n i t ng cá. ! giai o n
enzyme này ho t
ng y u, t i tháng th 2 ho t
tháng th 3 b t
u gi m d n khi protein trong n
hoàn toàn. H enzyme này ho t
ng
ng m nh t i c c
u, h
i, và t i
c m m phân gi i g n nh
pH = 5-10, pHopr = 9
H enzyme acid – protease:
Có trong n i t ng cá. H enzyme này d/ b
15% nên ch+ ho t
ng trong th"i gian
c ch b i n(ng
u c a quá trình th y phân. H này ch+
óng vai trị th y u trong quá trình s n xu t n
2.1.4. Quy trình s n xu&t n
Quá trình s n xu t n
Ng
i th c hi n: TR N
cm m
c m m g(m 2 giai o n:
I NGH A
mu i kho ng
c m m.
9
LU N V N TH C S
Giai o n thu0 phân protein nh" enzyme protease, quá trình này x y ra càng
tri t * thì ch t l
ng n
c m m càng ngon,
m càng cao.
Protein → acid amin, peptid
Giai o n t o h
ng th m: giai o n này n
c m m ã “ng u” (chín), t o mùi v
c tr ng do s t o thành c a các acid h#u c nh acid formic, acid acetic, acid
propionic, acid butylic (ng phân t o ra b i vi khu n Pediococcus halophilus
trong q trình lên men. Ngồi ra, nh#ng nghiên c u v n
nhân quan tr$ng trong vi c hình thành mùi th m
c m m cho th y tác
c tr ng c a n
vi khu n y m khí. N m 1930 Boer và Guillerm ã tách
c m m là các
c t& n
cm mm t
lo i vi khu n k. khí sinh nha bào là Clostridium, em c y vào môi tr "ng th chpepton s' sinh ra mùi c a n
c m m.
2.1.5. Các y u t
2.1.5.1. !nh h
Th"i gian
nh h
ng
n quá trình ch bi n n
ng c a nhi t
p mu i gi m khi nhi t
c a dung d ch hay c a cá khi
c a cá
c nâng cao, khi nâng nhi t
p mu i ph i th n tr$ng, vì quá trình ng m
mu i c a cá luôn ch m h n quá trình lên men phân gi i.
l n, nhi u m)
7oC.
d
i da và v y dày thì nhi t
i v i cá nh có th* mu i
nhi t
p mu i là 5 –
cao h n vì quá trình ng m mu i
thích h p là 37 – 50oC.
ng c a mu i
Thành ph n hố h$c và kích th
L
i v i cá có chi u dày
thích h p khi
nhanh h n s phá ho i c a vi sinh v t và th "ng nhi t
2.1.5.2. !nh h
cm m
c c a mu i:
ng mu i Ca, Mg trong mu i n cao làm c n tr NaCl ng m vào cá vì
chúng làm khơ b m t cá, protid b
th "ng dùng mu i tinh khi t, có
N(ng
ơng
t l i. Vì th , khi
p mu i ng "i ta
r n cao, khơng vón c c
mu i:
NaCl là mu i trung tính, n u l
ng mu i cho vào
t
n
bão hịa (358g/l
20oC) s m thì protein trong c th* cá khó hịa tan mà ngay c nh#ng protein
tan trong dung d ch c1ng có th* b t a. Nh v y l
Ng
i th c hi n: TR N
I NGH A
ng
m t ng c ng trong
10
ph n n
c ch
p s' b gi m. N u n(ng
kích thích thúc
ch
LU N V N TH C S
mu i lỗng thì có tác d ng nh ch t
y tác d ng c a enzym làm cho protein b th y phân nhanh h n,
p s' mau chín h n. N u n(ng
mu i
m
c thì nó s' làm tê li t ho t
ng c a vi sinh v t vì t bào vi sinh v t s' b m t n
cd n
n hi n t
ng co
nguyên sinh ch t, protein trong cá b t a. Vì th , * quá trình ch bi n ch
p
c nhanh chóng thơng th "ng ng "i ta cho vào 22 – 25% (mu i tinh khi t),
xác
nh s l n, t+ l , th"i gian cho vào bao lâu là thích h p nh t.
2.1.5.3. !nh h
ng c a nguyên li u
Các lo i cá khác nhau có thành ph n c u trúc hóa h$c khác nhau,
là h vi sinh v t t(n t i trong cá c1ng khác nhau. Cá t
c bi t
i, giá tr kinh t cao h n
là nguyên li u t t nh t cho quá trình ch bi n n
c m m. Nh#ng lồi cá nào có
thành ph n protein cao, n
c m m có l
c ít thì ch bi n ra n
ng
m cao.
Nh#ng lồi cá nào có c u trúc th t l ng l2o, c th t m m, m ng mình, ít
v y d/ ch bi n h n, ch
h p ch bi n n
cho n
p mau chín h n. Cá có nhi u m) c1ng khơng thích
c m m, khi ch bi n ch
p m) n i lên trên d/ b oxy hóa làm
c m m có mùi ơi khét khó ch u và m t ph n m) b th y phân sinh ra các
acid y u bay h i làm cho n
c m m có v chua.
Tùy thu c vào khu v c s ng c a cá, các lo i cá s ng
t ng n
l
c gi#a nh : cá c m, n c, thu, trích… ch bi n n
ng cao nh t. Cá s ng
t ng áy ch t l
ng n
t ng n
c trên và
c m m cho ch t
c m m khơng t t l m vì
chúng n bùn, rong rêu.
2.1.5.4. !nh h
ng c a di n tích ti p xúc
* t o i u ki n t t cho vi sinh v t ho t
ch bi n n
vi sinh v t
c m m, thì ta ph i xay nh ,
c phân b
ng c1ng nh rút ng n th"i gian
p d p, c t khúc, ánh khu y… khi ó
u ra tồn b kh i ch
p.
Cá xay nh thì di n tích ti p xúc l n nh t nh ng protein d/ b bi n tính
nhi u nh t m c dù vi sinh v t phát tri*n t t. Trong quá trình kéo rút d/ b t c.
Ng
i th c hi n: TR N
I NGH A
11
Cá
p d p v n gi#
LU N V N TH C S
c hình d ng nguyên con và c th t m m ra, t bào
b v) màng, nguyên sinh ch t ng m ra t o i u ki n cho vi sinh v t phát tri*n.
3u i*m không gây hi n t
ng t c.
Nói chung trong các bi n pháp c h$c trên thì cá
p d p có u i*m h n
c , vì v y * t ng di n tích ti p xúc, rút ng n th"i gian ch bi n ta nên s d ng
ph
ng pháp
p d p cá.
2.1.5.5. !nh h
ng c a ph "ng pháp
Nhìn chung thì t c
p mu i c a ph
h,n h p bé h n m t ít so v i t c
p mu i khô và
t
p mu i trong dung d ch, nh ng n u
p
mu i trong dung d ch tu n hồn thì t c
minh
p mu i
ng pháp
l i nhanh n#a. Ng "i ta ã ch ng
c r ng mu i trong dung d ch tu n hoàn th"i gian gi m i 1,3 l n so v i
p mu i khô, gi m i 1,8 l n so v i
hoàn. Sau ây là b ng * th y
B ng 1.1: !nh h
p mu i trong dung d ch không tu n
ct c
p mu i c a các ph
ng c a các ph "ng pháp
p mu i
ng pháp :
nt c
p mu i
theo th i gian
Ph
ng pháp
p mu i
3 p mu i khô
N(ng
mu i
trong cá
(g/L)
3 p mu i h,n
h p
3 p mu i tu n
hoàn
Th"i gian
p mu i (gi")
2
4
6
8
10
8.71
11.65
12.91
15.9
16.16
9.38
12.37
14.44
16.41
17.21
10.89
12.71
14.98
16.66
17.40
2.1.6. Tiêu chu n ánh giá ch&t l %ng n
Hi n nay các nhà s n xu t n
c m m t i Vi n Nam
cm m
u áp d ng tiêu chu n
TCVN 5107:2003 do Ban k4 thu t tiêu chu n c a B Khoa H$c và Công ngh
ban hành. Tiêu chu n này có các quy
Ng
i th c hi n: TR N
I NGH A
nh v hoá h$c nh hàm l
ng nit t ng,
12
hàm l
ng nit amin, hàm l
LU N V N TH C S
ng mu i… Các ch+ tiêu v vi sinh nh t ng s vi
sinh v t hi u khí, s khu n l c E.coli, Coliform…
2.2. T ng quan v( acid amin [3], [8], [9], [10], [16], [21]
2.2.1. Gi i thi u chung v( acid amin
Acid amin là 1 loai h p ch t h#u c có ch a nhóm amino -NH2 và nhóm
cacboxyl –COOH trong phân t .
Tu% theo v trí cu nhóm -NH2 so v i –COOH mà có các α ,β… acid amin.
Các α- acid amin là
n v c s câú t o nên c u trúc cu protein c a c th*
s ng.
Công th c c u t o t ng quát cu α-acid amin là:
COOH
R
CH
NH2
Protein có trên 20 lo i acid amin khác nhau tham gia vào c u trúc c a nó, các acid
amin ch+ khác nhau
ho t
g c R. Các tính ch t lý h$c nh kh n ng tan trong n
ng hóa h$c, kh n ng t o liên k t hidro c a acid amin c1ng ph thu c vào
b n ch t hóa h$c c a g c R ó.
2.2.2. Phân lo i các acid amin
-
D a vào
c tính m ch bên ngồi , ng
ì ta phân chia các acid amin th "ng
g p thành 1 s nhóm chính sau:
• Nhóm 1: Acid amin m ch th ng :
B ng 1.2: Các Acid amin monoamino_monocacboxylic
Tên g$i
Công th c câú t o
Kí hi u vi t t t
Glycine
Alanine
Ng
c,
i th c hi n: TR N
COOH
H2N CH2
COOH
H2N CH CH3
I NGH A
Gly
Ala
13
LU N V N TH C S
COOH
Leucine
H2N CH CH2 CH
COOH
Isoleucine
H2N CH CH
COOH
Valine
H2N CH CH
CH3
Leu
CH3
C2H5
Ile
CH3
CH3
Val
CH3
COOH
Serine
Ser
HC CH2 OH
NH2
COOH
Threonine
HC
Thr
CH CH3
NH2 OH
B ng 1.3: Các acid amin monoamino_dicacboxylic
Tên g$i
Công th c c u t o
Kí ki u vi t t t
COOH
Aspartic acid
Asp
HC CH2 COOH
NH2
COOH
Glutamic acid
Glu
HC CH2 CH2 COOH
NH2
B ng 1.4: Các acid amin diamino_monocacboxylic
Tên g$i
Cơng th c c u t o
COOH
Lysine
HC (CH2)4 NH2
Kí hi u vi t t t
Lys
NH2
COOH
Arginine
Ng
i th c hi n: TR N
HC (CH2)3 N C NH2
NH2
I NGH A
H NH
Arg
14
LU N V N TH C S
B ng 1.5: Các acid amin ch#a Sulfur
Tên g$i
Công th c c u t o
Kí hi u vi t t t
COOH
Cysteine
Cys
HC CH2 SH
NH2
COOH
Cystine
HC CH2 S S
NH2
HOOC
CH2 CH
H2N
COOH
Methionine
Met
HC CH2 S CH3
NH2
• Nhóm 2: Acid amin vòng th m:
B ng 1.6: Các acid amin vòng th"m
Tên g$i
Cơng th c c u t o
Kí hi u vi t t t
COOH
Phenylalanine
Phe
HC CH2
NH2
COOH
Tyrosine
Ng
i th c hi n: TR N
HC CH2
NH2
I NGH A
OH
Tyr
15
LU N V N TH C S
• Nhóm 3: Các acid amin d vòng
B ng 1.7: Các acid amin d vịng
Tên g$i
Cơng th c c u t o
Kí hi u vi t t t
COOH
CH2 CH
Tryptophane
NH2
N
H
N
Histidine
COOH
CH2 CH
HN
His
NH2
HOOC
Proline
Trp
Pro
HN
• Nhóm 4: Amit c a acid amin
B ng 1.8: Các amit c a acid amin
Tên g$i
Cơng th c c u t o
Kí hi u vi t t t
COOH
Asparagine
HC CH2 C NH2
NH2
Asn
O
COOH
Glutamine
HC CH2 CH2 C NH2
NH2
-
Gln
O
Ngồi ra ng "i ta cịn phân lo i các acid amin theo quan i*m dinh d )ng
thành 2 nhóm:
+ Nhóm các acid amin khơng thay th (c th* ng "i không t t ng h p
c):
Valine, Methionine, Lysine, leucine, Isoleucine, Tryptophane, Threonine,
Phenylalanine. Ngoài ra
Ng
i th c hi n: TR N
tr2 em thêm 2 acid amin là: Histidine và Arginine.
I NGH A
16
LU N V N TH C S
+ Nhóm các acid amin có th* thay th : Alanine, Glycine, Glutamic Acid, Aspartic
acid, Tyrosine, Asparagine, Cysteine, Cystine, Serine, Proline.
2.2.3. Các tính ch&t chung c a các acid amin
2.2.3.1. Tính tan
B ng 1.9: Tính tan S(g/L) c a các acid amin trong n
c
25oC
Acid amin
S(g/l)
Acid amin
S(g/l)
Alanine
167,2
Leucine
21,7
Arginine
855,6
Lysine
739,0
Asparagine
28,5
Methionine
56,2
Aspartic acid
5,0
Phenylalanine
27,6
Cysteine
-
Proline
1620,0
Glutamine
7,2(37oC)
Serine
422,0
Glutamic acid
8,5
Threonine
13,2
Glycine
249,9
Tryptophan
13,6
Histidine
-
Tyrosine
0,4
Isoleucine
34,5
Valine
58,1
2.2.3.2. Tính phân c c
- Tính phân c c c a acid amin trung hòa i n n m gi#a tính phân c c c a acid
amin khơng tan trong n
c và tính phân c c c a acid amin mang i n.
- Tính phân c c c a Ser vàThr là do nhóm –OH trong phân t có kh n ng t o liên
k t hidro liên phân t v i n
c.
- Tyr có ch a 1 nhóm –OH phenol có kh n ng ion hóa. Tyr ion hố trong mơi
tr "ng ki m y u, vì th c1ng
kh n ng tan trong n
khơng tan trong n
-
c coi là 1 acid amin phân c c. Tuy nhiên d a vào
c c a Tyr t i pH trung tính thì nó
c xem nh là acid amin
c.
Các acid amin không phân c c nh : Gly, Ala, Val, Leu, Ileu, Pro, Trp, Met,
Tyr, Phe
-
Các acid amin phân c c trong n
Arg, Cys, Asn
Ng
i th c hi n: TR N
I NGH A
c nh : Thr, Glu, His, Ser, Asp, Gln, Lys,