BAI 60AXIT CACBOXYLIC
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (433.34 KB, 29 trang )
<span class='text_page_counter'>(1)</span><div class='page_container' data-page=1>
ĐẠI HỌC ĐÀ NẴNG
TRƯỜNG ĐẠI HỌC SƯ PHẠM
KHOA HÓA
<b>XIN CHÀO MỪNG</b>
</div>
<span class='text_page_counter'>(2)</span><div class='page_container' data-page=2>
<b>BÀI GIẢNG ĐIỆN TỬ </b>
<b>HÓA HỌC 11 NC </b>
</div>
<span class='text_page_counter'>(3)</span><div class='page_container' data-page=3>
<b>KIỂM TRA BÀI CŨ</b>
HỌC SINH 1
1. Hãy nêu đặc điểm cấu trúc của
nhóm cacbonyl, và nhận xét sự
khác nhau giữa nhóm chức
andehyt và nhóm chức xeton.
2. Một andehit no A mạch hở,
khơng phân nhánh, có CTTN là
(C<sub>2</sub>H<sub>3</sub>O)<sub>n</sub>. Tìm CTCT của A. Viết
ptpư của A với H<sub>2</sub>,AgNO<sub>3</sub>/NH<sub>3</sub>
HỌC SINH 2
1. Nêu quá trình nhận biết để
phân biệt andehyt và xeton?
</div>
<span class='text_page_counter'>(4)</span><div class='page_container' data-page=4>
<b>BÀI</b>
<b>6</b>
<b>0</b>
<b>AXIT CACBOXYLIC:</b>
<b>CẤU TRÚC, DANH PHÁP </b>
<b>VÀ TÍNH CHẤT VẬT LÝ</b>
</div>
<span class='text_page_counter'>(5)</span><div class='page_container' data-page=5>
<b>NỘI DUNG BÀI HỌC:</b>
<b>I</b>
<b>II</b>
<b>ĐỊNH NGHĨA, PHÂN LOẠI, DANH PHÁP</b>
</div>
<span class='text_page_counter'>(6)</span><div class='page_container' data-page=6>
<b>I. ĐỊNH NGHĨA, PHÂN LOẠI, DANH PHÁP</b>
C H
O
R C OH
O
R
R
–
OH
H1.
H2. <sub>H3.</sub>
<b>Vậy ở H3, nhóm - COOH là sự kết hợp của nhóm cacbonyl ( >C=O ) </b>
<b>và nhóm hidroxyl (- OH). Nên được gọi là nhóm cacboxyl.</b>
</div>
<span class='text_page_counter'>(7)</span><div class='page_container' data-page=7>
Axit cacboxylic là những hợp chất hữu cơ mà
phân tử có nhóm cacboxyl ( - COOH) liên kết
trực tiếp với nguyên tử cacbon hoặc nguyên tử
hidro.
<b>1. ĐỊNH NGHĨA:</b>
VD: <b>HCOOH , CH<sub>3</sub>COOH , C<sub>6</sub>H<sub>5 </sub>COOH</b>
</div>
<span class='text_page_counter'>(8)</span><div class='page_container' data-page=8>
<sub>Theo gốc hidrocacbon</sub>
<b>2. PHÂN LOẠI:</b>
<b>I. ĐỊNH NGHĨA, PHÂN LOẠI, DANH PHÁP</b>
• <sub>Axit no: </sub>C<sub>n</sub>H<sub>2n+1</sub>COOH
• <sub>Axit khơng no : </sub>C<sub>n</sub>H<sub>2n+1-2a</sub>COOH
• <sub>Axit thơm : </sub> C<sub>n</sub>H<sub>2n-7</sub>COOH
• <sub>Đơn chức: RCOOH</sub>
• <sub>Đa chức: </sub>C<sub>n</sub>H<sub>2n+2-a </sub>(COOH )<sub>a</sub>
</div>
<span class='text_page_counter'>(9)</span><div class='page_container' data-page=9>
<b>3. DANH PHÁP</b>
<b>I. ĐỊNH NGHĨA, PHÂN LOẠI, DANH PHÁP</b>
TÊN
THƯỜNG
TÊN
THAY THẾ
Theo nguồn gốc tìm ra axit
</div>
<span class='text_page_counter'>(10)</span><div class='page_container' data-page=10>
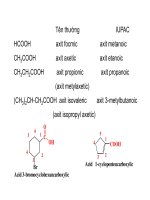
Công thức Tên thông thường Tên thay thế
H-COOH
CH<sub>3 </sub>-COOH
CH<sub>3</sub>CH<sub>2 </sub>–COOH
(CH <sub>3</sub>)<sub>2</sub>CH-COOH
CH<sub>3</sub>(CH <sub>2</sub>)<sub>3</sub>-COOH
CH<sub>2</sub>=CH-COOH
CH<sub>2</sub>=C(CH<sub>3</sub>)-COOH
HOOC-COOH
C<sub>6</sub>H<sub>5</sub>-COOH
Axit fomic
Axit axetic
Axit propionic
Axit isobutiric
Axit valeric
Axit acrylic
Axit metacrylic
Axit oxalic
Axit benzoic
Axit metanoic
Axit etanoic
Axit propanoic
Axit 2-metylpropanoic
Axit pentanoic
Axit propenoic
Axit 2-metylpropenoic
Axit etandioic
Axit benzoic
Dãy C<sub>n</sub>H<sub>2n+1</sub>COOH được gọi là dãy đồng đẵng của axit fomic (HCOOH<b>) </b>
</div>
<span class='text_page_counter'>(11)</span><div class='page_container' data-page=11></div>
<span class='text_page_counter'>(12)</span><div class='page_container' data-page=12>
<b>II. CẤU TRÚC VÀ TÍNH CHẤT VẬT LÍ</b>
R
C
<sub>O</sub>
<sub>H</sub>
H
O
<b>1. CẤU TRÚC:</b>
Sự dịch chuyển mật độ
</div>
<span class='text_page_counter'>(13)</span><div class='page_container' data-page=13>
<b>2. T</b>
<b>í</b>
<b>nh chất vật lý:</b>
<b>II. CẤU TRÚC VÀ TÍNH CHẤT VẬT LÍ</b>
<sub>Trạng thái: ở điều kiện thường, axit cacboxylic ở </sub>
trạng thái lỏng hoặc rắn
<sub>Nhiệt độ sôi: cao hơn anđehit, xeton và ancol </sub>
tương ứng có cùng số C
<sub>Tính tan: axit có số C thấp tan được trong nước. </sub>
Các axit C
1, C
2, C
3tan vô hạn trong nước. Số C tăng
độ tan giảm
</div>
<span class='text_page_counter'>(14)</span><div class='page_container' data-page=14>
→ t
0s(axit)
> t
0s(rượu)> t
0s(andehyt)> ete, dẫn xuất halogen
v
à
c
á
c hợp chất chất c
ó
phân tử lượng tương đương.
R
CO H O
O <sub>H</sub> <sub>O</sub>
C R
- Tạo liên kết hydro liên phân tử
.</div>
<span class='text_page_counter'>(15)</span><div class='page_container' data-page=15>
H
O
C
R
O
H
O
C
R
O
H
O
C
O
R
-
<sub>Tan được trong nước do tạo được liên kết hydro với</sub>
nước, C
<sub>1</sub>---> C
<sub>3</sub>tan gần như vô hạn trong nước.
</div>
<span class='text_page_counter'>(16)</span><div class='page_container' data-page=16></div>
<span class='text_page_counter'>(17)</span><div class='page_container' data-page=17>
<b>ĐỌC TÊN MỘT SỐ HỢP CHẤT </b>
CH
<sub>3</sub> <sub>CH</sub> <sub>CH</sub><sub>2</sub> <sub>COOH</sub>CH<sub>3</sub>
1
2
3
4
</div>
<span class='text_page_counter'>(18)</span><div class='page_container' data-page=18>
CH
<sub>2</sub><sub>C</sub>
<sub>CH</sub>
<sub>2</sub><sub>COOH</sub>
CH
<sub>3</sub>1
2
3
4
</div>
<span class='text_page_counter'>(19)</span><div class='page_container' data-page=19>
HOOC
CH
<sub>2</sub>CH
<sub>2</sub><sub>COOH</sub>
OH
OH
1
<sub>2</sub>
<sub>3</sub>
<sub>4</sub>
</div>
<span class='text_page_counter'>(20)</span><div class='page_container' data-page=20></div>
<span class='text_page_counter'>(21)</span><div class='page_container' data-page=21>
<i>Nước chanh vốn</i>
<i>có nhiều axit</i>
<i>Citric (axit</i>
</div>
<span class='text_page_counter'>(22)</span><div class='page_container' data-page=22>
Nho dùng để chế biến nhiều món ăn và đồ uống ngon, có
màu sắc và có mùi thơm hấp dẫn như rượu nho, nước
ép ....Trong nho có chứa axit tatric tạo vị chua nhẹ
</div>
<span class='text_page_counter'>(23)</span><div class='page_container' data-page=23>
Axit fomic: Axit này được S.Fischer và J.Wray nêu lên từ
năm 1670, nhưng đến năm 1749 A.S.Maggrat điều chế được
ở trạng thái tương đối nguyên chất bằng cách chưng cất loài
kiến đỏ có tên là fomica rufa. Chính từ đó, vào năm 1971,
người ta đặt tên nó là axit fomic.
</div>
<span class='text_page_counter'>(24)</span><div class='page_container' data-page=24>
<b>AXIT LACTIC</b>
</div>
<span class='text_page_counter'>(25)</span><div class='page_container' data-page=25>
Axit axetic : Đã từ rất lâu người ta biết axit này có trong
vang bị chua. Khoảng năm 1700, Stahl điều chế được
axit axetic đậm đặc. Tên Latinh của CH3COOH là
acidum acetium, có nghĩa là axit của vang chua (acere:
chua). .
</div>
<span class='text_page_counter'>(26)</span><div class='page_container' data-page=26></div>
<span class='text_page_counter'>(27)</span><div class='page_container' data-page=27>
<sub>Nhóm cacboxyl là sự tổ hợp của nhóm </sub>
cacbonyl
(>C=O)
và nhóm hiđroxyl (-OH).
<i><b></b></i>
<i> NHĨM C = O khơng giống trong anđehit và xeton.</i>
<i><b></b></i>
<i> Nhóm –O–H phân cực hơn nhóm –O–H trong ancol và phenol </i> <i><b></b></i>
</div>
<span class='text_page_counter'>(28)</span><div class='page_container' data-page=28>
Nhóm cacbonyl có cấu trúc như sau: >C = O
Andehyt là sự liên kết trực tiếp giữa 1 gốc hidrocacbon và 1 nguyên tử H
R C
O
H
Xeton là sự liênkết giữa 2 gốc hidrocacbon
R
CO
R
</div>
<span class='text_page_counter'>(29)</span><div class='page_container' data-page=29>
CÂU 2:
Cho dung dịch amoniac vào ống nghiệm đựng dung dịch AgNO<sub>3 </sub>đến khi
kết tủa sinh ra bị hòa tan hồn tồn, lần lượt thêm vào đó từng dung dịch
một ( nhiệt độ) , dung dịch nào làm cho trên thành ống nghiệm xuất hiện
lớp bạc sáng . Đó chính là andehyc.
AgNO<sub>3</sub> + 3NO<sub>3</sub> + H<sub>2</sub>O → [Ag(NH<sub>3</sub>)<sub>2</sub>]OH + NH<sub>4</sub>NO<sub>3</sub>
(phức chất tan)
</div>
<!--links-->