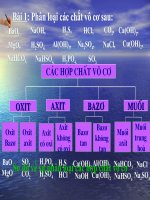
Bài 13. LUYỆN TẬP CHƯƠNG I: CÁC LOẠI HỢP CHẤT VÔ CƠ
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (132.99 KB, 4 trang )
<span class='text_page_counter'>(1)</span>Ngày soạn: Ngày giảng:. Tiết 17. Bài 13. LUYỆN TẬP CHƯƠNG I: CÁC LOẠI HỢP CHẤT VÔ CƠ I. Mục tiêu 1. Kiến thức - Hs được ôn tập để hiểu kỹ về tính chất hóa học của các loại hợp chất vô cơ và mối quan hệ của chúng. - Viết được các phương trình hoá học thực hiện sự chuyển hóa của các loại hợp chất vô cơ đó. 2. Năng lực *Năng lực chung: Năng lực tự học, năng lực tự giải quyết vấn đề, năng lực hợp tác, năng lực tính toán. *Năng lực chuyên biệt: Năng lực sử dụng ngôn ngữ hóa học, năng lực thực hành hóa học, năng lực vận dụng kiến thức hóa học vào cuộc sống. 3. Phẩm chất: - Chăm chỉ, trung thực, trách nhiệm. II. Thiết bị dạy học và học liệu 1. GV: + Bảng phụ : Sơ đồ sự phân loại các hợp chất vô cơ . Sơ đồ câm t/c hoá học của các loại hợp chất vô cơ . + Bảng phụ : bài tập 1,2 SGK , 12 . 8 (SBT ) 2. HS: Đọc trước bài ở nhà. Ôn lại các kiến thức về oxit, axit, bazơ, muối. Bảng nhóm, bút dạ. III. Tiến trình dạy học. A. Hoạt động mở đầu: 5’ - Mục tiêu: Giúp học sinh phát sinh nhu cầu tìm hiểu về vấn đề cần giải quyết - Nội dung: HS 2 đội thi viết sơ đồ tư duy về tính chất hóa học của các chất đã ôn tập ở bài 12. - Sản phẩm: Sơ đồ tư duy về tính chất hóa học của các chất đã ôn tập ở bài 12 của nhóm - Cách tổ chức thực hiện: Hoạt động của GV và HS GV: tổ chức trò chơi thi giữa 2 đội: Yêu cầu HS viết HS viết sơ đồ tư duy về tính chất hóa học của các chất đã ôn tập ở bài 12.đã ôn tập ở bài 12. HS: Thực hiện theo yêu cầu của GV, cử 5 hs viết lên bảng lớp HS: thảo luận nhóm viết câu trả lời vào phiếu học tập. Sau 3 phút cử 5 bạn viết nhanh lên. Nội dung.
<span class='text_page_counter'>(2)</span> bảng, mỗi HS viết 1 lần HS: nghe câu trả lời, nhận xét, bổ sung nếu có. Gv: nhận xét, đánh giá điểm và nêu vấn đề B. Hoạt động hình thành kiến thức Hoạt động 1: Kiến thức cần nhớ(10’) - Mục tiêu: Củng cố được sự phân loại, tính chất hóa học của các hợp chất vô cơ. - Nội dung: Hs trả lời câu hỏi hệ thống kiến thức các tính chất hóa học của oxit bazơ, oxit axit, axit, muối. - Sản phẩm: Câu trả lời của HS - Cách tổ chức thực hiện: Hoạt động của GV-HS - Hợp chất VC được phân thành mấy loại? → 4 loại: oxit, axit, bazơ, muối. Nội dung ghi bảng I. Kiến thức cần nhớ + H2O. 1. Phân loại các hợp chất vô cơ. - Mỗi loại hợp chất đó lại được phân loại 2. Tính chất hóa học các hợp chất vô như thế nào? cơ - Cho 3 ví dụ cụ thể về mỗi loại chất? → HS trả lời →Cho ví dụ - Nhìn vào sơ đồ nhắc lại các tính chất hóa học của oxit bazơ, oxit axit, axit, muối → HS trả lời - Muối có những tính chất hóa học nào? -M + KL; M + Axit; M + Bazo; M + M; phân hủy Hoạt động 2: II. Luyện tập (20’) - Mục tiêu: HS rèn kĩ năng làm bài tập định tính và định lượng. - Nội dung: HS hoạt động theo nhóm, cá nhân làm bài tập phần luyện tập - Sản phẩm: Nội dung bài làm của HS, nhóm. - Cách tổ chức thực hiện: Hoạt động của GV-HS 1. Trình bày phương pháp hóa học để nhận biết 5 lọ hóa chất mà chỉ dùng quỳ tím: KOH, HCl, H2SO4, Ba(OH)2, KCl HS làm theo nhóm . - Lấy vào lọ 1 ít dung dịch. Cho giấy. Nội dung ghi bảng II. Luyện tập 1. - Lấy vào lọ 1 ít dung dịch. Cho giấy quỳ vào → Không chuyển màu: KCl → Đỏ: HCl, H2SO4 → (I).
<span class='text_page_counter'>(3)</span> quỳ vào → Không chuyển màu: KCl → Đỏ: HCl, H2SO4 → (I) → Xanh: KOH, Ba(OH)2 → (II) - Cho lần lượt các dd ở (I) vào các dd ở (II) + Kết tủa trắng là H2SO4 (I) và Ba(OH)2 (II) + Còn lại là HCl (I) và KOH (II) Ba(OH)2 + H2SO4 → BaSO4 + 2H2O 2. Cho biết Mg(OH)2, CaCO3, K2SO4, CuO, NaOH, P2O5 a. Gọi tên phân loại các hợp chất trên? b. Chất nào tác dụng được với: - Dung dịch HCl - dung dịch Ba(OH)2 - Dung dịch BaCl2 Viết các ptpư xảy ra? - Hướng dẫn các nhóm lập bảng: 3. Hòa tan 9,2 g hỗn hợp gồm Mg, MgO cần vừa đủ m(g) dd HCl 14,6%. Sau phản ứng thu được 1,12 lít khí(đktc) a. Tính % về khối lượng mỗi chất trong hỗn hợp đầu? b. Tính C% của dung dịch thu được sau phản ứng? → HS nêu hướng giải từng câu?. → Xanh: KOH, Ba(OH)2 → (II) - Cho lần lượt các dd ở (I) vào các dd ở (II) + Kết tủa trắng là H2SO4 (I) và Ba(OH)2 (II) + Còn lại là HCl (I) và KOH (II) Ba(OH)2+ H2SO4 → BaSO4 + 2H2O BT 2 ⃗ Mg(OH)2 + HCl ❑ ⃗ CaCO3 + HCl ❑ ⃗ CuO + HCl ❑ ⃗ NaOH + HCl ❑ ⃗ K2SO4 + Ba(OH)2 ❑ ⃗ HNO3 + Ba(OH)2 ❑ ⃗ P2O5 + Ba(OH)2 ❑ ⃗ K2SO4 + BaCl2 ❑. BT3. a. Mg + 2HCl → MgCl2 + H2 (1) MgO + 2HCl → MgCl2 + H2O (2) V 1 , 12 = =0 ,05 (mol) 22 , 4 22 , 4 (1):n Mg=nMgCl =n H =0 , 05(mol) mMg=0 , 05. 24=1,2 g mMgO =9,2− 1,2=8 g 1,2 %Mg = . 100 %=13 % 9,2 %MgO =100 −13=87 % nH = 2. 2. 2. b. (1)nHCl =2 n M =0,1 mol 8 nMgO = =0,2 mol 40 (2):nHCl =2 . nMgO =0,4 mol nHCl(1),(2)=0,1+0,4=0,5 mol m HCl=0,5. 36 , 5=18 , 25 g 18 ,25 mddHCl = . 100=125 g 14 , 6 g. c.. nMgCl (1) =0 , 05 mol nMgCl (2) =0,2 mol → nMgCl (1),(2 )=0 , 05+0,2=0 , 25 mol m MgCl =0 , 25 . 95=23 , 75 g 2. 2. 2. 2. mdd sau phản ứng = m hỗn hợp + mddHCl - mH. 2.
<span class='text_page_counter'>(4)</span> = 9,2 + 125 -0,05.2 = 134,1g. % MgCl = 2. 23 ,75 . 100 %=17 , 7 % 134 , 1. C. Hoạt động luyện tập: 5’ - Mục tiêu: Đánh giá kĩ năng làm bài tập định lượng của HS - Nội dung: HS làm cá nhân bài tập 1 GV giao tại lớp vào vở. - Sản phẩm: Bài làm của cá nhân HS - Cách tổ chức thực hiện: Bài 1: Cho CuCl2 dư vào 200ml dung dịch NaOH 2M. Tính khối lượng kết tủa thu được sau phản ứng? HS: Làm cá nhân GV: Thu vở chấm Đáp án:: nNaOH =200.2/1000 = 0,4(mol) PTHH: 2NaOH + CuCl2 Cu(OH)2 +2NaCl Theo PTHH: nCu(OH)2=1/2.nNaOH= 0,2(mol) mCu(OH)2 = 0,2.98=19,6(g). D. Hoạt động vận dụng: 4’ - Mục tiêu: - Củng cố kiến thức bài học qua sơ đồ tư duy. - Vận dụng kiến thức đã học làm bài tập 2. - Nội dung: - HS hoạt động hoạt động nhóm đôi hoàn thiện sơ đồ tư duy của bài học. - Hs làm bài tập 2 cá nhân. - Sản phẩm:Phần bài làm của HS. - Cách tổ chức thực hiện: Vẽ sơ đồ tư duy khái quát lại nội dung bài học Bài tập 2: Thổi 2,464 lit khí CO2 vào một dung dịch NaOH thì được 9,46g hỗn hợp 2 muối Na2CO3 và NaHCO3. Hãy xác định thành phần khối lượng của hỗn hợp 2 muối đó. Đáp số: 8,4g NaHCO3 và 1,06g Na2CO3 *Hướng dẫn tự học ở nhà. - Làm bài tập trang 43 SGK, 12.5 trang 15 SBT. - Ôn tập, chuẩn bị kiểm tra giữa kì.
<span class='text_page_counter'>(5)</span>