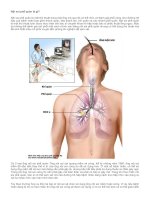
nội soi phế quản áp dụng mitomycin c tạo chỗ điều trị hẹp đường thở lành tính
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (281.08 KB, 6 trang )
NỘI SOI PHẾ QUẢN ÁP DỤNG MITOMYCIN C
TẠI CHỖ ĐIỀU TRỊ HẸP ĐƯỜNG THỞ LÀNH TÍNH
PGS.TS.BSCKII. Nguyễn Chi Lăng
Bệnh viện Phổi Trung ương
TĨM TẮT
Hẹp đường thở trung tâm lành tính ( Benign central airway stenosis / BTS) được định
nghĩa là một q trình bệnh khơng ác tính dẫn đến thu hẹp khí quản và phế quản gốc.
Có vơ số các bệnh lý lành tính có thể dẫn đến hẹp đường thở nghiêm trọng gây tình
trạng đe doạ tính mạng người bệnh.Việc xử lý BTS lành tính, địi hỏi một cách tiếp cận
đa mô thức, thường bao gồm bác sĩ phổi can thiệp, bác sĩ phẫu thuật lồng ngực, bác sĩ
tai mũi họng, bác sĩ thấp khớp, bác sĩ chuyên khoa bệnh truyền nhiễm và bác sĩ gây
mê. Các mục tiêu chính của xử lý BTS lành tính bao gồm ổn định đường thở, giải quyết
các triệu chứng và cải thiện chất lượng cuộc sống thông qua cải thiện sự thông thoáng
đường thở.
Hiện nay phương pháp nội soi phế quản đa mơ thức có sẵn để điều trị hẹp nghẽn đường
thở bao gồm các liệu pháp nóng (laser Nd: YAG, đốt điện, đông huyết tương argon),
các liệu pháp lạnh (áp lạnh, cryodebridement, cryospray), microdebrider, nong bóng và
đặt stent đường thở. Mặc dù một loạt các kỹ thuật nội soi can thiệp gần đây đã được
phát triển để làm giảm tắc nghẽn đường thở ngay lập tức, nhưng chúng có thể gây ra tổn
thương cho cấu trúc đường thở, dẫn đến mô hạt quá mức và hình thành sẹo trong quá
trình chữa lành vết thương và cuối cùng là tái hẹp.
Trong bài viết tổng quan này chúng tơi trình bày một số báo cáo về áp dụng mitomycin
C tại chỗ trong khi nội soi phế quản can thiệp để hạn chế tái phát hẹp đường thở.lành
tính.
SUMMARY
Benign central airway stenosis (BTS) is defined as a non-malignant disease process that
results in narrowing of the trachea and main bronchus. The treatment of benign BTS
requires a multimodal approach, often including interventional pulmonologist, thoracic
surgeon, otolaryngologist, rheumatologist, infectious disease specialist and
anesthesiologist.The main goals of management of benign BTS include stabilizing the
airway, resolving symptoms, and improving quality of life through improved airway
patency.
Currently, multimodal bronchoscopy is available for the treatment of airway obstruction
including hot therapies (Nd:YAG laser, electrocoagulation, argon plasma coagulation),
cryotherapy (cryotherapy, cryodebridement , cryospray), microdebrider, balloon dilation
and airway stenting. Although a variety of interventional endoscopic techniques have
recently been developed to provide immediate relief of airway obstruction, but they can
cause damage to airway structures, resulting in excessive granulation tissue and
formation scarring during wound healing and finally re-narrowing.
In this review, we present several reports on topical application of mitomycin C during
interventional bronchoscopy to limit recurrence of benign airway stenosis.
1
1. Cơ sở áp dụng mitomycin C tại chỗ điều trị sẹo hẹp
Mitomycin là một loại kháng sinh được sản xuất bởi Streptomyces caespitosus . Nó
lần đầu tiên được phân lập bởi Wakaki và các cộng sự vào năm 1958 [1]. Nó có đặc tính
chống ung thư và chống tăng sinh. Hoạt động chống ung thư của Mitomycin tương tự như
hoạt động của các chất alkyl hóa, gây ra sự phá vỡ băng đơn và liên kết chéo của DNA tại các
phân tử adenosine và guanine, do đó ức chế sự tổng hợp RNA và protein. Là một chất chống
tăng sinh, nó có thể ức chế sự tăng sinh nguyên bào sợi do đó giảm sự hình thành sẹo.
Năm 1963, Kunitomo và Mori [2] trình bày ứng dụng lâm sàng đầu tiên của
mitomycin để điều trị mộng thịt. Đặc tính chống tăng sinh của Mitomycin trên nguyên bào sợi
đã được thể hiện trong cơ thể sống và trong ống nghiệm [3]. Kể từ những năm 1980,
mitomycin đã được chấp nhận rộng rãi như một chất chống sẹo trong lĩnh vực nhãn khoa và
đã được sử dụng thành công như một phương pháp điều trị hỗ trợ trong phẫu thuật tăng nhãn
áp, phẫu thuật cắt u nang bìu và cắt dây thần kinh thị giác [4] , Ward và April [5] đã chỉ ra
rằng mitomycin có thể có hiệu quả trong việc giảm sẹo hẹp khí quản và mơ hạt. Rahbar và
các cộng sự [6,7], đã báo cáo việc sử dụng lâm sàng đầu tiên việc sử dụng mitomycin tại chỗ
như một phương pháp điều trị bổ trợ để điều trị bằng laser carbon dioxide qua nội soi đối với
chứng hẹp thanh quản và khí quản ở trẻ em và người lớn.Trong thập kỷ qua, mitomycin đã
được chú ý rộng rãi trong việc ngăn ngừa sự hình thành sẹo vì khả năng ức chế mạnh sự tăng
sinh nguyên bào sợi của nó.
2. Hẹp thanh quản.
Reza Rahbar và cộng sự[8], Nghiên cứu thử nghiệm để khảo sát các ứng dụng của
mitomycin-C tại chỗ trong phẫu thuật, để điều trị và phòng ngừa hẹp thanh môn và dưới thanh
môn. Tám bệnh nhân bị hẹp thanh môn sau và / hoặc hẹp dưới thanh môn được điều trị bằng
phương pháp cắt bỏ bằng laser CO2 qua nội soi, sau đó bơi 0,5 mml mitomycin-C 0,4 mg cho
mỗi ml nước muối trong 4 phút tại vết mổ. Sau thời gian theo dõi trung bình 15 tháng (10-20)
tất cả bệnh nhân đã cải thiện lâm sàng đường thở và giải quyết các triệu chứng trước phẫu
thuật của họ. Khơng có biến chứng nào được ghi nhận trong nghiên cứu này.
Nội soi điều trị hẹp thanh quản bằng cách nong đường thở, mặc dù cải thiện trong thời
gian ngắn, nhưng thường tái phát. Ứng dụng bôi MMC tại thời điểm cắt đốt nội soi và phẫu
thuật laser đã được đề xuất để cải thiện kết quả, nhưng điều này chưa được nghiên cứu một
cách chặt chẽ.
Marshall E Smith và cộng sự [9], nghiên cứu: hai lần bôi MMC tại chỗ cách nhau 3-6
tuần sẽ làm giảm sẹo / tái hẹp đường thở và so sánh với một lần bôi MMC duy nhất. Thiết kế
nghiên cứu: Một thử nghiệm lâm sàng ngẫu nhiên, tiền cứu, mù đơi, có đối chứng với giả
dược: 26 bệnh nhân bị hẹp khí quản do hẹp dưới thanh quản vơ căn, hẹp khí quản sau đặt nội
khí quản, hoặc u hạt Wegener. Tất cả bệnh nhân được điều trị theo một qui trình 3 giai đoạn.
Giai đoạn đầu tiên, sau khi rạch xuyên tâm chỗ hẹp bằng laser CO2 và nong đường thở, tất cả
bệnh nhân được bôi MMC (0,5 mg / mL) tại chỗ vào tổn thương đường thở. Giai đoạn thứ
hai, sau một tháng tất cả bệnh nhân được nội soi lại, thực hiện rạch xuyên tâm và nong chỗ
rạch. Ở giai thứ hai này các bệnh nhân được ngẫu nhiên sử dụng lần thứ hai của mitomycin-C
hoặc áp dụng giả dược nước muối. Giai đoạn ba, sau giai đoạn thứ hai 2 tháng tháng tất cả
VILA I 2
bệnh nhân được nội soi nong bóng mà khơng dùng MMC. Bệnh nhân được theo dõi đến 5
năm vì tái phát hẹp đường thở với các triệu chứng lâm sàng đủ để yêu cầu một thủ thuật tiếp
theo. Các kết quả: Tỷ lệ tái phát ở giai đoạn 1, 3 và 5 năm là 7%, 36% và 69% đối với bệnh
nhân được điều trị với hai lần ứng dụng MMC so với 33%, 58% và 70%, đối với bệnh nhân
được điều trị với một lần bôi MMC. Khoảng thời gian trung bình để tái phát là 3,8 năm ở
nhóm hai lần bơi MMC, so với 2,4 năm ở nhóm một lần bôi MMC. Tac giả kết luận: Thử
nghiệm mù đôi ngẫu nhiên ngẫu nhiên có đối chứng giả dược này cho thấy rằng, trong điều trị
nội soi của hẹp khí quản, hai lần áp dụng MMC cách nhau 3-4 tuần sau khi rạch xuyên tâm
đường thở và giãn nở làm giảm tỷ lệ tái hẹp trong 2 đến 3 năm sau khi điều trị so với một ứng
dụng bôi MMC duy nhất. Tuy nhiên, sự tái phát triệu chứng chậm lại và tái phát hẹp vẫn tiếp
tục và sau 5 năm tỷ lệ tái phát là như nhau. Do đó, MMC có thể làm chậm q trình hẹp,
nhưng khơng ngăn cản tái hẹp.
3. Hẹp thanh - khí quản
Hẹp thanh, khí quản lành tính (LTS) là một thực thể khó điều trị, với nhiều bệnh nhân
phải làm thủ thuật nhiều lần. Lara K Reichert và cộng sự [10], nghiên cứu và đánh giá hiệu
quả của việc áp dụng mitomycin C (MMC) tại chỗ trong phẫu thuật hẹp thanh, khí quản.
Nhóm tác giả xem xét biểu đồ lâm sàng của những bệnh nhân được phẫu thuật LTS từ tháng
1 năm 2005 đến tháng 5 năm 2013. 71 bệnh nhân được chia hai nhóm: 30 bệnh nhân phẫu
thuật có dùng MMC và 41 bênh nhân không dùng MMC. Kết quả được đánh giá số lần thủ
thuật nội soi bôi MMC và khoảng cách thời gian giữa các lần làm thủ thuật. Kết quả: 71 bệnh
nhân được đưa vào nghiên cứu (30 dùng MMC, 41 khơng dùng MMC). Số lượng thủ thuật
trung bình nhóm dùng và không dùng MMC tương tự (2,3 , 2,0 , p> 0,05). Thời gian trung
bình giữa các thủ thuật là 360 ngày ở bệnh nhân dùng MMC và 178 ngày ở bệnh nhân không
dùng MMC với (p = 0,015). Số bệnh nhân suy hơ hấp ở nhóm dùng mitomycin ít hơn nhóm
khơng dùng MMC (6,6 so với 19,5%, p> 0,05). Sử dụng Mitomycin làm tăng thời gian giữa
các thủ thuật ở những bệnh nhân LTS, đặc biệt cho chứng hẹp dưới thanh môn (375 so với
186 ngày, p> 0,05). Tác giả kết luận: kết quả và kinh nghiệm của tác giả với mitomycin
chứng minh nó là một tác nhân hiệu quả để điều trị bổ trợ LTS. Việc sử dụng nó làm kéo dài
thời gian khơng có triệu chứng.
Hẹp khí quản lành tính đã nổi lên như một thách thức điều trị cho các bác sĩ liên quan
đến việc chăm sóc những người sống sót tại các đơn vị chăm sóc quan trọng. Mặc dù phương
pháp điều trị tái tạo phẫu thuật mở truyền thống vẫn được coi là tiêu chuẩn vàng, các liệu
pháp nội soi như cắt đốt tổn thương bằng laser, nong bóng hoặc đặt stent thường được thực
hiện trong bệnh lý phế quản xâm lấn gây chít hẹp. Các u hạt gây tắc nghẽn tái phát là một
thách thức đối với các bác sĩ nội soi. Mitomycin C (MyC) là một chất gây độc tế bào được
phân lập từ Streptomyces caespitosus và hoạt động bằng cách ức chế tổng hợp DNA và RNA
thơng qua q trình alkyl hóa và liên kết chéo. Boaz Tiran và cộng sự 2020[11]. Nghiên cứu
phương pháp tiêm MMC dưới niêm mạc qua nội soi phế quản ống mềm như một phương
pháp điều trị tái phát hẹp khí quản. Các tác giả báo cáo kinh nghiệm thành công của họ
với phương pháp tiêm MMC dưới niêm mạc trong điều trị u hạt tắc nghẽn / hẹp tái phát bằng
cách sử dụng ống nội soi phế quản mềm trên một loạt 10 bệnh nhân từ năm 2005 đến 2019.
3
Các kết quả cho thấy tiêm MMC qua đường nội soi bằng ống soi mềm sau khi điều trị nội soi
vùng tổn thương chít hẹp có thể làm giảm tốc độ hình thành mơ hạt và sẹo sau đó mà khơng
có tác dụng phụ.
Để đánh giá hiệu quả của mitomycin C (MMC) trong điều trị nội soi hẹp thanh khí quản,
Daniele Cristina Cataneo và cộng sự [12], nghiên cứu nong và bôi MMC tại chỗ cho 22 bệnh
nhân hẹp thanh khí quản (15 nam và 7 nữ) được điều trị từ năm 2003 đến 2010. Nguyên nhân
hẹp do đặt nội khí quản ở 15 bệnh nhân và phẫu thuật ở 8. Hẹp khí quản đơn thuần gặp ở 13
bệnh nhân, hẹp dưới thanh quản gặp ở 4, hẹp khí quản. gặp ở 3 và hẹp phức tạp gặp ở 2.
Chiều dài của hẹp từ 0,5 cm đến 2,5 cm, và tỷ lệ hẹp dao động từ 40% đến 100%. Chín bệnh
nhân đã được phẫu thuật mở khí quản và đặt ống Montgomery T có bơi MMC tại chỗ. Điều
trị thành cơng ở 14 bệnh nhân, những người khơng có triệu chứng trong ít nhất 12 tháng. Số
lần bơi MMC tại chỗ từ 1 đến 5 lần. Các biến chứng bao gồm nhiễm nấm, sẹo lồi, u hạt và khí
thũng trung thất. Tác giả kết luận: MMC tỏ ra có hiệu quả trong điều trị nội soi hẹp khí quản.
Hẹp khí quản sau đặt nội khí quản (PITS) tiếp tục là thách thức về chẩn đốn, xử trí và
phịng ngừa. Tình trạng tái phát là phổ biến do sự hình thành mơ hạt q mức và q trình
hình thành sẹo từ từ. Ứng dụng tại chỗ mitomycin-C như một điều trị bổ trợ để xử trí hẹp ống
nội soi đã cho kết quả tốt. Các tác giả nhằm đánh giá kết quả của việc bôi MMC tại chỗ sau
nong nội soi phế quản như một chất bổ trợ trong điều trị PITS. F Viveiros và cộng sự 2013
[13], hồi cứu những bệnh nhân PITS đã được nong phế quản ống cứng sau đó bơi MMC tại
chỗ bổ trợ cho điều trị nội soi. MMC ở nồng độ 0,4 mg / ml được bơi bằng que bơng quanh
vùng tổn thương chít hẹp và mô hạt trong 3 phút. Kết quả: 11 bệnh nhân PITS được điều trị
nong bằng soi phế quản ống cứng bội MMC tại chỗ. Mức độ hẹp khí quản ban đầu trước khi
tiến hành thủ thuật trung bình 75% đường kính. Số lần bơi MMC trung bình được thực hiện
lại là 3,5 lần. Đáp ứng tốt và kéo dài thời gian hình thành mơ hạt ở 55% trường hợp, trung
bình ở 18% và tái phát ở 27%. Cải thiện tình trạng hẹp trung bình là 34%. Kết luận: Sử dụng
MMC tại chỗ ở nồng độ 0,4 mg / ml dường như có kết quả tốt như một chất bổ trợ trong quản
lý PITS với việc giảm mô hạt và cải thiện bền vững đường kính khí quản.
Asad Anwar và cộng sự 2020[14 ] nghiên cứu đánh giá tác dụng của việc bôi
Mitomycin C tại chỗ qua nội soi phế quản cứng ở bệnh nhân hẹp khí quản và mơ hạt quá mức.
Bảy bệnh nhân được chọn cả hồi cứu và hồi cứu. Dung dịch Mitomycin C nồng độ cao 0,4mg
/ ml được bôi lên miếng gạc (2mls) và đưa dưới tầm nhìn trực tiếp qua ống soi phế quản cứng
theo 4 góc phần tư chu vi, mỗi góc 2 phút. Kết quả: Có 2 nam và 5 nữ với độ tuổi trung bình
là 64 tuổi. Sáu bệnh nhân trước đó đã được triển khai đặt stent khí quản để điều trị hẹp khí
quản thứ phát: sau đặt nội khí quản / mở khí quản (2), chèn ép khí quản thứ phát sau ung thư
hạch (3) và rách khí quản (1). Một bệnh nhân bị hẹp khí quản vơ căn. Năm bệnh nhân thu
được kết quả tuyệt vời sau khi bơi Mitomycin C mà khơng có hoặc ít mơ hạt được quan sát
thấy khi nội soi phế quản theo dõi. Giảm tần suất can thiệp cũng được quan sát thấy ở 5 bệnh
nhân này. Mô hạt vẫn tồn tại ở 2 bệnh nhân mặc dù tốc độ tiến triển đã giảm khi nội soi phế
quản cách qng. Khơng có biến chứng nào gặp phải. Tác giả kết luận: Sử dụng Mitomycin C
tại chỗ dường như có kết quả tốt trong xử trí hẹp khí quản với giảm mơ hạt, giảm tiến triển và
cải thiện bền vững đường kính lịng khí quản.
VILA I 4
Hẹp phế quản là một biến chứng đường thở đáng kể ở những bệnh nhân sau ghép
phổi. Xử trí hiện tại với nong phế quản bằng bóng và đặt stent là chưa thật hồn hảo vì một số
ít bệnh nhân đòi hỏi phải làm thủ thuật nhiều lần để duy trì sự thơng thống của đường
thở. Mitomycin C đã được sử dụng vì đặc tính chống xơ hóa của nó trong bệnh hẹp khí quản
khơng ác tính nhưng ứng dụng của nó chưa được nghiên cứu kỹ trong bệnh hẹp đường thở sau
ghép phổi. Davidson và cộng sự, 2019 [15] thực hiện nghiên cứu để đánh giá xem ứng dụng
MMC có làm giảm nhu cầu nong phế quản bằng bóng lặp đi lặp lại trong trường hợp hẹp
đường thở sau ghép phổi hay không. Một nghiên cứu thuần tập hồi cứu về tất cả những người
ghép phổi bị chứng hẹp đường thở và những người đã được điều trị MMC trên 4 năm. MMC
được tiêm dưới niêm mạc chỗ hẹp đường thở. Để đánh giá kết quả tác, giả so sánh tỷ lệ giãn
phế quản trong khoảng thời gian 3 và 6 tháng trước và sau khi điều trị MMC. Kết quả: Mười
một người ghép phổi, bị hẹp đường thở đã được đưa vào nghiên cứu, những người yêu cầu
nong bóng tái đi tái lại nhiều lần, mặc dù đã đặt stent đường thở ở 73% số bệnh nhân
này. Đánh giá kết quả ở thời điểm 3 tháng sau khi điều trị MMC, giảm độ hẹp phế quản từ độ
3 xuống 1 ( P = 0,023), và ở tháng thứ 6, giám độ hẹp phế quản từ độ 3 đến độ 2 ( P=
0,004). Đo chức năng hơ hấp có xu hướng cải thiện thể tích thở ra cưỡng bức trong một giây (
FEV1) và dung tích sống cưỡng bức (FVC). Khơng có tác dụng phụ nào liên quan đến điều trị
MMC. Tác giả kết luận: Ứng dụng MMC là an tồn và có liên quan đến việc giảm tần suất
phải soi phế quản nong bóng giãn khí phế quản ở bệnh nhân hẹp đường thở sau ghép phổi.
Đánh giá liệu việc bổ sung mitomycin-C tại chỗ vào vết thương sau khi điều trị nội soi
hẹp thanh khí quản (LTS) có dẫn đến cải thiện kết quả lâm sàng hay không, C Blake Simpson
và cộng sự, 2006 [16], nghiên cứu hồi cứu những bệnh nhân bị LTS được điều trị trong
khoảng thời gian 6 năm. Các bệnh nhân được phân chia thành hai nhóm, nhóm 1: bệnh nhân
được điều trị nội soi đơn thuần và nhóm 2: điều trị nội soi + MMC tại chỗ. Khoảng thời gian
"khơng có triệu chứng" được xác định (tính bằng tháng) cho mỗi đối tượng bằng cách sử dụng
thuật toán kiểm định T test, để phân tích thống kê của các nhóm 1 và nhóm 2. Sáu mươi bảy
thủ thuật nội soi đã được thực hiện cho 36 bệnh nhân bị LTS (trung bình là 1,86 lần soi cho
mỗi bệnh nhân) Thời gian trung bình của khoảng thời gian khơng có triệu chứng sau khi điều
trị nội soi đối với LTS là 4,9 tháng ở nhóm chỉ điều trị nội soi đơn thuần và 23,2 tháng ở
nhóm nội soi được áp dụng MMC tại chỗ. Khoảng thời gian khơng có triệu chứng quan sát
được ở nhóm có MMC dài hơn đáng kể so với nhóm khơng có MMC (P = 1 x 10). Kết quả
của nghiên cứu này cung cấp bằng chứng rõ ràng rằng: MMC tại chỗ là một chất bổ trợ hiệu
quả trong điều trị hẹp thanh khí phế quản.
KẾT LUẬN
Với tác dụng ức chế mạnh tăng sinh nguyên bào sợi, mitomycin C được áp dụng tại
chỗ, bôi hoặc tiêm dưới niêm mạc trong khi nôi soi phế quản can thiệp cho bệnh nhân sẹo
hẹp đường thở lành tính, MMC chứng tỏ có hiệu quả làm giảm mức độ sẹo hẹp, tăng khoảng
thời gian sẹo hẹp tái phát và cải thiện chất lượng chất lượng cuộc sống cho người bệnh.
5
TÀI LIỆU THAM KHẢO
1. Ghabner BAAllegra CJCurt GACalabresi P Antineoplastic agents. In: Goodman LS,
Gilman A, Harman JG, Limbrid LE, eds. The Pharmacological Basis of
Therapeutics. 9th ed. New York, NY: McGraw-Hill; 1996:1233-1287.
2. Kunitomo NMori S Studies on the pterygium, IV: a treatment of the pterygium by
mitomycin-C instillation. Acta Soc Ophthalmol Jpn.1963;67:601-607.
3. Lee DALee TCCortes AEKitada S Effects of mithramycin, mitomycin, daunorubicin,
and bleomycin on human subconjunctival fibroblast attachment and
proliferation. Invest Ophthalmol Vis Sci.1990;31:2136-2144.
4..Palmer
SS Mitomycin
as
adjunct
chemotherapy
with
trabeculectomy. Ophthalmology.1991;98:317-321.
5.Ward RFApril MM Mitomycin-C in the treatment of tracheal cicatrix after tracheal
reconstruction. Int J Pediatr Otorhinolaryngol.1998;44:221-226.
6. Rahbar RValdez TAShapshay SM Preliminary results of intraoperative mitomycin C in
the treatment and prevention of glottic and subglottic stenosis. J Voice.2000;14:282286.
7. Rahbar RShapshay SMHealy GB Mitomycin: effects on laryngeal and tracheal
stenosis: benefits and complications. Ann Otol Rhinol Laryngol.2001;110:1-6.
8. Reza Rahbar et al. Preliminary Results of Intraoperative Mitomycin-C in the Treatment
and Prevention of Glottic and Subglottic Stenosis. Journal of Voice 14(2):282-6.July
2000
9. Marshall E Smith, Mark Elstad. Mitomycin C and the Endoscopic Treatment of
Laryngotracheal Stenosis: Are Two Applications Better Than One? February 2009.The
Laryngoscope 119(2):272-83.
10. Lara K Reichert 1, Alice S Zhao, Lisa T Galati, Stanley M Shapshay.The Efficacy of
Mitomycin C in the Treatment of Laryngotracheal..Stenosis: Results and Experiences
with a Difficult Disease Entity. Otorhinolaryngol Relat Spec. 2015;77(6):351-8.
11. Boaz Tiran, Tal Parluk , et al. Fiberoptic, Bronchoscopic Submucosal Injection of
Mitomycin C for Recurrent Bening Tracheal Stenosis: A Case Series. sr Med Assoc J.
2020 Dec;22(12):757-760.
12. Daniele Cristina Cataneo, 1 Aglaia Moreira Garcia Ximenes. Mitomycin C in the
endoscop treatment of tracheal stenosis: A prospect cohort study. J Bras Pneumol. 2018
Nov-Dec; 44(6): 486–490.
13 F Viveiros , J Gomes, A Oliveira, S Neves, J Almeida. Topical application of mitomycinC as an adjuvant treatment to bronchoscopic procedures in post-intubation tracheal
stenosis. Rev Port Pneumol. 2013 Nov-Dec;19(6):276-80.
14.Asad Anwar, NorditaRamos Bascon, Natalie Barnes, Brendan
Patrick Madden.Usefulness of topical Mitomycin C application via rigid bronchoscopy in the
management of tracheal stenosis.European Respiratory Journal 2020 56: 1196.
15. Davidson, Kevin R. 1 ; Elmasri, Mary et al. Management of Lung Transplant Bronchial
Stenosis With Mitomycin C. Journal of Bronchology & Interventional Pulmonology,
Volume 26, Number 2. 2019 Apr;26(2):124-128.
16. C Blake Simpson, C Blake Simpson. The Efficacy of Mitomycin-C in the Treatment of
Laryngotracheal Stenosis..The Laryngoscope. November 2006 116(10):1923-5.
VILA I 6