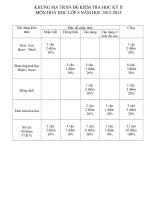
KT Hóa 8 có ma trận & đáp án
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (75.98 KB, 3 trang )
Thứ
PHÒNG GIÁO DỤC – ĐT QUI NHƠN
TRƯỜNG THCS LÊ LI
KIỂM TRA 1 TIẾT
MÔN :HOÁ HỌC
Tiết 46
Thời gian làm bài : 45 phút (không kể thời gian phát đề)
Họ và tên : ……………………………………………………………………………………
Lớp : 8A
Điểm
ngày
tháng năm 2010
– NĂM HỌC : 2009 – 2010
LỚP : 8A
Lời phê của giáo viên
Mã phách
Mã phách
I. TRẮC NGHIỆM: (5 điểm)
Khoanh tròn các chữ cái A,B,C,D của câu mà em cho là đúng:
1. Sự oxi hóa là
A. Sự tác dụng của oxi với một đơn chất
B. Sự tác dụng của oxi với một hợp chất
C. Sự tác dụng của oxi với một chất
D. Sự tác dụng của oxi với một hỗn hợp
2. Dựa vào hóa trò các nguyên tố tạo nên hợp chất oxit với oxi có CTHH đúng là:
A. Na2O , Cu2O , Al2O3 , SO3
B. NaO , CuO , Al2O3 , SO3
C. Na2O , CuO
, Al2O3 , SO4
D. NaO , CuO2 , AlO , SO3
3. Công thức hóa học của các axit tương ứng các oxit sau: CO2 , P2O5 , SO3 , Mn2O7
A. H2CO3 , H3PO4 , H2SO3 , HMnO4
B. H2CO3 , H3PO3
, H2SO4 , HMn2 O7
C. H2CO3 , H3PO4
, H2SO4 , HMnO4
D. H2CO2 , H3PO3 , H2SO3 , HMnO4
4. Qua thí nghiệm ta đã xác đònh thành phần không khí có:
A. 21% khí oxi, 78% các khí khác, 1% khí Nitơ
B. 21% khí oxi, 78% khí Nitơ, 1% các khí khác
C. 21% Nitơ, 78% khí oxi, 1% các khí khác
D. 21% Nitơ, 78% các khí khác, 1% khí oxi
5. Nhiệt phân 0,3mol KclO3 thì thể tích khí oxi thu được (ở đktc) là:
A. 10,08 lít
B. 2,24 lít
C. 6,75 lít
D. 8,96 lít.
6. Oxit là hợp gồm:
A. Oxit là hợp chất của oxi với một nguyên tố khác
B. Oxit là hợp chất có chứa nhóm (SO 4)
C. Oxit là hợp chất có chứa oxi
D. Oxit là hợp chất có chứa nhóm (OH)
7. Oxi có tính chất vật lý là:
A. Chất khí không màu, không mùi, tan nhiều trong nước nặng hơn không khí.
B. Chất khí không màu, không mùi, tan nhiều trong nước nhẹ hơn không khí.
C. Chất khí không màu, không mùi, ít tan trong nước nặng hơn không khí.
D. Là chất khí không màu, mùi hắc, độc, ít tan trong nước, nặng hơn không khí.
8. Sự cháy là:
A. Sự oxi hóa có tỏa nhiệt, không phát sáng
B. Sự oxi hóa chậm có tỏa nhiệt, không phát sáng
C. Sự oxi hóa chậm có tỏa nhiệt, phát sáng
D. Sự oxi hóa có tỏa nhiệt, phát sáng
9. PTHH của phả
đp n ứng điện phân nước.
đp
A. H2O
2H2 + O2
B. 2 H2O
2H2 + O2
C. 2H2O
4H + O2
D. H2O
H2 + O2
10. Đốt cháy 12,8g lưu huỳnh trong không khí, lưu huỳnh cháy sinh ra khí lưu huỳnh đi oxit có khối
lượng là:
A. 256g
B. 2,56g
C. 10,256g
D. 25,6g
II. TỰ LUẬN: ( 5 điểm)
1. (1,5đ) Phân loại các oxit có CTHH sau là oxit axit hay oxit bazơ, và đọc tên các oxit đó
ZnO , Fe2O3 , N2O5 , CO2 , CO3 , K2O
2. (1đ) Hoàn thành cá
c PTHH sau và cho biết thuộc loại phản ứng hóa học nào đã học.
to
a) Al(OH)3
Al2O3 + H2O
b) CaCO3 +o H2O + CO2
Ca(HCO3)2
t
c) KMnO4
K2MnO4 + MnO2 + O2
d) P2O5 + H2O
H3PO4
3. (2,5đ) Đốt cháy 12,4g photpho trong bình đựng không khí sau phản ứng thu được chất rắn màu trắng.
a) Ghi PTHH, đọc tên sản phẩm
b) Tính thể tích khí oxi cần dùng
c) Tính thể tích không khí đã dùng (các khí ở đktc)
d) Tính khối lượng chất tạo thành
BÀI LÀM
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
....................................................................................................................................................................................
ĐÁP ÁN
(Năm học: 2009-2010)
MÔN: HOÁ 8 (tiết 46)
I . TRẮC NGHIỆM (5 điểm) Mỗi câu đúng 0,5đ
Câu
Đáp án
1
C
2
A
3
C
4
B
5
A
6
A
7
C
8
D
9
B
II. TỰ LUẬN: (5 điểm)
Câu 1: (1,5đ) Mỗi CTHH phân loại, gọi tên đúng (0,25đ)
Oxit bazơ
Oxit axit
ZnO : Kẽm oxit
N2O5 : đinitơ penta oxit
Fe2O3 : sắt (III) oxit
CO2 : cacbon đi oxit
K2O : Kali oxit
SO3 : lưu huỳnh tri oxit
Câu 2: (1đ) Mỗi PTHH
ghi đúng, phân loại đúng (0,25đ)
to
a) 2Al(OH)3
Al2O3
+ 3H2O
(PỨ phân hủy)
b) CaCO3 + H2O + CO2
Ca(HCO3)2
(PỨ hóa hợp)
o
t
c) 2 KMnO4
K2MnO4 + MnO2 + O2 (PỨ phân hủy)
d) P2O5 + 3H2O
2H3PO4
(PỨ hóa hợp)
Câu 3: (2,5đ)
a) PTHH 4P + 5O2
to
2P2O5
(đi phopho penta oxit)
(0,5đ)
b) Số mol P = 0,4 (mol)
(0,25đ)
Theo PT tính số mol oxi = 0,5 mol
(0,25đ)
=> VO2 = 11,2 lít
(0,5đ)
c) => Vkk = 56 lít
(0,5đ)
d) Theo PT tính nP2O5 = 0,2 mol -> mP2O5 = 28,4gam
(0,5đ)
10
D