Maladies oculaires - part 8 docx
Bạn đang xem bản rút gọn của tài liệu. Xem và tải ngay bản đầy đủ của tài liệu tại đây (1.11 MB, 44 trang )
Accueil | Photothèque | Annonces | Art | Histoire | Liens | Vue |
Maladies
| Chirurgie | Homepage |
Nous écrire
Maladie de Refsum
Heredopathia atactica polyneuritiformis
Refsum disease
Rev 23-01-2005
jmm
Call to Research project on Refsum disease
<=>
Projet de recherche clinique sur la maladie de
Refsum adulte
Sigvald Refsum
By courtesy of Refsum family
La réalisation de cette page n'aurait pas été possible sans l'aide du
Professeur Patrick Aubourg
(Hôpital Saint-Vincent de Paul, Paris France). Nous le remercions beaucoup.
Définition
Il s'agit d'une
maladie héréditaire du métabolisme
, autosomique récessive, décrite en
1946 par le Norvégien
Sigvald Bernhard Refsum (1907-1991)
.
Cette maladie est due à un mauvais fonctionnement d'
une enzyme
localisée dans les
péroxysomes
qui sont des organites intra-cellulaires dont les fonctions sont multiples:
la dégradation de l'H
2
O
2
produite par les oxydases (rôle antioxydant des
péroxysomes),
la biosynth
è
se de phospholipides
à
liaison
é
ther (plasmalog
è
nes),
et l'oxydation des acides gras à longue chaîne (AGL), à très longue chaîne
(AGTLC), et d'acides gras branchés, dont
l'acide phytanique
.
Les
péroxysomes
contiennent plus de 60 enzymes et sont particulièrement abondants
dans le foie et le rein, mais aussi le système nerveux central et périphérique, ainsi que la
rétine.
L'acide phytanique
est un acide gras issu des aliments. Il provient principalement de la
dégradation de la chlorophylle. On le trouve dans les végétaux et les produits des
herbivores (viande, lait, beurre ).
Acide phytanique
L'acide phytanique doit être régulièrement dégradé par ß-oxydation, comme tous les
acides gras, et cette dégradation ne se fait que dans le péroxysome (la plupart des acides
gras sont dégradés dans la mitochondrie).
L’acide phytanique doit d’abord être activé en ester de CoenzymeA (c'est le phytanoyl
CoA), mais celui-ci ne peut être ß-oxydé directement. Le phytanoyl CoA doit être
hydroxylé en 2-hydroxy-phytanoyl-CoA par une enzyme appellée
phytanoyl-CoA
hydroxylase
(PAHX ou PHYH). C’est cette enzyme qui est dé
ficiente dans la maladie de
Refsum adulte
. Le 2-hydroxy-phytanoyl-CoA est ensuite converti en
acide pristanique
qui peut ensuite être ß-oxydé dans le péroxysome (Fig 1).
Fig. 1: Métabolisme de l'acide phytanique
Le
déficit
d’activité de la
PAHX
provoque une
accumulation
progressive d'acide
phytanique (acide 3,7,11,15
-
t
é
tram
é
thylhexad
é
cano
ï
que) dans tous les organes de
l'organisme, mais provoque des lésions essentiellement dans la rétine, le systè
me nerveux
central (SNC) et les nerfs périphériques.
Il existe d’
autres maladies péroxysomales
comportant une accumulation d’acide
phytanique, mais celles-ci s’accompagnent toujours d’une accumulation d’un autre acide
gras, l’acide pristanique, et souvent d’autres métabolites :
1°) le déficit en
alpha-méthylacyl-CoA racémase
(qui convertit les stéréoisomers R du
phytanoyl-CoA en stéréoisomers S) (Fig.2) provoque une accumulation d’acide
phytanique et pristanique, et une neuropathie sensitivo-motrice avec ou sans rétinite
pigmentaire (comme dans le Refsum adulte). McLean BN, Allen J, Ferdinandusse S,
Wanders RJ. A new defect of peroxisomal function involving pristanic acid: a case
report.J Neurol Neurosurg Psychiatry 2002 Mar;72(3):396-9
2°) le déficit de la
deuxième enzyme
(protéine D-bifonctionnelle) de la ß-oxydation
péroxysomale des AGTLC provoque une accumulation d’
acide phytanique et pristanique
et des intermédiaires de la synthèse des acides biliaires. Ce déficit entraîne une atteinte
neurologique grave dès la naissance ou les premiers mois de vie conduisant au décès
avant l’âge de 2 ans.
3°) les maladies génétiques de la
biogénèse du péroxysomes
entraînent une atteinte
neurologique grave dès la naissance, mais qui peut se manifester parfois seulement à
l’adolescence ou à l’âge adulte. Les formes les moins sévères de ces maladies ont été
décrites dans le passé comme maladie de « Refsum infantile », parce que le premier
métabolite que l’on ait trouvé, s’accumulant anormalement, a été l’acide phytanique. Ces
maladies sont cliniquement, biochimiquement, et génétiquement totalement différentes
de la maladie de Refsum adulte.
Fig. 2: Action de l'alpha-méthylacyl-CoA racémase
Génétique
La grande majorité des maladies de Refsum adulte sont dues à des mutations du gène
PAHX
localisé en 10pter-p11.2, et ces mutations altèrent l’activité enzymatique de
l
’
enzyme.
Une
minorité
des patients atteints de maladie de Refsum n’ont pas de mutation du gène
PAHX. Ils ont par contre une mutation d’une protéine (pex 7) impliquée dans la
biogenèse des péroxysomes. Cette protéine est un récepteur qui permet de cibler à la
surface des péroxysomes les enzymes qui ont un motif d’adressage de type PTS2
(Arg/Lys-Leu-X5-Gln/His-Leu). La phytanoyl-CoA hydroxylase a précisément ce motif
d’adressage PTS2. En cas de mutation de son récepteur (la péroxine 7) dans le cytosol de
la cellule, l’enzyme PAHX ne peut être ciblée dans le péroxysome (Fig. 3). D’autres
mutations du gène PEX 7 donnent une maladie cliniquement totalement différente
(chrondrodysplasie rhyzomélique).
Fig. 3: Le motif d'adressage PTS2
Clinique
Les signes cliniques de cette maladie commencent entre 5 et 20 ans. Il existe souvent une
grande variabilité dans l’intensité et la date d’apparition de chaque symptôme, même
parmi les patients d’une même famille.
On décrit différents groupes de signes cliniques:
=> une rétinopathie pigmentaire,
=> une ataxie cérebelleuse,
=> une polyneuropathie distale motrice symétrique,
=> et parfois
un syndrome pyramidal
une dysarthrie
une anosmie
une surdit
é
et une atteinte cardiaque avec troubles de la conduction.
On peut aussi parfois observer une ichtyose cutanée et une dysplasie modérée des
épiphysaires.
Coup de vent cubital
Latéro-flexion de la main vers le bord cubital
Maladie de Refsum
Le
dosage plasmatique
de l’acide phytanique permet de porter le diagnostic. Il doit être
confirmé par la mesure de l’oxydation de l’acide phytanique dans les
fibroblastes
et la
recherche de la
mutation
du gène PAHX. Il est important d’éliminer d’autres maladies
péroxysomales qui peuvent donner parfois un phénotype clinique voisin (déficit en
racémase, anomalies de la biogénèse des péroxysomes).
Traitements
Pour l'instant il n'y a pas de traitement de l'anomalie génétique.
On a
proposé
de combattre la thésaurismose d'acide phytanique par un
régime
alimentaire
sans produits végétaux et sans aliment contenant de l'acide phytanique. Ce
régime est très difficile à suivre et n’a, à lui seul, que peu d’effets sur la maladie. Par
contre, sa combinaison avec des
plasmaphérèses
régulières permet de diminuer
l'importance de l'ichtyose, et stabiliser la neuropathie et l’atteinte cardiaque. L’
effet de ce
traitement sur l’atteinte oculaire et la surdité
est moins certaine. Il est probable cependant
que plus ce traitement est commencé tôt, plus il a de chance d’être efficace.
Régime diététique pour la maladie de Refsum adulte
Schématiquement :
- pas de viandes rouges : blanc de volaille
- poissons maigres
- 2 œufs par semaine pas plus
- fruits de mer autorisés
- pattes, riz
- légumes uniquement qui poussent sous la terre
-
fruits
é
pluch
é
s et sans p
é
pins
- laitage : 0% matière grasse
- margarine type « Fruit d’Or ».
Alimentation à environ 70 g de protides et 2700 calories, limitée en acide phytanique.
Exemple de répartition au cours de la journée en fonction de vos goû
ts et habitudes alimentaires avec
un apport calorique suffisant pour éviter tout catabolisme entraînant une lipolyse.
Petit déjeuner :
1 café sucré
1 petit pain + confitures ou miel
1 ou 2 verres de jus de fruits : orange, pamplemousse, citron + sucre
Déjeuner :
Crudités en salade assaisonnées à l‘huile de tournesol (1 cuillère à soupe)
Viande ou poisson (voir liste)
Pommes de terre (ou pâtes ou riz) + 1 cuillère à soupe d’huile de tournesol
1 petit pain (ou _ de baguette)
Fruits au sirop
1 verre de jus de fruits sucré
Goûter :
1 petit pain
1 compote + 1 fromage blanc à 0 % de matières grasses ou 1 yaourt à 0 % de matières grasses
+ sucre
1 verre de jus de fruit sucré ou 1 café bien sucré
Soir :
Repas identique à celui du déjeuner avec des légumes en plus.
Dans la soirée :
1 bouillie : 1 à 2 cuillerée à soupe de Maïzena à faire cuire dans _ de litre de lait écrémé ;
lorsque la Maïzena est cuite, ajouter du sucre et un parfum : caramel, vanille ou extrait de
fruits.
Les aliments
strictement interdits
sont principalement les aliments contenant des graisses telles
que :
1. - Graisses du lait et des laitages : fromage, fromage blanc, yaourts au lait entier ou desserts
gélifiés au lait entier ou dessert à base de crème fraîche.
2. - Graisses contenues dans les fruits secs ou oléagineux : olives, noix, noisettes, amandes,
cacahuètes
3. - Chocolat.
4. - Viande des ruminants : bœuf, mouton, chevreuil
5. - Abats, lard.
6. - Poissons gras : poissons bleus. Exemples de poissons maigres : bar, colin, cabillaud, carrelet,
dorade, églefin, limande, sole, merlan, raie ; coquillages (coques, moules) ; seiche ; crabe ;
crevettes.
Lorigine de lacide phytanique et de son prộcurseur le phytol serait
alimentaire plus de 90 %
.
Un rộgime standard (il est trốs difficile de laffirmer dans la mesure oự
la teneur en ces 2 constituants
na ộtộ que trốs peu ộtudiộe) apporterait en moyenne 60 mg/jour dacide phytanique.
Le phytol libre est bien absorbộ par lintestin (60 90 %de la dose ingộrộe) dont 10 20 % sont
transformộs en acide phytanique.
Par contre, le phytol liộ la chrorophylle contenue dans les lộgumes verts est en grande partie
ộliminộe dans les selles.
Un rộgime standard apporterait en moyenne 2 mg/jour de phytol libre.
=>
Lors de la
dộcouverte de la maladie
, alors que les taux sộriques dacide phytanique sont
maximaux (avec des troubles moteurs graves) et selon la compliance du malade, un rộgime trố
s strict
peut ờtre instaurộ ne contenant pas dacide phytanique et/ou de phytol (1ốre ộtape).
Le rộgime est un rộgime liquide, difficile suivre sur de trốs longues pộriodes car peu variộ et
pouvant ờtre plus ou moins bien tolộrộ entraợnant anorexie, vomissements ou diarrhộe. Mais il a pour
but :
- De faire diminuer rapidement laccumulation dacide phytanique.
- Dapporter suffisamment de calories pour ộviter tout catabolisme entraợnant une lipolyse.
- Dộviter les pộriodes de jeỷne puisquil sera pris intervalles rộguliers au cours de la journộe (en 4
ou 5 prises).
Il se compose de la faỗon suivante :
150 g de poudre de lait ộcrộmộ.
30 g Alburone ou Hyperprotidine.
200 g Dextrine Maltose ou Caloreen } composition pour 2 litres
20 g Huile de maùs.
Et sera donnộ raison de 2 ou 2,5 litres par jour
(voir les supplộmentations vitaminiques, minộrales et oligo-ộlộments).
=>
La
2ốme ộtape
du rộgime est de rộintroduire lacide phytanique (et le phytol libre ou liộ la
chlorophylle), mais de faỗon obtenir un rộgime apportant < 10 mg dacide phytanique par jour.
Pour ce faire, diffộrentes listes daliments ont ộtộ faites.
Liste daliments
permis
, volontộ:
Lait ộcrộmộ, yaourts maigres
Poulet, dinde, lapin Poissons maigres (voir liste)
ufs
Fruits en boợte (pas les fruits verts)
Orange fraợche et pamplemousse frais, citron
Betteraves, carottes, champignons, oignons, navets, radis
Lentilles
Huile de tournesol
Th
ộ
,
boissons gazeuses, bi
ố
re, pulpes de fruits, caf
ộ
,
eau, coca
Confitures, gelées, sirops, mélasse, miel
Epices, moutarde
Liste d’aliments
interdits
(graisses des laitages et viandes des ruminants):
Lait entier, lait concentré
Yaourts, fromage blanc, crème
Bœuf, agneau, abats, poissons gras
Maïs, pop-corn
Pommes, bananes, groseilles, raisin, rhubarbe, fruits secs, noix
Tous les légumes verts
Huile végétale, huile d’arachide, beurre, margarine, lard, saindoux
Chocolat, entremets
Fines herbes fraîches
Liste d’aliments
contrôlés:
Aliments contenant 1 mg d
’acide phytanique
- Riz blanc bouilli 100 g
- Spaghettis cuits 85 g
- Pain 60 g
- Corn Flakes 85 g
- Rice Krispies 35 g
- Sugar Puffs 95 g
- Weetabix 65 g
- Crème au lait écrémé 120 g
- Pois chiches en boîte 50 g
- Pommes de terre
Bouillies 150 g
Chips 100 g
Rôties ou sautées 120 g
Aliments contenant 2 mg d
’acide phytanique
Fromage blanc à la louche 100 g
Veau mijoté 90 g
Porc mijoté 50 g
Jambon blanc 40 g
Morue grillée 50 g
Haddock fumé 80 g
Crabe 40 g
Haricots blancs en boîte 70 g
Pois chiches en boîte 100 g
Liste de poissons maigres (taux de lipides < 2 %) : brochet, carpe, goujon, tanche, bar, colin,
cabillaud, carrelet, dorade, églefin, limande, sole, merlan, raie ; coquillages (coques, moules) ;
seiche ; crabe ; crevettes ; grenouille.
Conseil génétique
Un patient atteint de maladie de Refsum n’a aucune chance de transmettre la maladie à
ses enfants, sauf si l
’
autre parent a un lien de parent
é
(
consanguinit
é
).
Les parents d’enfants atteints de maladie de Refsum ont 25% de risque d’avoir d’autre
enfants atteints de la même maladie.
Un
diagnostic pré-natal
peut être proposé dans les familles à risque.
Bibliographie
OMIM
Le site web du péroxysome (en anglais)
Jansen GA, Wanders RJ, Watkins PA, Mihalik SJ.
Phytanoyl-coenzyme A
hydroxylase deficiency the enzyme defect in Refsum's diseas N Engl J Med 1997 Jul
10;337(2):133-4
Jansen GA, Ofman R, Ferdinandusse S, Ijlst L, Muijsers AO, Skjeldal OH, Stokke
O, Jakobs C, Besley GT, Wraith JE, Wanders RJ.
Refsum disease is caused by
mutations in the phytanoyl-CoA hydroxylase gene Nat Genet 1997 Oct;17(2):190-3
Masters-Thomas A, Bailes J, Billimoria JD, Clemens ME, Gibberd FB, Page NG.
Heredopathia atactica polyneuritiformis (Refsum's disease): 1. Clinical features and
dietary management J Hum Nutr 1980 Aug;34(4):245-50
Mihalik SJ, Morrell JC, Kim D, Sacksteder KA, Watkins PA, Gould SJ.
Identification of PAHX, a Refsum disease gene Nat Genet 1997 Oct;17(2):185-9.
Mukherji M, Chien W, Kershaw NJ, Clifton IJ, Schofield CJ, Wierzbicki AS, Lloyd
MD.
Structure-function analysis of phytanoyl-CoA 2-hydroxylase mutations causing
Refsum's disease. Hum Mol Genet. 2001 Sep 1;10(18):1971-82.
Refsum, S.; Salomonsen, L.; Skatvedt, M.
: Heredopathia atactica polyneuritiformis in
children. J. Pediat. 35: 335-343, 1949.
Refsum S
. Heredopathia atactica polyneuritiformis phytanic-acid storage disease,
Refsum's disease:" a biochemically well-defined disease with a specific dietary
treatment" Arch Neurol 1981 Oct;38(10):605-6
Scriver CR, Beaudet AL, Sly WS, Valle D, eds.
The metabolic and molecular basis of
inherited disease, 7th edition. New York: McGraw-hill, Inc.; 1995. 2351-2369.
Traboulsi E.
Genetic diseases of the eye Oxford 1998.
Wanders RJ, Jansen GA, Skjeldal OH.
Refsum disease, peroxisomes and phytanic
acid oxidation: a review J Neuropathol Exp Neurol 2001 Nov;60(11):1021-31.
Wierzbicki AS, Lloyd MD, Schofield CJ, Feher MD, Gibberd FB.
Refsum's disease: a
peroxisomal disorder affecting phytanic acid alpha-oxidation J Neurochem 2002 Mar;80
(5):727
-
35.
Sigvald Refsum
By courtesy of Refsum family
Je remercie la famille de la jeune fille porteuse de cette maladie, qui m'a sensibilis
é à cette
pathologie, ce qui m'a incit
é à écrire ces quelques lignes.
jmm
Accueil | Photothèque | Annonces | Art | Histoire | Liens | Vue |
Maladies
| Chirurgie | Homepage |
Nous écrire
Toxémie gravidique, prééclampsie
Signes oculaires
Pregnancy toxemia
Grossesse et prééclampsie
Rev 17
-
02
-
2003
jmm
Nous remercions le Dr St
éphane Dumas (CHR Orléans France) qui a réalisé
l'angiographie dont nous présentons quelques images.
Définitions
La
toxémie gravidique
, ou
prééclampsie
, est un syndrome général qui atteint 5% de
femmes enceintes, classiquement au dernier trimestre de grossesse, et qui associe une
hypertension artérielle
(HTA), une
protéinurie
, des
oedèmes
, une
hyperuricémie
, une
thrombopénie
, une augmentation des
ASAT
(activité sérique de l'alanine
aminotransférase), et un retard de croissance in utero (RCIU). Sans traitement l'évolution
se fait vers l'éclampsie.
L'
éclampsie
correspond à la survenue de convulsions et/ou de troubles de la conscience.
Elle est responsable en France de 2,2% des morts maternelles (conférence d'experts
2000). Les facteurs de risques sont le jeune
â
ge et le manque de surveillance pr
é
natale.
L'interruption de la grossesse avec extraction de l'enfant, associée à un traitement géné
ral
puissant, visera à éviter la
mort
du foetus et de la mère.
On peut parfois assister à un
HELLP syndrome
, décrit en 1982 par Weinstein, qui
associe hémolyse, cytolyse hépatique et thrombopénie (
H
aemolysis,
E
levated
L
iver
enzymes,
L
ow
P
latelet count). Il peut survenir sans signe de prééclampsie et son
diagnostic est parfois difficile. Le risque majeur est la rupture hépatique avec hématomes
hépatiques. Les signes oculaires de baisse de vision et de soulèvement rétinien peuvent
être présents alors que les signes de prééclampsie sont absents, ce qui doit faire suspecter
le syndrome.
Clinique
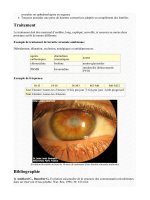
La toxémie gravidique s'accompagne de troubles visuels varié
s pouvant aller de baisse de
vision modérée au décollement séreux rétinien (DSR) bilatéral, comme présenté dans
l'angiographie ci
-dessous. Le
DSR
est dû à un
spasme artériolaire
qui entraîne une
ischémie choroïdienne
. En principe l'atteinte rétinienne est proportionnelle à l'élévation
de la tension artérielle et à la sévérité de la prééclampsie.
L'évolution oculaire
favorable
est la rè
gle, sans traitement chirurgical. C'est le traitement
du syndrome général qui va aboutir à une réapplication de la rétine.
La patiente dont nous présentons l'angiographie avait une vision très faible le premier
jour, elle voyait juste bouger la main devant elle. Apr
ès un traitement adapté, la
récupération fut excellente, avec une vision de 8/10ème, Parinaud 2.
L'angiographie à la phase aiguë objective une
asymétrie de remplissage choroïdien
avec d'
important territoires restant non perfusés
tout au long de la séquence
angiographique:
Angiographie Dr Stéphane Dumas
clichés à J0
Le contrôle au
4ème mois
retrouve des
exsudats
lipidiques profonds de résorption à
gauche, et des
altérations maculaires droites de l'épithélium pigmentaire
qui
expliquent la baisse d'acuité visuelle relative séquellaire sur cet oeil.
On note des
taches d'Elschnig
qui correspondent à des infarctus locaux de la
choriocapillaire. Les artérioles choroïdiennes sont en effet obstruées, ce qui va entraîner
une fuite du colorant lors de l'angiographie. Avec la cicatrisation, ces infarctus se
transforment en lésions pigmentées au centre, avec une dépigmentation périphérique.
On objective aussi des
stries de Siegrist,
qui sont des séquelles de l'ischémie
choroïdienne, et qui apparaissent comme une pigmentation radiaire rectiligne.
Angiographie Dr Stéphane Dumas
clichés à 4 mois
Traitement
Ce sera celui de l'HTA, avec souvent un déclenchement de l'accouchement à cause de la
souffrance foetale aiguë. Le risque d'éclampsie existant pour la mère, il faut une prise en
charge en milieu très spécialisé.
On s'attachera à laisser ces patientes en decubitus dorsal pour limiter le risque d'ectopie
maculaire (Dr Stéphane Dumas).
Conclusion
Ces pathologies ne sont pas exceptionnelles, il faut donc s'en méfier. Tout
trouble visuel
chez la femme enceinte nécessite une consultation ophtalmologique en
urgence
. De cet
examen dépend parfois l'avenir de la femme et de son enfant.
Bibliographie
Réanimation des formes graves de prééclampsie
de Juan E Jr, Vander JF.
Effective macular translocation without scleral imbrication.
Am J Ophthalmol. 1999 Sep;128(3):380
-2.
Fineman MS, Maguire JI, Fineman SW, Benson WE.
Safety of indocyanine green
angiography during pregnancy: a survey of the retina, macula, and vitreous societies.
Arch Ophthalmol. 2001 Mar;119(3):353
-5.
Gonzalvo FJ, Abecia E, Pinilla I, Izaguirre LB, Olivan JM, Honrubia FM.
Central
retinal vein occlusion and HELLP syndrome.
Gupta LY, Mansour SE
. Bilateral bullous retinal detachment as a complication of the
HELLP syndrome. Can J Ophthalmol. 1994 Oct;29(5):242
-5.
Iida T, Kishi S.
Choroidal vascular abnormalities in preeclampsia. Arch Ophthalmol.
2002 Oct;120(10):1406
-
7.
Omarov SM, Yamedov TG
. [Rheo
-
ophthalmology in late pregnancy toxemias] Akush
Ginekol (Mosk). 1972 Mar;48(3):23
-
5.
Valluri S, Adelberg DA, Curtis RS, Olk RJ
. Diagnostic indocyanine green
angiography in preeclampsia. Am J Ophthalmol. 1996 Nov;122(5):672
-
7.
Weinstein L.
Syndrome of hemolysis, elevated liver enzymes, and low platelet count: a
severe consequence of hypertension in pregnancy. Am J Obstet Gynecol. 1982 Jan
15;142(2):159
-
67.
Wenzel M, Lehnen H
. A case of mild ocular manifestations in pregnancy induced
hypertension with HELLP syndrome. Acta Ophthalmol (Copenh). 1994 Jun;72(3):391
-
2.
Accueil | Photothèque | Annonces | Art | Histoire | Liens | Vue |
Maladies
| Chirurgie | Homepage |
Nous écrire
Toxocarose oculaire /1
Rev 19-09-2004
jmm
Suite du texte page 2
Nous remercions beaucoup le
Professeur J
-
F Magnaval
(
Service de Parasitologie, CHU
Rangueil 31403 Toulouse 4
-
France
) qui nous a fourni de nombreux éléments pour réaliser
ce chapitre.
Définition
La
toxocarose
est une anthropozoonose due à l'infestation de l'Homme par des larves
d'un Nématode parasite des Canidés (
Toxocara canis
) ou des Félidés (
Toxocara cati
).
Environ
25% des chiens
et plus de
50% des chats
sont porteurs de ces vers.
Habituellement bénigne, cette parasitose a parfois des complications oculaires, souvent à
type d'
uvéites
.
Les malades présentant une toxocarose oculaire sont souvent de
jeunes enfants
,
contaminés par contact avec un sol souillé d'excréments animaux, ou géophages.
Larve de
Toxocara canis
Cliché
Pr J
-
F Magnaval
, Service de Parasitologie, CHU Rangueil Toulouse France
Historique
Dès
1920
des expériences permirent de retrouver des larves dans les tissus des
mammifères à qui on avait fait avaler des oeufs de
Toxocara canis
.
En
1937 Calhoun
rapporta l'observation d'un enfant porteur d'une larve de nématode
dans la chambre antérieure de l'oeil.
En
1950 Wilder
trouva des débris larvaires ou des larves de nématodes dans certains
globes oculaires enlevés par erreur pour rétinoblastome.
Le parasite
Toxocara canis
est un helminthe (ver) de la classe des Nématodes (vers ronds), qui ne
devient adulte que chez le chien et dont les larves sont en
impasse parasitaire
chez
l'homme.
Toxocara canis
vit dans le duodéno
-
jéjunum du chient. La femelle mesure 6 à 18 cm de
long et le mâle de 4 à 10 cm. Une femelle pond 20.000 à 200.000 oeufs par jour. Ces
oeufs de 80 µ comprennent des micro
-
dépressions (photo ci
-
dessus à droite).
Les
oeufs
émis dans les déjections sont
non embryonnés
et donc
non infectieux
.
L'embryonnement
dans le milieu extérieur (sol) demande une quizaine de jours dans
des conditions de températures optimales. Ces oeufs vont alors contenir une
larve
infestante L2
. Les oeufs embryonnés sont résistants et peuvent rester 2 ans dans le sol;
ils ont une coque ext
é
rieure adh
é
sive, ce qui permet leur fixation sur les doigts, les
Oeuf de
Toxocara canis
Cliché
Pr J
-
F Magnaval
, Service de
Parasitologie, CHU Rangueil Toulouse France
Oeuf de
Toxocara canis
au microscope
électronique à balayage
Cliché
Dr Christophe Guitton
Laboratoire de biologie animale, Université de
Perpignan, France
végétaux
Le chien se
contamine
en absorbant des aliments contenant des oeufs du parasite situés
sur le sol.
Commence alors chez le chien le
cycle somatique
du parasite. Les larves L2 perforent la
paroi intestinale et vont se répandre dans les organes de l'animal.
Les larves qui arrivent à perforer les alvéoles pulmonaires continuent un parcours qui les
amène au carrefour aéro
-
digestif. Elles se retrouvent alors dans le tube digestif du chien
et vont donner des
parasites adultes
.
Larve de
Toxocara canis
dans rétine de singe macaque
Cliché
Pr L.T.Glickman
, Veterinary School, West Lafayette, Indiana, Etats
-
Unis
Contamination de l'homme
L'homme se contamine en absorbant des
oeufs embryonnés
ou des
larves
.
C'est
le sol souillé
par les déjections animales qui est responsable de la contamination, et
non le contact direct avec les chiens (chiots exceptés) ou les chats.
La toxocarose survient souvent chez des personnes qui ont dans leur environnement des
chiens infectés
, ou bien chez les enfants qui ont l'habitude de porter à la bouche leurs
mains après avoir touché le sol ou remué la terre.
Clinique
Les signes cliniques sont fonctions du nombre de larves ingérées, du terrain du patient
(allergique), de son génotype et de la localisation des larves dans les tissus.
Outre la toxocarose oculaire, on rencontre plusieurs autres formes de la maladie.
Larva migrans visc
é
rale
Chez l'adulte on constate une asthénie, des douleurs digestives et parfois une éruption
urticarienne généralisée avec
hyperéosinophilie
. Des granulomes hépatiques peuvent
être localisés (voir image ci
-
dessous). Cette anomalie correspond à un hypersignal T2 en
IRM.
Granulome (hypodense) hépatique à
Toxocara canis
Cliché
Pr J
-
F Magnaval
, Service de Parasitologie, CHU Rangueil Toulouse France
Suite du texte page 2
Accueil | Photothèque | Annonces | Art | Histoire | Liens | Vue |
Maladies
| Chirurgie | Homepage |
Nous écrire
Toxoplasmose oculaire
Cicatrice maculaire
Définition
La
toxoplasmose
est une
zoonose
(maladie des animaux vertébrés transmissible à
l'homme). Cette maladie parasitaire cosmopolite est due à un
protozoaire
nommé
toxoplasme
et plus précisemment
Toxoplasma Gondii
. En raison de sa
faible spécificité
,
cette infection peut atteindre aussi bien l'
homme
que les
animaux homéothermes
(qui
maintiennent une température constante).
Grâce à la présence d'anticorps, on considère qu'en France
90%
des sujets adultes ont
rencontré le parasite.
Cette affection est très fréquente et habituellement
bénigne
. Elle entraîne de graves
problèmes chez la
femme enceinte (foetopathie)
et chez l'
immunodéprimé
.
Une
nouvelle notion
permet d'évoquer la gravité de certaines
toxoplasmoses acquises
qui peuvent parfois donner des lésions oculaires.
Historique
L'histoire retient principalement la découverte de
Charles Nicolle
et
L.Manceaux
en
1908
à l'Institut Pasteur de Tunis. A la suite d'une épidémie de laboratoire chez un
rongeur, le Gondi , ils isolèrent un protozoaire de forme arquée
.
Ils
nommèrent donc le parasite
Toxoplasma Gondii
. L'origine grecque du mot vient de toxon
(arc) et plasma (forme).
Cette découverte sera présentée le 26 octobre 1908 par Laveran, à l'Académie des
Sciences de Paris.
A peu près au même moment,
A.Splendore
trouve ce parasite à la suite de la mort de
lapins de laboratoire, à Sao Paulo. La publication de ces résultats se fera le 16 juillet
1908.
Parasitologie
Clichés dus à l'obligeance du Dr Marie
-
Hélène Bessières, Laboratoire de Parasitologie et
Mycologie, CHU de Rangueil, Toulouse France
Le toxoplasme libre
Il a une forme d'arc avec une extrémité plus effilée, mesure environ 4µm sur 2µm de
large et est appelé
tachyzoïte
. Ce terme vient du grec tachus (rapide) pour évoquer la
rapidité de sa division dans les cellules qui l'hébergent. Il peut se déplacer par des
mouvements circulaires, ondulatoires ou par rotation. Il peut aussi changer de forme, ce
qui a rendu son identification délicate dans les années 1900.
Il ne peut vivre qu'à l'intérieur d'une cellule qu'il parasite. La pénétration peut venir de
deux mécanismes : le parasite peut lyser la membrane cellulaire et s'immiscer à l'inté
rieur
de la cellule, ou bien il peut se faire phagocyter.
Le kyste
Lors de réaction de l'organisme, on peut assister à la formation de kystes toxoplasmiques
(
zoïtokystes
) quasiment immobiles. Il ne se divise que très peu et est appelé bradyzoïte
(du grec bradus
-
lent). Lors de conditions favorables, il y a une transformation des
bradyzoïtes en tachyzoïtes qui vont se déplacer et coloniser les cellules de l'hôte.
Ces kystes sont très résistants au froid et aux agressions exté
rieures, ce qui leur permet de
survivre et de se transformer quand ils trouvent un hôte accueillant.
Les facteurs de transmission
Le cha
t
4 Tachyzoïtes intracellulaires Kyste toxoplasmique
La contamination d'une population dépend étroitement de la fréquence des chats. Ils sont
les seuls
hôtes définitifs
des toxoplasmes, l'homme n'étant qu'un hôte intermédiaire. Les
ookystes
émis par le chat dans les déjections sont très résistants au froid et subsistent des
mois dans la nature. Ils peuvent contaminer des cours d'eau qui seront infestants.
L'absorbtion de ces ookystes par l'homme va entraîner une toxoplasmose.
La viande
La consommation de viande contaminée est la principale cause d'infection
toxoplasmique. La consommation de viande crue ou insuffisamment cuite, rôtie ou
grillée augmente la fréquence de séropositivité.
Clinique
L'infection toxoplasmique du sujet immunocompétent (normal)
=> C'est
très exceptionnellement
une maladie
grave
(quelques sujets dans la litté
rature).
Dans ce cas
-
là on découvre des lésions cardiaques, pulmonaires, neurologiques. En
phase aiguë septicémique le sujet fiévreux transmet des parasites par les larmes, la sueur
ou la salive. Le décès peut survenir rapidement.
=> C'est dans 20% des cas une
forme subaiguë
, avec des adénopathies du cou et de la
nuque (ganglions). Le sujet pyrétique présente une augmentation des monocytes
sanguins. Ce tableau de
lymphadénite
ressemble à une
mononucléose
infectieuse et va
guérir progressivement.
=> Dans 80% des cas il s'agit d'une
forme inapparente
car le patient n'a pas de fièvre,
mais seulement des adénopathies du cou pendant une huitaine de jours. Il ne s'en
souviendra souvent pas.
L'infection foetale
En cours de grossesse le placenta peut être contaminé. Plus l'infection du foetus est
tardive
et plus tard les symptômes cliniques se manifestent. Sur 800000 grossesses
annuelles, 2000 femmes feront une toxoplasmose et 700 foetus seront contaminés. Une
sérologie est obligatoire en prénuptial.
=> La
toxoplasmose congénitale grave
entraîne des
calcifications intracrâniennes
pathognomoniques (caractéristiques). Il s'y ajoute souvent un crâne augmenté
de volume,
une dilatation ventriculaire, des perturbations neurologiques (convulsions, hypotonie) et
des anomalies oculaires graves. On retrouve en effet une
chorior
é
tinite toxoplasmique
uni ou bilatérale qui peut siéger sur la macula et rendre l'enfant quasiment aveugle. Les
formes les plus graves entraînent la mort du foetus.
=> La
toxoplasmose viscérale
, moins grave, atteint malgré tout le foie et entraîne un
ictère néo
-natal associé parfois à des troubles hématologiques.
=> La toxoplasmose congénitale moins sévère, avec des lésions oculaires immédiates ou
survenant plus tardivement chez l'enfant. Ce décalage entre l'infection et la découverte
d'une choriorétinite toxoplasmique est fréquent.
Chez l'immunodéprimé
Que ce soit dans le cadre du sida ou bien dans le temps post
-
opératoire des transplantés
et greffés, on va assiste à une toxoplasmose souvent grave avec prolifération de
tachyzoïtes.
Nouvelles notions de la toxoplasmose acquise
On a longtemps considéré que les lésions oculaires survenaient à la suite de
toxoplasmoses congénitales contractées in utero.
En fait quelques rares auteurs ont décrit des lésions oculaires après des foyers régionaux
de toxoplasmose dus à une contamination de l'eau ou des aliments.
C'est ce qui s'est passé dans le sud du Bré
sil, ainsi qu'en Colombie britannique entre 1994
et 1995. On a vu des séries de chorio-rétinites toxoplasmiques après contamination de
ces populations. Le dogme de la contamination in utero a donc été remis en question.
Les lésions oculaires
Les lésions oculaires sont généralement faciles à reconnaitre mais il existe des formes
cliniques qui peuvent égarer le diagnostic. Classiquement on découvre une
lésion
jaun
âtre
(cliché de gauche) qui peut être paramaculaire ou parapapillaire et cette
anomalie va évoluer vers une
cicatrisation pigmentée
comme sur le cliché de droite. Ici
la lésion est loin de la macula et n'obère pas le pronostic visuel, mais des localisations
plus dangereuses vont nécessiter un traitement adapté.
Le foyer de rétino
-
choroïdite toxoplasmique aiguë
On découvre un foyer typique à bords flous,
jaunâtre
, accompagné souvent d'une
réaction inflammatoire du vitré et de la chambre antérieure. La découverte de foyers
anciens cicatrisés à distance facilite le diagnostic.
Quand le foyer se situe à côté de la papille, on est en face d'une
chorio
-
rétinite juxta
-
papillaire de Jensen
(décrite en
1908
) responsable d'une baisse de vision par déficit
fasciculaire (lésion des fibres nerveuses qui vont vers le nerf optique). Le champ visuel
met en évidence un scotome fasciculaire qui peut s'aggraver sans traitement.
L'angiographie fluorescéïnique montre une lésion hypofluorescente aux temps précoces
puis il y a une coloration du foyer par les bords et les temps tardifs correspondent à une
diffusion globale du colorant.
Des complications peuvent survenir, comme une papillite, un décollement séreux
rétinien, des néovaisseaux prérétiniens ou sous
-
rétiniens.
L'évolution se fera en quelques semaines vers un foyer pigmenté typique.
Le foyer cicatriciel
Il est souvent découvert par hasard et permet de caractériser l'affection. Une cicatrice
maculaire va laisser un oeil quasiment aveugle alors qu'une cicatrice périphé
rique loin du
centre de la vision passsera inaperçue pour le patient.
Une complication est décrite pour ces foyers pigmentés, l'appartion d'une
membrane
épirétinienne
qui va s'étendre sur le pôle postérieur et plisser de plus en plus la ré
tine. Le
sujet verra des images déformées (métamorphopsies). Seul un traitement chirurgical
permettra l'ablation de ces membranes tr
è
s invalidantes.
Lésion toxoplasmique récente jaunâtre
Photo Pr André Mathis CHU Toulouse-Rangueil
France
Lésion toxoplasmique cicatricielle périph
é
Photo Pr André Mathis CHU Toulouse
-
Rangueil
France
Diagnostic biologique
Le
coefficient C de Desmonts
permet d'évaluer la production d'anticorps anti-
toxoplasmiques dans l'humeur aqueuse, prélevée par ponction de chambre antérieure
(pca).
anticorps antitoxoplasmiques dans l'humeur aqueuse
Immunoglobulines totales dans l'humeur aqueuse
C=_________________________________________
anticorps antitoxoplasmiques sériques
Immunoglobulines totales sériques
Il y a production locale d'anticorps si C est supérieur à 3 et probable entre 2 et 3.
Dr Bessières, laboratoire de parasitologie et mycologie, Toulouse
-
Rangueil (France) :
Au niveau du sérum
Sérologie de la toxoplasmose sur le sérum :
L'absence d'anticorps
IgG
anti-toxoplasmiques permet d'exclure une
toxoplasmose
oculaire
La présence d'anticorps
IgG
anti-toxoplasmiques permet d'évoquer une
toxoplasmose
oculaire
: elle est à comparer à la sérologie de l'humeur aqueuse. Il est possible de
mettre en évidence une synthèse locale d'anticorps dans l'humeur aqueuse par le calcul
des charges immunitaires de l'humeur aqueuse et du sérum.
Au niveau de l'humeur aqueuse
Sérologie de l'humeur aqueuse :
L'absence d'anticorps spécifiques
IgG
anti
-
toxoplasmiques ne permet pas d'exclure une
toxoplasmose oculaire
La mise en évidence d'une synthèse locale d'anticorps
IgG
dans l'humeur aqueuse est le
témoin d'une toxoplasmose oculaire.
Il est possible de faire une recherche d'
ADN
toxoplasmique dans l'humeur aqueuse mais
un examen négatif ne permet pas d'exclure une toxoplasmose oculaire.